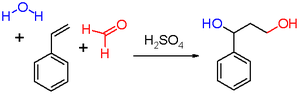
La reacción de Prins es una reacción orgánica que consiste en una adición electrófila de un aldehído o cetona a un alqueno o alquino seguida de la captura de un nucleófilo o la eliminación de un ion H + . [1] [2] [3] El resultado de la reacción depende de las condiciones de la reacción. Con agua y un ácido prótico tal como ácido sulfúrico como medio de reacción y formaldehído , el producto de reacción es un 1,3-diol ( 3 ). Cuando no hay agua, el intermedio catiónico pierde un protón para dar un alcohol alílico ( 4 ). Con un exceso de formaldehído y una temperatura de reacción baja, el producto de la reacción es un dioxano ( 5 ). Cuando el agua se reemplaza por ácido acético se forman los ésteres correspondientes .

Los reactivos originales empleados por el químico holandés Hendrik Jacobus Prins en su publicación de 1919 fueron estireno ( esquema 2 ), pineno , canfeno , eugenol , isosafrol y anetol . Estos procedimientos se han optimizado. [4]
Hendrik Jacobus Prins descubrió dos nuevas reacciones orgánicas durante su investigación doctoral en el año 1911-1912. La primera es la adición de un compuesto polihalógeno a olefinas y la segunda reacción es la adición catalizada por ácido de aldehídos a compuestos de olefina. Los primeros estudios sobre la reacción de Prins son de naturaleza exploratoria y no atrajeron mucha atención hasta 1937. El desarrollo del craqueo del petróleo en 1937 aumentó la producción de hidrocarburos insaturados. Como consecuencia, la disponibilidad comercial de olefinas inferiores junto con un aldehído producido a partir de la oxidación de parafina de bajo punto de ebullición aumentó la curiosidad por estudiar la condensación de olefina-aldehído. Más tarde, la reacción de Prins surgió como una poderosa técnica de formación de enlaces CO y CC en la síntesis de varias moléculas en síntesis orgánica. [5]
En 1937 se investigó la reacción como parte de la búsqueda de diolefinas para usar en caucho sintético .

El mecanismo de reacción para esta reacción se representa en el esquema 5. El reactivo carbonilo (2) es protonado por un ácido prótico y para el ion oxonio 3 resultante se pueden dibujar dos estructuras de resonancia . Este electrófilo participa en una adición electrófila con el alqueno al intermedio carbocatiónico 4. Se debe determinar exactamente cuánta carga positiva está presente en el átomo de carbono secundario en este intermedio para cada conjunto de reacción. Existe evidencia de la participación en grupos vecinos del oxígeno hidroxilo o de su átomo de carbono vecino. Cuando la reacción general tiene un alto grado de concertación , la carga acumulada será modesta.
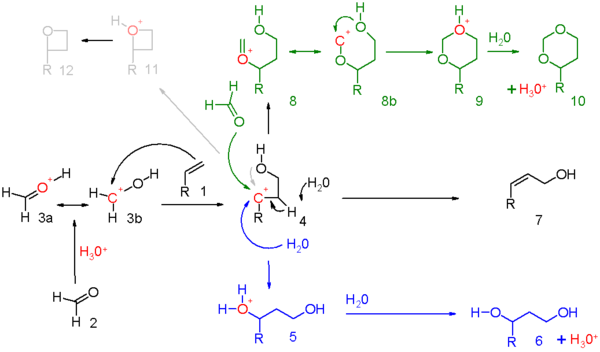
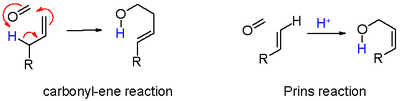
Los tres modos de reacción abiertos a este intermedio de oxocarbenio son :
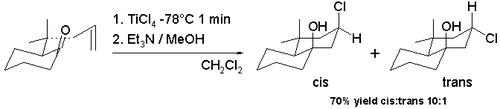
Existen muchas variaciones de la reacción de Prins porque se presta fácilmente a reacciones de ciclación y porque es posible capturar el ion oxocarbenio con una gran variedad de nucleófilos. La reacción halo-Prins es una de esas modificaciones con la sustitución de ácidos próticos y agua por ácidos de Lewis como el cloruro estánnico y el tribromuro de boro . El halógeno es ahora el nucleófilo que se recombina con el carbocatión. La ciclación de ciertas alil pulegonas en el esquema 7 con tetracloruro de titanio en diclorometano a -78 °C da acceso al esqueleto de decalina con el grupo hidroxilo y el grupo cloro predominantemente en configuración cis (91% cis). [7] Esta diastereoselectividad cis observada se debe a la formación intermedia de un alcóxido de triclorotitanio que hace posible una fácil entrega de cloro al ion carbocatión desde la misma cara. Se prefiere el isómero trans (98% cis) cuando se cambia a una reacción de tetracloruro de estaño a temperatura ambiente .
La reacción de Prins-pinacol es una reacción en cascada de una reacción de Prins y un reordenamiento de pinacol . El grupo carbonilo en el reactivo del esquema 8 [8] está enmascarado como un dimetil acetal y el grupo hidroxilo está enmascarado como un éter triisopropilsilílico (TIPS). Con el cloruro estánnico del ácido de Lewis, el ion oxonio se activa y el reordenamiento del pinacol del intermedio de Prins resultante da como resultado la contracción del anillo y la derivación de la carga positiva al éter TIPS que eventualmente forma un grupo aldehído en el producto final como una mezcla de cis y trans. isómeros con diastereoselectividad modesta.

El intermedio clave oxo-carbenio se puede formar por otras rutas además de la simple protonación de un carbonilo. En un paso clave de la síntesis de exiguólida, se formó mediante la protonación de un éster vinólogo : [9]

