El queratán sulfato ( KS ), también llamado queratosulfato , es cualquiera de varios glicosaminoglicanos (carbohidratos estructurales) sulfatados que se han encontrado especialmente en la córnea , el cartílago y el hueso . También se sintetiza en el sistema nervioso central , donde participa tanto en el desarrollo [1] como en la formación de la cicatriz glial tras una lesión. [2] Los sulfatos de queratán son moléculas grandes y altamente hidratadas que en las articulaciones pueden actuar como un cojín para absorber los golpes mecánicos .
Al igual que otros glicosaminoglicanos, el queratán sulfato es un polímero lineal que consta de una unidad disacárida repetida . El sulfato de queratán se presenta como un proteoglicano (PG) en el que las cadenas de KS están unidas a proteínas de la superficie celular o de la matriz extracelular , denominadas proteínas centrales. Las proteínas centrales del KS incluyen lumican , queratocán , mimecano , fibromodulina , PRELP , osteoadherina y agrecano .
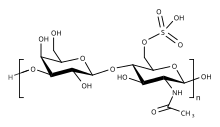
La unidad básica de disacárido repetitivo dentro del sulfato de queratán es -3 Gal β1-4 GlcNAc6S β1-. Este se puede sulfatar en la posición de carbono 6 (C6) de uno o ambos monosacáridos Gal o GlcNAc . Sin embargo, es mejor considerar que la estructura primaria detallada de tipos específicos de KS está compuesta por tres regiones: [3]
El monosacárido manosa se encuentra dentro de la región de enlace del queratán sulfato tipo I (KSI). Los disacáridos dentro de la región repetida de KSII pueden estar fucosilados y el ácido N-acetilneuramínico cubre el extremo de todas las cadenas de queratán sulfato tipo II (KSII) y hasta el 70% de las cadenas de tipo KSI. [4]
Las denominaciones KSI y KSII se asignaron originalmente en función del tipo de tejido del que se aisló el sulfato de queratán. KSI se aisló de tejido corneal y KSII de tejido esquelético . [5] [6] Existen diferencias menores en la composición de monosacáridos entre el KS extraído de ambas fuentes e incluso el KS extraído de la misma fuente. Sin embargo, se producen diferencias importantes en la forma en que cada tipo de SK se une a su proteína central. [7] Las designaciones KSI y KSII ahora se basan en estas diferencias en el enlace de proteínas. KSI está unido por N a aminoácidos de asparagina específicos a través de N -acetilglucosamina y KSII está unido a O a aminoácidos de serina o treonina específicos a través de N -acetilgalactosamina . [8] La clasificación del SK basada en tejidos ya no existe ya que se ha demostrado que los tipos de SK no son específicos de tejido. [4] También se ha aislado un tercer tipo de KS (KSIII) a partir de tejido cerebral que está unido mediante O a aminoácidos específicos de serina o treonina a través de manosa . [9]
La cantidad de KS que se encuentra en la córnea es 10 veces mayor que en el cartílago y entre 2 y 4 veces mayor que en otros tejidos. [10] Es producido por los queratocitos corneales [11] y se cree que desempeña un papel de amortiguador dinámico de la hidratación corneal. En un trastorno progresivo poco común llamado distrofia corneal macular (MCDC), la síntesis de queratán sulfato está ausente (MCDC tipo I) o es anormal (MCDC tipo II). [12]
La osteoadherina , la fibromodulina y PRELP son proteínas centrales que se encuentran en el hueso y el cartílago y que están modificadas por cadenas de KS unidas a N. Las cadenas KS unidas a osteoadherina y fibromodulina son más cortas que las que se encuentran en la córnea, normalmente de 8 a 9 unidades de disacárido de longitud. [13] Mientras que el KSI corneal se compone de una serie de dominios que muestran grados variables de sulfatación, el más largo de los cuales puede tener entre 8 y 32 unidades de disacárido de longitud. El terminal no reductor de Fibromodulin KS tiene una estructura más similar al terminal no reductor de un sulfato de queratán tipo KSII que al KSI corneal. Por lo tanto, se cree que la estructura de KS está determinada por la disponibilidad específica del tejido de las glicosiltransferasas en lugar del tipo de enlace con la proteína central. [4]
El cartílago KSII está casi completamente sulfatado y consta de monómeros disulfatados interrumpidos ocasionalmente por un único monómero de lactosamina monosulfatado . [8] La fucosilación también es común con la fucosa con enlace alfa presente en la posición del carbono 3 de la GlcNAc sulfatada , excepto en el caso de KSII traqueal donde esta característica está ausente.