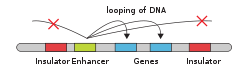

En genética , un potenciador es una región corta (50-1500 pb ) de ADN que puede unirse mediante proteínas ( activadores ) para aumentar la probabilidad de que se produzca la transcripción de un gen en particular. [1] [2] Estas proteínas generalmente se denominan factores de transcripción . Los potenciadores actúan en cis . Pueden ubicarse hasta 1 Mbp (1.000.000 de pb) de distancia del gen, aguas arriba o aguas abajo del sitio de inicio. [2] [3] Hay cientos de miles de potenciadores en el genoma humano. [2] Se encuentran tanto en procariotas como en eucariotas. [4]
El primer descubrimiento de un potenciador eucariota fue en el gen de la cadena pesada de inmunoglobulina en 1983. [5] [6] [7] Este potenciador, ubicado en el intrón grande , proporcionó una explicación para la activación transcripcional de los promotores del gen Vh reordenado mientras que los promotores del gen Vh no reordenados Los promotores permanecieron inactivos. [8] Últimamente, se ha demostrado que los potenciadores están involucrados en ciertas condiciones médicas, por ejemplo, la mielosupresión . [9] Desde 2022, los científicos han utilizado inteligencia artificial para diseñar potenciadores sintéticos y los han aplicado en sistemas animales, primero en una línea celular, [10] y un año después también in vivo. [11] [12]
En las células eucariotas la estructura del complejo de cromatina del ADN está plegada de una manera que imita funcionalmente el estado superenrollado característico del ADN procariótico , por lo que aunque el ADN potenciador puede estar lejos del gen de forma lineal, está espacialmente cerca del promotor . y gen. Esto le permite interactuar con los factores de transcripción generales y la ARN polimerasa II . [13] El mismo mecanismo es válido para los silenciadores en el genoma eucariota. Los silenciadores son antagonistas de los potenciadores que, cuando se unen a sus factores de transcripción adecuados llamados represores , reprimen la transcripción del gen. Los silenciadores y potenciadores pueden estar muy próximos entre sí o incluso pueden estar en la misma región, diferenciados únicamente por el factor de transcripción al que se une la región.
Un potenciador puede estar situado aguas arriba o aguas abajo del gen que regula. Además, no es necesario ubicar un potenciador cerca del sitio de inicio de la transcripción para afectar la transcripción, ya que se han encontrado algunos ubicados varios cientos de miles de pares de bases aguas arriba o aguas abajo del sitio de inicio. [14] Los potenciadores no actúan sobre la región promotora en sí, sino que están unidos por proteínas activadoras . Estas proteínas activadoras interactúan con el complejo mediador , que recluta la polimerasa II y los factores de transcripción generales que luego comienzan a transcribir los genes. Los potenciadores también se pueden encontrar dentro de los intrones. La orientación de un potenciador puede incluso invertirse sin afectar su función; Además, se puede extirpar un potenciador e insertarlo en otra parte del cromosoma y aún así afectar la transcripción genética. [15] Esa es una de las razones por las que los polimorfismos de los intrones pueden tener efectos aunque no estén traducidos . [ cita necesaria ] Los potenciadores también se pueden encontrar en la región exónica de un gen no relacionado [16] [17] [18] y pueden actuar sobre genes de otro cromosoma . [19]
Los potenciadores están unidos a p300-CBP y ChIP-seq puede predecir su ubicación frente a esta familia de coactivadores. [20] [21] [22] [23]

La expresión génica en mamíferos está regulada por muchos elementos reguladores en cis , incluidos los promotores centrales y los elementos proximales al promotor que se encuentran cerca de los sitios de inicio de la transcripción de los genes. Los promotores centrales son suficientes para dirigir el inicio de la transcripción, pero generalmente tienen una actividad basal baja. [24] Otros módulos reguladores cis importantes se localizan en regiones del ADN que están distantes de los sitios de inicio de la transcripción. Estos incluyen potenciadores, silenciadores , aisladores y elementos de anclaje. [25] Entre esta constelación de elementos, los potenciadores y sus factores de transcripción asociados tienen un papel principal en la regulación de la expresión génica. [26] Un potenciador localizado en una región del ADN distante del promotor de un gen puede tener un efecto muy grande en la expresión génica, y algunos genes experimentan una expresión aumentada hasta 100 veces debido a un potenciador activado. [27]
Los potenciadores son regiones del genoma que son importantes elementos reguladores de genes. Los potenciadores controlan los programas de expresión génica específicos de cada tipo de célula, con mayor frecuencia recorriendo largas distancias para acercarse físicamente a los promotores de sus genes diana. [28] Si bien hay cientos de miles de regiones de ADN potenciadoras, [2] para un tipo particular de tejido sólo potenciadores específicos se acercan a los promotores que regulan. En un estudio de neuronas corticales del cerebro, se encontraron 24.937 bucles que llevaban potenciadores a sus promotores objetivo. [27] Múltiples potenciadores, cada uno a menudo a decenas o cientos de miles de nucleótidos distantes de sus genes diana, se enlazan con los promotores de sus genes diana y pueden coordinarse entre sí para controlar la expresión de su gen diana común. [28]
La ilustración esquemática de esta sección muestra un potenciador dando vueltas para acercarse físicamente al promotor de un gen diana. El bucle se estabiliza mediante un dímero de una proteína conectora (por ejemplo, dímero de CTCF o YY1 ), con un miembro del dímero anclado a su motivo de unión en el potenciador y el otro miembro anclado a su motivo de unión en el promotor (representado por el zigzags rojos en la ilustración). [29] Varios factores de transcripción específicos de la función celular (hay alrededor de 1.600 factores de transcripción en una célula humana [30] ) generalmente se unen a motivos específicos en un potenciador [31] y una pequeña combinación de estos factores de transcripción unidos al potenciador, cuando se acercan a un promotor mediante un bucle de ADN, gobiernan el nivel de transcripción del gen diana. El mediador (un complejo que generalmente consta de aproximadamente 26 proteínas en una estructura que interactúa) comunica señales regulatorias desde factores de transcripción potenciadores unidos al ADN directamente a la enzima ARN polimerasa II (pol II) unida al promotor. [32]
Los potenciadores, cuando están activos, generalmente se transcriben a partir de ambas cadenas de ADN con ARN polimerasas que actúan en dos direcciones diferentes, produciendo dos ARN potenciadores (eRNA), como se ilustra en la figura. [33] Al igual que los ARNm , estos ARNe suelen estar protegidos por su tapa 5′ . [34] Un potenciador inactivo puede estar unido a un factor de transcripción inactivo. La fosforilación del factor de transcripción puede activarlo y ese factor de transcripción activado puede luego activar el potenciador al que está unido (ver la pequeña estrella roja que representa la fosforilación del factor de transcripción unido al potenciador en la ilustración). [35] Un potenciador activado comienza la transcripción de su ARN antes de activar la transcripción del ARN mensajero de su gen objetivo. [36]
A partir de 2005 [actualizar], existen dos teorías diferentes sobre el procesamiento de la información que se produce en los potenciadores: [37]
HACNS1 (también conocido como CENTG2 y ubicado en la Región Acelerada Humana 2) es un potenciador genético "que puede haber contribuido a la evolución del pulgar humano excepcionalmente oponible , y posiblemente también a modificaciones en el tobillo o el pie que permiten a los humanos caminar sobre dos piernas". La evidencia hasta la fecha muestra que de las 110.000 secuencias potenciadoras de genes identificadas en el genoma humano , HACNS1 ha sufrido el mayor cambio durante la evolución de los humanos tras la división con los antepasados de los chimpancés . [ cita necesaria ]
Se ha descrito un potenciador cercano al gen GADD45g que puede regular el crecimiento cerebral en chimpancés y otros mamíferos, pero no en humanos. [38] El regulador GADD45G en ratones y chimpancés está activo en regiones del cerebro donde se encuentran las células que forman la corteza, el prosencéfalo ventral y el tálamo y puede suprimir una mayor neurogénesis. La pérdida del potenciador GADD45G en humanos puede contribuir a un aumento de ciertas poblaciones neuronales y a la expansión del prosencéfalo en humanos. [ cita necesaria ]
El desarrollo, la diferenciación y el crecimiento de células y tejidos requieren patrones de expresión genética regulados con precisión . Los potenciadores funcionan como elementos reguladores cis para mediar en el control espacial y temporal del desarrollo al activar la transcripción en células específicas y/o reprimirla en otras células. Por tanto, la combinación particular de factores de transcripción y otras proteínas de unión al ADN en un tejido en desarrollo controla qué genes se expresarán en ese tejido. Los potenciadores permiten utilizar el mismo gen en diversos procesos en el espacio y el tiempo. [ cita necesaria ] [39]
Tradicionalmente, los potenciadores se identificaban mediante técnicas de trampa de potenciadores utilizando un gen informador o mediante análisis de secuencia comparativo y genómica computacional. En modelos genéticamente manejables como la mosca de la fruta Drosophila melanogaster , por ejemplo, una construcción indicadora como el gen lacZ puede integrarse aleatoriamente en el genoma utilizando un transposón del elemento P. Si el gen indicador se integra cerca de un potenciador, su expresión reflejará el patrón de expresión impulsado por ese potenciador. Por tanto, teñir las moscas para determinar la expresión o actividad de LacZ y clonar la secuencia que rodea el sitio de integración permite la identificación de la secuencia potenciadora. [40]
Sin embargo, el desarrollo de tecnologías genómicas y epigenómicas ha cambiado drásticamente las perspectivas para el descubrimiento de módulos reguladores cis (CRM). Los métodos de secuenciación de próxima generación (NGS) ahora permiten ensayos de descubrimiento de CRM funcionales de alto rendimiento y cantidades cada vez mayores de datos disponibles, incluidas bibliotecas a gran escala de motivos de sitios de unión de factores de transcripción (TFBS) , colecciones de CRM validados y anotados, y datos epigenéticos extensos en muchos tipos de células, están haciendo que el descubrimiento de CRM computacional preciso sea un objetivo alcanzable. Un ejemplo de enfoque basado en NGS llamado DNase-seq ha permitido la identificación de regiones de cromatina abiertas o empobrecidas en nucleosomas, que pueden contener CRM. Más recientemente se han desarrollado técnicas como ATAC-seq que requieren menos material de partida. Las regiones empobrecidas en nucleosomas se pueden identificar in vivo mediante la expresión de Dam metilasa , lo que permite un mayor control de la identificación del potenciador específico del tipo celular. [41] Los métodos computacionales incluyen genómica comparativa , agrupación de sitios de unión de TF conocidos o previstos y enfoques supervisados de aprendizaje automático entrenados en CRM conocidos. Todos estos métodos han demostrado ser eficaces para el descubrimiento de CRM, pero cada uno tiene sus propias consideraciones y limitaciones, y cada uno está sujeto a un número mayor o menor de identificaciones falsas positivas. [42] En el enfoque de genómica comparada , la conservación de la secuencia de regiones no codificantes puede ser indicativa de potenciadores. Se alinean secuencias de múltiples especies y las regiones conservadas se identifican computacionalmente. [43] Las secuencias identificadas luego se pueden unir a un gen indicador, como la proteína verde fluorescente o lacZ, para determinar el patrón in vivo de expresión genética producido por el potenciador cuando se inyecta en un embrión. La expresión del ARNm del indicador se puede visualizar mediante hibridación in situ , que proporciona una medida más directa de la actividad potenciadora, ya que no está sujeto a las complejidades de la traducción y el plegamiento de proteínas . Aunque mucha evidencia ha apuntado a la conservación de secuencias para potenciadores críticos del desarrollo, otros trabajos han demostrado que la función de los potenciadores se puede conservar con poca o ninguna conservación de la secuencia primaria. Por ejemplo, los potenciadores de RET en humanos tienen muy poca conservación de secuencia en comparación con los del pez cebra., sin embargo, las secuencias de ambas especies producen patrones casi idénticos de expresión del gen informador en el pez cebra. [43] De manera similar, en insectos muy divergentes (separados por alrededor de 350 millones de años), se encontró que patrones de expresión genética similares de varios genes clave estaban regulados a través de CRM constituidos de manera similar, aunque estos CRM no muestran ninguna conservación de secuencia apreciable detectable mediante alineación de secuencia estándar. métodos como BLAST . [44]
Los potenciadores que determinan la segmentación temprana en embriones de Drosophila melanogaster se encuentran entre los potenciadores del desarrollo mejor caracterizados. En el embrión temprano de mosca, los factores de transcripción del gen gap son responsables de activar y reprimir una serie de genes de segmentación, como los genes de la regla del par . Los genes gap se expresan en bloques a lo largo del eje anteroposterior de la mosca junto con otros factores de transcripción de efecto materno , creando así zonas dentro de las cuales se expresan diferentes combinaciones de factores de transcripción. Los genes de regla de pares están separados entre sí por células que no los expresan. Además, las franjas de expresión de diferentes genes de regla de par están compensadas por unos pocos diámetros celulares entre sí. Por lo tanto, combinaciones únicas de expresión genética de regla de par crean dominios espaciales a lo largo del eje anteroposterior para configurar cada uno de los 14 segmentos individuales. El potenciador de 480 pb responsable de impulsar la raya afilada dos del gen de la regla del par omitida ( eve ) ha sido bien caracterizado. El potenciador contiene 12 sitios de unión diferentes para factores de transcripción de genes maternos y gap. Los sitios de activación y represión se superponen en secuencia. Eve solo se expresa en una franja estrecha de células que contienen altas concentraciones de activadores y bajas concentraciones de represores para esta secuencia potenciadora. Otras regiones potenciadoras impulsan la expresión de víspera en otras seis franjas del embrión. [45]
Establecer ejes corporales es un paso crítico en el desarrollo animal. Durante el desarrollo embrionario del ratón, Nodal , un ligando de la superfamilia del factor de crecimiento transformante beta , es un gen clave involucrado en el modelado tanto del eje anteroposterior como del eje izquierda-derecha del embrión temprano. El gen Nodal contiene dos potenciadores: el potenciador del epiblasto proximal (PEE) y el potenciador asimétrico (ASE). El PEE está aguas arriba del gen Nodal e impulsa la expresión nodal en la porción de la línea primitiva que se diferenciará en el nodo (también conocido como nodo primitivo ). [46] El PEE activa la expresión nodal en respuesta a una combinación de señalización Wnt más una segunda señal desconocida; por tanto, un miembro de la familia de factores de transcripción LEF/TCF probablemente se une a un sitio de unión de TCF en las células del nódulo. La difusión de Nodal lejos del nodo forma un gradiente que luego modela la extensión del eje anteroposterior del embrión. [47] El ASE es un potenciador intrónico unido por el factor de transcripción Fox1 del dominio de la cabeza de la horquilla . Al principio del desarrollo, la expresión nodal impulsada por Fox1 establece el endodermo visceral. Más adelante en el desarrollo, la unión de Fox1 al ASE impulsa la expresión nodal en el lado izquierdo del mesodermo de la placa lateral , estableciendo así la asimetría izquierda-derecha necesaria para el desarrollo asimétrico de órganos en el mesodermo. [48]
El establecimiento de tres capas germinales durante la gastrulación es otro paso crítico en el desarrollo animal. Cada una de las tres capas germinales tiene patrones únicos de expresión genética que promueven su diferenciación y desarrollo. El endodermo se especifica en las primeras etapas del desarrollo mediante la expresión de Gata4 , y Gata4 dirige la morfogénesis intestinal más adelante. La expresión de Gata4 está controlada en el embrión temprano por un potenciador intrónico que se une a otro factor de transcripción del dominio forkhead, FoxA2. Inicialmente, el potenciador impulsa una amplia expresión genética en todo el embrión, pero la expresión rápidamente se restringe al endodermo, lo que sugiere que otros represores pueden estar involucrados en su restricción. Al final del desarrollo, el mismo potenciador restringe la expresión a los tejidos que se convertirán en el estómago y el páncreas. Un potenciador adicional es responsable de mantener la expresión de Gata4 en el endodermo durante las etapas intermedias del desarrollo intestinal. [49]
Algunos genes implicados en procesos críticos del desarrollo contienen múltiples potenciadores de funciones superpuestas. Los potenciadores secundarios, o "potenciadores de sombra", se pueden encontrar a muchas kilobases de distancia del potenciador primario ("primario" generalmente se refiere al primer potenciador descubierto, que a menudo está más cerca del gen que regula). Por sí solo, cada potenciador impulsa patrones de expresión genética casi idénticos. ¿Son los dos potenciadores realmente redundantes? Trabajos recientes han demostrado que múltiples potenciadores permiten que las moscas de la fruta sobrevivan a perturbaciones ambientales, como un aumento de temperatura. Cuando se eleva a una temperatura elevada, un solo potenciador a veces no logra impulsar el patrón completo de expresión, mientras que la presencia de ambos potenciadores permite la expresión genética normal. [50]
Un tema de investigación en biología del desarrollo evolutivo ("evo-devo") es investigar el papel de los potenciadores y otros elementos reguladores cis en la producción de cambios morfológicos a través de diferencias de desarrollo entre especies. [ cita necesaria ]
Trabajos recientes han investigado el papel de los potenciadores en los cambios morfológicos en el pez espinoso de tres espinas . Los espinosos existen tanto en ambientes marinos como de agua dulce, pero los espinosos en muchas poblaciones de agua dulce han perdido por completo sus aletas pélvicas (apéndices homólogos a la extremidad posterior de los tetrápodos).
Pitx1 es un gen homeobox implicado en el desarrollo de las extremidades posteriores en los vertebrados. Los análisis genéticos preliminares indicaron que los cambios en la expresión de este gen eran responsables de la reducción pélvica de los espinosos. Los peces que expresan únicamente el alelo de agua dulce de Pitx1 no tienen espinas pélvicas, mientras que los peces que expresan un alelo marino conservan espinas pélvicas. Una caracterización más exhaustiva mostró que una secuencia potenciadora de 500 pares de bases es responsable de activar la expresión de Pitx1 en la yema de la aleta posterior. Este potenciador está ubicado cerca de un sitio cromosómico frágil : una secuencia de ADN que probablemente se rompa y, por lo tanto, es más probable que mute como resultado de una reparación imprecisa del ADN . Este sitio frágil ha causado pérdidas repetidas e independientes del potenciador responsable de impulsar la expresión de Pitx1 en las espinas pélvicas en poblaciones aisladas de agua dulce, y sin este potenciador, los peces de agua dulce no pueden desarrollar espinas pélvicas. [51]
Los patrones de pigmentación proporcionan una de las diferencias más llamativas y fáciles de calificar entre las diferentes especies de animales. La pigmentación del ala de Drosophila ha demostrado ser un sistema particularmente adecuado para estudiar el desarrollo de fenotipos de pigmentación complejos. El ala de Drosophila guttifera tiene 12 manchas de pigmentación oscuras y 4 parches internervados de color gris más claro. Las manchas de pigmentación surgen de la expresión del gen amarillo , cuyo producto produce melanina negra . Trabajos recientes han demostrado que dos potenciadores en el gen amarillo producen expresión genética precisamente en este patrón: el potenciador de la mancha venosa impulsa la expresión del gen indicador en los 12 puntos, y el potenciador del tono intervenoso impulsa la expresión del indicador en los 4 parches distintos. Estos dos potenciadores responden a la vía de señalización Wnt , que se activa mediante la expresión sin alas en todas las ubicaciones pigmentadas. Por lo tanto, en la evolución del fenotipo de pigmentación complejo , el gen del pigmento amarillo evolucionó potenciadores que respondían a la señal sin alas y la expresión sin alas evolucionó en nuevas ubicaciones para producir nuevos patrones de alas. [52]
Cada célula normalmente contiene varios cientos de una clase especial de potenciadores que se extienden a lo largo de secuencias de ADN de muchas kilobases de longitud, llamados " superpotenciadores ". [53] Estos potenciadores contienen una gran cantidad de sitios de unión para factores de transcripción inducibles específicos de secuencia y regulan la expresión de genes implicados en la diferenciación celular. [54] Durante la inflamación , el factor de transcripción NF-κB facilita la remodelación de la cromatina de una manera que redistribuye selectivamente los cofactores de los potenciadores de alta ocupación, reprimiendo así los genes implicados en el mantenimiento de la identidad celular cuya expresión mejoran; al mismo tiempo, esta remodelación y redistribución impulsada por F-κB activa otros potenciadores que guían los cambios en la función celular a través de la inflamación. [55] [56] Como resultado, la inflamación reprograma las células, alterando sus interacciones con el resto del tejido y con el sistema inmunológico. [57] [58] En el cáncer, las proteínas que controlan la actividad de NF-κB están desreguladas, lo que permite que las células malignas disminuyan su dependencia de las interacciones con el tejido local y dificultan su vigilancia por parte del sistema inmunológico . [59] [60]
Los elementos reguladores sintéticos, como los potenciadores, prometen ser una herramienta poderosa para dirigir productos genéticos a tipos de células particulares con el fin de tratar enfermedades activando genes beneficiosos o deteniendo estados celulares aberrantes.
Desde 2022, la inteligencia artificial y las estrategias de aprendizaje por transferencia han permitido comprender mejor las características de las secuencias reguladoras de ADN, la predicción y el diseño de potenciadores sintéticos. [61] [62]
Sobre la base del trabajo en cultivos celulares, [63] los potenciadores sintéticos se aplicaron con éxito a organismos vivos completos en 2023. Utilizando redes neuronales profundas , los científicos simularon la evolución de secuencias de ADN para analizar la aparición de características que subyacen a la función del potenciador. Esto permitió el diseño y producción de una gama de potenciadores sintéticos funcionales para diferentes tipos de células del cerebro de la mosca de la fruta. [64] Un segundo enfoque entrenó modelos de inteligencia artificial con datos de accesibilidad al ADN unicelular y transfirió los modelos aprendidos a la predicción de potenciadores para tejidos seleccionados en el embrión de la mosca de la fruta. Estos modelos de predicción de potenciadores se utilizaron para diseñar potenciadores sintéticos para el sistema nervioso, el cerebro, los músculos, la epidermis y el intestino. [sesenta y cinco]