
La respuesta de las células B policlonales es un modo natural de respuesta inmunitaria que exhibe el sistema inmunitario adaptativo de los mamíferos . Asegura que un único antígeno sea reconocido y atacado a través de sus partes superpuestas, llamadas epítopos , por múltiples clones de células B. [ 1] [2]
En el curso de una respuesta inmunitaria normal, el sistema inmunitario reconoce partes de los patógenos (p. ej. , bacterias ) como extrañas (no propias) y las elimina o neutraliza de manera eficaz para reducir su daño potencial. Una sustancia reconocible de este tipo se denomina antígeno . El sistema inmunitario puede responder de múltiples maneras a un antígeno; una característica clave de esta respuesta es la producción de anticuerpos por parte de las células B (o linfocitos B) que involucran un brazo del sistema inmunitario conocido como inmunidad humoral . Los anticuerpos son solubles y no requieren contacto directo de célula a célula entre el patógeno y la célula B para funcionar.
Los antígenos pueden ser sustancias grandes y complejas, y cualquier anticuerpo individual solo puede unirse a un área pequeña y específica del antígeno. En consecuencia, una respuesta inmunitaria eficaz a menudo implica la producción de muchos anticuerpos diferentes por muchas células B diferentes contra el mismo antígeno. De ahí el término "policlonal", que deriva de las palabras poli , que significa muchos, y clones del griego klōn , que significa brote o ramita; [3] [4] [5] un clon es un grupo de células que surgen de una célula "madre" común. Los anticuerpos así producidos en una respuesta policlonal se conocen como anticuerpos policlonales . Los anticuerpos policlonales heterogéneos son distintos de las moléculas de anticuerpos monoclonales , que son idénticos y reaccionan solo contra un único epítopo, es decir, son más específicos.
Aunque la respuesta policlonal confiere ventajas al sistema inmune, en particular una mayor probabilidad de reaccionar contra patógenos, también aumenta las posibilidades de desarrollar ciertas enfermedades autoinmunes resultantes de la reacción del sistema inmune contra moléculas nativas producidas dentro del huésped.
Las enfermedades que pueden transmitirse de un organismo a otro se conocen como enfermedades infecciosas , y el agente biológico causal involucrado se conoce como patógeno . El proceso por el cual el patógeno se introduce en el cuerpo se conoce como inoculación , [nota 1] [6] y el organismo al que afecta se conoce como huésped biológico . Cuando el patógeno se establece en un paso conocido como colonización , [7] puede resultar en una infección , [7] dañando en consecuencia al huésped directamente o a través de las sustancias dañinas llamadas toxinas que puede producir. [7] Esto da como resultado los diversos síntomas y signos característicos de una enfermedad infecciosa como la neumonía o la difteria .
La lucha contra las diversas enfermedades infecciosas es muy importante para la supervivencia del organismo susceptible, en particular, y de la especie, en general. Esto lo consigue el huésped eliminando el patógeno y sus toxinas o haciéndolos no funcionales. El conjunto de diversas células , tejidos y órganos que se especializa en proteger al cuerpo contra las infecciones se conoce como sistema inmunitario . El sistema inmunitario logra esto a través del contacto directo de ciertos glóbulos blancos con el patógeno invasor, involucrando un brazo del sistema inmunitario conocido como inmunidad celular , o produciendo sustancias que se desplazan a sitios distantes de donde se producen, "buscan" las células y toxinas causantes de la enfermedad al unirse específicamente [nota 2] con ellas y las neutralizan en el proceso, conocido como el brazo humoral del sistema inmunitario. Estas sustancias se conocen como anticuerpos solubles y desempeñan funciones importantes para contrarrestar las infecciones. [nota 3] [8]
Los anticuerpos cumplen diversas funciones para proteger al huésped contra el patógeno. Las formas solubles que llevan a cabo estas funciones son producidas por las células B plasmáticas , un tipo de glóbulo blanco. Esta producción está estrictamente regulada y requiere la activación de las células B por las células T activadas (otro tipo de glóbulo blanco), que es un procedimiento secuencial. Los principales pasos implicados son: [9]

Los patógenos sintetizan proteínas que pueden servir como antígenos " reconocibles " ; pueden expresar las moléculas en su superficie o liberarlas al entorno (fluidos corporales). Lo que hace que estas sustancias sean reconocibles es que se unen de forma muy específica y algo fuerte a ciertas proteínas del huésped llamadas anticuerpos . Los mismos anticuerpos pueden anclarse a la superficie de las células del sistema inmunitario, en cuyo caso sirven como receptores , o pueden secretarse en la sangre, conocidos como anticuerpos solubles. A escala molecular, las proteínas son relativamente grandes, por lo que no pueden reconocerse como un todo; en cambio, pueden reconocerse sus segmentos, llamados epítopos . [1] Un epítopo entra en contacto con una región muy pequeña (de 15 a 22 aminoácidos) de la molécula de anticuerpo; esta región se conoce como paratopo . [1] En el sistema inmunitario, los anticuerpos unidos a la membrana son el receptor de células B (BCR). Además, aunque el receptor de células T no está clasificado bioquímicamente como un anticuerpo, cumple una función similar en el sentido de que se une específicamente a epítopos complejados con moléculas del complejo mayor de histocompatibilidad (MHC). [nota 5] [10] La unión entre un paratopo y su antígeno correspondiente es muy específica, debido a su estructura, y está guiada por varios enlaces no covalentes , no muy diferente del emparejamiento de otros tipos de ligandos (cualquier átomo, ion o molécula que se une a cualquier receptor con al menos cierto grado de especificidad y fuerza ). La especificidad de la unión no surge de un tipo de interacción rígida de cerradura y llave , sino que requiere que tanto el paratopo como el epítopo experimenten ligeros cambios conformacionales en presencia del otro. [11]
En la figura de la izquierda, se ha demostrado que los diversos segmentos que forman el epítopo son continuamente colineales, lo que significa que se han mostrado como secuenciales; sin embargo, para la situación que se analiza aquí (es decir, el reconocimiento del antígeno por parte de la célula B), esta explicación es demasiado simplista. Dichos epítopos se conocen como epítopos secuenciales o lineales , ya que todos los aminoácidos que contienen están en la misma secuencia (línea). Este modo de reconocimiento solo es posible cuando el péptido es pequeño (alrededor de seis a ocho aminoácidos de longitud), [1] y lo emplean las células T (linfocitos T).
Sin embargo, las células B de memoria/naive reconocen las proteínas intactas presentes en la superficie del patógeno. [nota 6] En esta situación, la proteína en su estructura terciaria está tan plegada que algunos bucles de aminoácidos llegan a estar en el interior de la proteína, y los segmentos que los flanquean pueden estar en la superficie. El paratopo en el receptor de células B entra en contacto solo con aquellos aminoácidos que se encuentran en la superficie de la proteína. Los aminoácidos de la superficie pueden en realidad ser discontinuos en la estructura primaria de la proteína , pero se yuxtaponen debido a los complejos patrones de plegamiento de la proteína (como en la figura adjunta). Estos epítopos se conocen como epítopos conformacionales y tienden a ser más largos (15-22 residuos de aminoácidos) que los epítopos lineales. [1] De la misma manera, los anticuerpos producidos por las células plasmáticas que pertenecen al mismo clon se unirían a los mismos epítopos conformacionales en las proteínas del patógeno. [12] [13] [14] [15]
La unión de un antígeno específico con las moléculas BCR correspondientes da como resultado una mayor producción de las moléculas MHC-II. Esto adquiere importancia ya que lo mismo no sucede cuando el mismo antígeno se internaliza mediante un proceso relativamente inespecífico llamado pinocitosis , en el que el antígeno con el líquido circundante es "bebido" como una pequeña vesícula por la célula B. [16] Por lo tanto, un antígeno de este tipo se conoce como un antígeno inespecífico y no conduce a la activación de la célula B ni a la posterior producción de anticuerpos contra ella.
Los macrófagos y las células relacionadas emplean un mecanismo diferente para reconocer al patógeno. Sus receptores reconocen ciertos motivos presentes en el patógeno invasor que es muy poco probable que estén presentes en una célula huésped. Dichos motivos repetitivos son reconocidos por receptores de reconocimiento de patrones (PRR) como los receptores tipo Toll (TLR) expresados por los macrófagos. [1] [17] Dado que el mismo receptor podría unirse a un motivo dado presente en superficies de microorganismos muy dispares , este modo de reconocimiento es relativamente inespecífico y constituye una respuesta inmune innata .

Después de reconocer un antígeno, una célula presentadora de antígeno como el macrófago o el linfocito B lo engulle completamente mediante un proceso llamado fagocitosis . La partícula engullida, junto con algún material que la rodea, forma la vesícula endocítica (el fagosoma ), que se fusiona con los lisosomas . Dentro del lisosoma, el antígeno se descompone en pedazos más pequeños llamados péptidos por proteasas ( enzimas que degradan proteínas más grandes). Luego, los péptidos individuales se complejan con moléculas del complejo mayor de histocompatibilidad clase II ( MHC clase II ) ubicadas en el lisosoma; este método de "manipulación" del antígeno se conoce como la vía exógena o endocítica de procesamiento de antígeno en contraste con la vía endógena o citosólica , [17] [18] [19] que compleja las proteínas anormales producidas dentro de la célula (por ejemplo, bajo la influencia de una infección viral o en una célula tumoral ) con moléculas de MHC clase I.
También se ha demostrado una vía alternativa de procesamiento endocítico en la que ciertas proteínas, como el fibrinógeno y la mioglobina, pueden unirse en conjunto a las moléculas MHC-II después de que se desnaturalizan y se reducen sus enlaces disulfuro (rompiendo el enlace mediante la adición de átomos de hidrógeno a través de él). Las proteasas luego degradan las regiones expuestas del complejo proteína-MHC II. [19]
Después de que el antígeno procesado (péptido) se une a la molécula MHC, ambos migran juntos a la membrana celular , donde se exhiben (elaboran) como un complejo que puede ser reconocido por el CD4+ (célula T colaboradora) , un tipo de glóbulo blanco. [nota 7] [20] Esto se conoce como presentación de antígeno. Sin embargo, los epítopos (epítopos conformacionales) que son reconocidos por la célula B antes de su digestión pueden no ser los mismos que se presentan a la célula T colaboradora. Además, una célula B puede presentar diferentes péptidos complejos con diferentes moléculas MHC-II. [16]
Las células CD4+ a través de su complejo receptor de células T- CD3 reconocen las moléculas MHC II unidas al epítopo en la superficie de las células presentadoras de antígenos y se "activan" . Tras esta activación, estas células T proliferan y se diferencian en células Th 1 o Th 2. [ 16] [21] Esto hace que produzcan señales químicas solubles que promueven su propia supervivencia. Sin embargo, otra función importante que llevan a cabo es la estimulación de las células B estableciendo contacto físico directo con ellas. [10]
La estimulación completa de las células T colaboradoras requiere que la molécula B7 presente en la célula presentadora de antígeno se una a la molécula CD28 presente en la superficie de la célula T (en estrecha proximidad con el receptor de la célula T). [10] Asimismo, también es necesaria una segunda interacción entre el ligando CD40 o CD154 ( CD40L ) presente en la superficie de la célula T y el CD40 presente en la superficie de la célula B. [21] Las mismas interacciones que estimulan a la célula T colaboradora también estimulan a la célula B, de ahí el término coestimulación . Todo el mecanismo asegura que una célula T activada solo estimule a una célula B que reconozca el antígeno que contiene el mismo epítopo que reconoce el receptor de células T de la célula T colaboradora "coestimulante". La célula B se estimula, aparte de la coestimulación directa, por ciertos factores de crecimiento, a saber, las interleucinas 2 , 4 , 5 y 6 de forma paracrina . Estos factores suelen ser producidos por la célula T colaboradora recién activada. [22] Sin embargo, esta activación ocurre sólo después de que el receptor de células B presente en una célula B de memoria o ingenua se hubiera unido al epítopo correspondiente, sin el cual los pasos iniciales de la fagocitosis y el procesamiento del antígeno no habrían ocurrido.
Una célula B ingenua (o inexperta ) es aquella que pertenece a un clon que nunca ha encontrado el epítopo al que es específica. Por el contrario, una célula B de memoria es aquella que deriva de una célula B ingenua o de memoria activada. La activación de una célula B ingenua o de memoria es seguida por una proliferación múltiple de esa célula B en particular, la mayor parte de cuya progenie se diferencia terminalmente en células B plasmáticas ; [nota 8] el resto sobrevive como células B de memoria. Por lo tanto, cuando las células ingenuas que pertenecen a un clon particular encuentran su antígeno específico para dar lugar a las células plasmáticas, y también dejan unas pocas células de memoria, esto se conoce como la respuesta inmune primaria . En el curso de la proliferación de este clon, los genes del receptor de células B pueden sufrir mutaciones frecuentes (una de cada dos divisiones celulares) [8] en los genes que codifican paratopos de anticuerpos. Estas mutaciones frecuentes se denominan hipermutación somática . Cada una de estas mutaciones altera ligeramente la capacidad de unión del paratopo al epítopo, creando nuevos clones de células B en el proceso. Algunos de los paratopos recién creados se unen con más fuerza al mismo epítopo (lo que lleva a la selección de los clones que los poseen), lo que se conoce como maduración de la afinidad . [nota 9] [8] [21] Otros paratopos se unen mejor a epítopos que son ligeramente diferentes del epítopo original que había estimulado la proliferación. Las variaciones en la estructura del epítopo también suelen producirse por mutaciones en los genes del patógeno que codifican su antígeno. La hipermutación somática, por tanto, hace que los receptores de células B y los anticuerpos solubles en encuentros posteriores con antígenos, sean más inclusivos en su potencial de reconocimiento de antígenos de epítopos alterados , además de otorgar una mayor especificidad para el antígeno que indujo la proliferación en primer lugar. Cuando las células de memoria son estimuladas por el antígeno para producir células plasmáticas (como en la respuesta primaria del clon), y dejan aún más células de memoria en el proceso, esto se conoce como una respuesta inmune secundaria , [21] que se traduce en una mayor cantidad de células plasmáticas y una tasa más rápida de producción de anticuerpos que dura períodos más largos. Las células B de memoria producidas como parte de la respuesta secundaria reconocen el antígeno correspondiente más rápido y se unen con más fuerza a él (es decir, mayor afinidad de unión) debido a la maduración de la afinidad. Los anticuerpos solubles producidos por el clon muestran una mejora similar en la unión al antígeno. [21]
Las respuestas son de naturaleza policlonal, ya que cada clon se especializa de alguna manera en producir anticuerpos contra un epítopo determinado y porque cada antígeno contiene múltiples epítopos, cada uno de los cuales a su vez puede ser reconocido por más de un clon de células B. Para poder reaccionar ante innumerables antígenos, así como ante múltiples epítopos constituyentes, el sistema inmunológico requiere la capacidad de reconocer una gran cantidad de epítopos en total, es decir, debe haber una gran diversidad de clones de células B.
Las células B de memoria y las células B ingenuas normalmente existen en cantidades relativamente pequeñas. Como el cuerpo necesita poder responder a una gran cantidad de patógenos potenciales, mantiene un grupo de células B con una amplia gama de especificidades. [17] En consecuencia, si bien casi siempre hay al menos una célula B (ingenua o de memoria) capaz de responder a cualquier epítopo dado (de todos los que el sistema inmunológico puede combatir), hay muy pocos duplicados exactos. Sin embargo, cuando una sola célula B encuentra un antígeno al que puede unirse, puede proliferar muy rápidamente. [21] Un grupo de células de este tipo con idéntica especificidad hacia el epítopo se conoce como clon y se deriva de una célula "madre" común. Todas las células B "hijas" coinciden con la célula "madre" original en su especificidad de epítopo y secretan anticuerpos con parátopos idénticos. Estos anticuerpos son anticuerpos monoclonales , ya que derivan de clones de la misma célula madre. Una respuesta policlonal es aquella en la que los clones de múltiples células B reaccionan al mismo antígeno.

Un único antígeno puede considerarse como una secuencia de múltiples epítopos superpuestos. Muchos clones de células B únicos pueden unirse a los epítopos individuales. Esto imparte una multiplicidad aún mayor a la respuesta general. [3] Todas estas células B pueden activarse y producir grandes colonias de clones de células plasmáticas, cada una de las cuales puede secretar hasta 1000 moléculas de anticuerpos contra cada epítopo por segundo. [21]
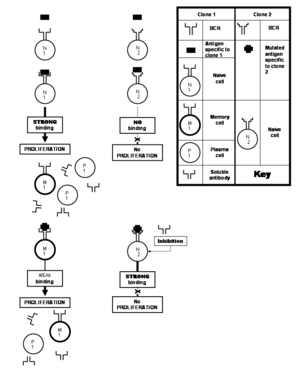
Además de que las distintas células B reaccionan a distintos epítopos del mismo antígeno, las células B pertenecientes a distintos clones también pueden reaccionar al mismo epítopo. Se dice que un epítopo que puede ser atacado por muchas células B diferentes es altamente inmunogénico . En estos casos, las afinidades de unión de los respectivos pares epítopo-parátopo varían, y algunos clones de células B producen anticuerpos que se unen fuertemente al epítopo, mientras que otros producen anticuerpos que se unen débilmente. [1]
Los clones que se unen a un epítopo particular con mayor fuerza tienen más probabilidades de ser seleccionados para una mayor proliferación en los centros germinales de los folículos en varios tejidos linfoides como los ganglios linfáticos . Esto no es muy diferente de la selección natural : los clones se seleccionan por su aptitud para atacar los epítopos (fuerza de unión) en el patógeno encontrado. [23] Lo que hace que la analogía sea aún más fuerte es que los linfocitos B tienen que competir entre sí por señales que promuevan su supervivencia en los centros germinales.
Aunque existen muchos patógenos diversos, muchos de los cuales están mutando constantemente, es sorprendente que la mayoría de las personas permanezcan libres de infecciones. Por lo tanto, el mantenimiento de la salud requiere que el cuerpo reconozca todos los patógenos (antígenos que presentan o producen) que probablemente existan. Esto se logra manteniendo un grupo inmensamente grande (alrededor de 10 9 ) de clones de células B, cada uno de los cuales reacciona contra un epítopo específico al reconocerlo y producir anticuerpos contra él. Sin embargo, en un momento dado, muy pocos clones permanecen realmente receptivos a su epítopo específico. Por lo tanto, aproximadamente 10 7 epítopos diferentes pueden ser reconocidos por todos los clones de células B combinados. [21] Además, a lo largo de la vida, un individuo generalmente requiere la generación de anticuerpos contra muy pocos antígenos en comparación con la cantidad que el cuerpo puede reconocer y contra los que puede responder. [21]
Si un antígeno puede ser reconocido por más de un componente de su estructura, es menos probable que el sistema inmunológico lo "pase por alto". [nota 10] La mutación de organismos patógenos puede provocar la modificación de la estructura del antígeno y, por lo tanto, de la del epítopo. Si el sistema inmunológico "recuerda" cómo son los otros epítopos, el antígeno y el organismo seguirán siendo reconocidos y sujetos a la respuesta inmunológica del cuerpo. Por lo tanto, la respuesta policlonal amplía la gama de patógenos que pueden reconocerse. [24]
Muchos virus sufren mutaciones frecuentes que dan lugar a cambios en la composición de aminoácidos de sus proteínas importantes. Los epítopos situados en la proteína también pueden sufrir alteraciones en el proceso. Un epítopo alterado de este tipo se une con menos fuerza a los anticuerpos específicos del epítopo inalterado que habrían estimulado el sistema inmunológico. Esto es desafortunado porque la hipermutación somática da lugar a clones capaces de producir anticuerpos solubles que se habrían unido al epítopo alterado con la suficiente avidez como para neutralizarlo. Pero estos clones consistirían en células ingenuas a las que los anticuerpos de unión débil producidos por el clon previamente estimulado no les permiten proliferar. Esta doctrina se conoce como el pecado antigénico original . [21] Este fenómeno entra en juego particularmente en las respuestas inmunitarias contra los virus de la gripe , el dengue y el VIH . [25] Sin embargo, esta limitación no está impuesta por el fenómeno de la respuesta policlonal, sino más bien, en su contra por una respuesta inmunitaria que está sesgada a favor de las células de memoria experimentadas en contra de las células ingenuas "novatas".
En la autoinmunidad, el sistema inmunitario reconoce erróneamente ciertas moléculas nativas del cuerpo como extrañas ( autoantígeno ) y monta una respuesta inmunitaria contra ellas. Dado que estas moléculas nativas, como partes normales del cuerpo, siempre existirán naturalmente en el cuerpo, los ataques contra ellas pueden hacerse más fuertes con el tiempo (similar a la respuesta inmunitaria secundaria). Además, muchos organismos exhiben mimetismo molecular , que implica mostrar aquellos antígenos en su superficie que son antigénicamente similares a las proteínas del huésped. Esto tiene dos posibles consecuencias: primero, o bien el organismo se salvará como autoantígeno; o segundo, que los anticuerpos producidos contra él también se unirán a las proteínas nativas imitadas. Los anticuerpos atacarán a los autoantígenos y los tejidos que los albergan activando varios mecanismos como la activación del complemento y la citotoxicidad mediada por células dependiente de anticuerpos . Por lo tanto, cuanto más amplia sea la gama de especificidades de los anticuerpos, mayor será la probabilidad de que uno u otro reaccione contra los autoantígenos (moléculas nativas del cuerpo). [26] [27]
Los anticuerpos monoclonales son moléculas de inmunoglobulina estructuralmente idénticas con idéntica especificidad de epítopo (todas ellas se unen al mismo epítopo con la misma afinidad) en comparación con sus contrapartes policlonales que tienen afinidades variables para el mismo epítopo. Por lo general, no se producen en una respuesta inmune natural, sino solo en estados patológicos como el mieloma múltiple o mediante técnicas de laboratorio especializadas. Debido a su especificidad, los anticuerpos monoclonales se utilizan en ciertas aplicaciones para cuantificar o detectar la presencia de sustancias (que actúan como antígeno para los anticuerpos monoclonales) y para dirigirse a células individuales (por ejemplo, células cancerosas). Los anticuerpos monoclonales se utilizan en varias modalidades de diagnóstico (ver: Western blot e inmunofluorescencia ) y terapias , particularmente del cáncer y enfermedades con componente autoinmune. Pero, dado que prácticamente todas las respuestas en la naturaleza son policlonales, hace que la producción de anticuerpos monoclonales inmensamente útiles sea menos sencilla . [8]
La primera evidencia de la presencia de una sustancia neutralizante en la sangre que podía contrarrestar las infecciones se produjo cuando Emil von Behring y Kitasato Shibasaburō desarrollaron en 1890 un suero eficaz contra la difteria. Para ello, transfirieron el suero producido a partir de animales inmunizados contra la difteria a animales que la padecían. De esta forma, la transferencia del suero podía curar a los animales infectados. Behring recibió el Premio Nobel por este trabajo en 1901. [28]
En ese momento, sin embargo, no se conocía la naturaleza química exacta de lo que en la sangre confería esta protección. En unas décadas más tarde, se demostró que el suero protector podía neutralizar y precipitar toxinas y agrupar bacterias. Todas estas funciones se atribuyeron a diferentes sustancias en el suero y se denominaron en consecuencia antitoxina , precipitina y aglutinina . [17] Elvin A. Kabat demostró en 1939 que las tres sustancias eran una sola entidad ( gammaglobulinas ) . El año anterior, Kabat había demostrado la heterogeneidad de los anticuerpos mediante estudios de ultracentrifugación de sueros de caballos. [29]
Hasta ese momento, la inmunidad celular y la inmunidad humoral se consideraban teorías rivales para explicar la respuesta inmunitaria eficaz, pero la primera se quedó atrás debido a la falta de técnicas avanzadas. [17] La inmunidad celular recibió un impulso en su reconocimiento y estudio cuando en 1942, Merrill Chase transfirió con éxito la inmunidad contra la tuberculosis entre cerdos mediante la transferencia de glóbulos blancos. [17] [30]
Más tarde, en 1948, Astrid Fagraeus demostró en su tesis doctoral que las células B plasmáticas están específicamente implicadas en la producción de anticuerpos. [31] El papel de los linfocitos en la mediación de las respuestas tanto mediadas por células como humorales fue demostrado por James Gowans en 1959. [30]
Para explicar la amplia gama de antígenos que el sistema inmunológico puede reconocer, Paul Ehrlich en 1900 había planteado la hipótesis de que los "receptores de cadena lateral" preexistentes se unen a un patógeno determinado, y que esta interacción induce a la célula que exhibe el receptor a multiplicarse y producir más copias del mismo receptor. Esta teoría, llamada teoría selectiva , no se demostró durante las siguientes cinco décadas, y había sido cuestionada por varias teorías instructivas que se basaban en la noción de que un anticuerpo asumiría su estructura efectiva al plegarse alrededor del antígeno. [17] Sin embargo, a fines de la década de 1950, los trabajos de tres científicos: Jerne , Talmage y Burnet (que modificaron en gran medida la teoría), dieron lugar a la teoría de la selección clonal , que demostró todos los elementos de la hipótesis de Ehrlich excepto que los receptores específicos que podían neutralizar el agente eran solubles y no estaban unidos a la membrana. [17] [30]
La teoría de la selección clonal resultó correcta cuando Sir Gustav Nossal demostró que cada célula B siempre produce sólo un anticuerpo. [32]
En 1974, Rolf Zinkernagel y Peter C. Doherty demostraron el papel del MHC en la presentación de antígenos . [30]
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ){{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )