La patogenómica es un campo que utiliza tecnología de detección de alto rendimiento y bioinformática para estudiar la resistencia de los microbios codificados, así como los factores de virulencia (VF), que permiten que un microorganismo infecte a un huésped y posiblemente cause una enfermedad. [1] [2] [3] [4] Esto incluye el estudio de genomas de patógenos que no pueden cultivarse fuera de un huésped. [5] En el pasado, a los investigadores y profesionales médicos les resultaba difícil estudiar y comprender los rasgos patógenos de los organismos infecciosos. [6] Con tecnología más nueva, los genomas de patógenos se pueden identificar y secuenciar en un tiempo mucho más corto y a un costo menor, [7] [8] mejorando así la capacidad de diagnosticar, tratar e incluso predecir y prevenir infecciones y enfermedades patógenas. [9] También ha permitido a los investigadores comprender mejor los eventos de evolución del genoma (pérdida, ganancia, duplicación, reordenamiento de genes) y cómo esos eventos impactan la resistencia de los patógenos y su capacidad para causar enfermedades. [8] Esta afluencia de información ha creado la necesidad de herramientas bioinformáticas y bases de datos para analizar y hacer accesibles a los investigadores grandes cantidades de datos, [10] [11] y ha planteado cuestiones éticas sobre la conveniencia de reconstruir especies previamente extintas y mortales. patógenos para comprender mejor la virulencia. [12]
Durante los primeros tiempos en que se estudiaba la genómica, a los científicos les resultaba difícil secuenciar la información genética. [13] El campo comenzó a explotar en 1977 cuando Fred Sanger , PhD, junto con sus colegas, secuenciaron el genoma basado en ADN de un bacteriófago , utilizando un método ahora conocido como Método Sanger . [14] [15] [16] El método Sanger para secuenciar ADN avanzó exponencialmente en la biología molecular y condujo directamente a la capacidad de secuenciar genomas de otros organismos, incluido el genoma humano completo. [14] [15]
El genoma de la influenza Haemophilus fue uno de los primeros genomas de organismos secuenciados en 1995 por J. Craig Venter y Hamilton Smith utilizando la secuenciación escopeta del genoma completo. [17] [15] Desde entonces, se han desarrollado secuenciaciones de alto rendimiento más nuevas y más eficientes, como la secuenciación genómica de próxima generación (NGS) y la secuenciación genómica unicelular. [15] Mientras que el método Sanger puede secuenciar un fragmento de ADN a la vez, la tecnología NGS puede secuenciar miles de secuencias a la vez. [18] Con la capacidad de secuenciar rápidamente el ADN, se desarrollaron nuevos conocimientos, como el descubrimiento de que, dado que los genomas procarióticos son más diversos de lo que se pensaba originalmente, es necesario secuenciar múltiples cepas en una especie en lugar de solo unas pocas. [19] E. coli fue un ejemplo de por qué esto es importante, con genes que codifican factores de virulencia en dos cepas de la especie que difieren en al menos un treinta por ciento. [19] Este conocimiento, junto con un estudio más exhaustivo de la ganancia, pérdida y cambio del genoma, está brindando a los investigadores información valiosa sobre cómo los patógenos interactúan en los entornos del huésped y cómo pueden infectarlos y causar enfermedades. [19] [13]
Con esta gran afluencia de nueva información, ha surgido una mayor demanda de bioinformática para que los científicos puedan analizar adecuadamente los nuevos datos. En respuesta, se han desarrollado software y otras herramientas para este propósito. [10] [20] Además, a partir de 2008, la cantidad de secuencias almacenadas se duplicaba cada 18 meses, lo que hacía urgente la necesidad de mejores formas de organizar los datos y ayudar a la investigación. [21] En respuesta, se han creado muchas bases de datos y otros recursos de acceso público, incluido el programa de detección de patógenos NCBI, el Centro de integración de recursos de Pathosystems (PATRIC), [22] Pathogenwatch, [23] la base de datos de factores de virulencia (VFDB) de patógenos. bacterias, [24] [3] [21] la base de datos Victors de factores de virulencia en patógenos humanos y animales. [25] Hasta 2022, los patógenos más secuenciados son Salmonella enterica y E. coli - Shigella. [10] Se han revisado exhaustivamente las tecnologías de secuenciación, las herramientas bioinformáticas, las bases de datos, las estadísticas relacionadas con los genomas de patógenos y las aplicaciones en medicina forense, epidemiología, práctica clínica y seguridad alimentaria. [10]
Los patógenos pueden ser procarióticos ( arqueas o bacterias ), eucariotas unicelulares o virus . Los genomas procarióticos normalmente han sido más fáciles de secuenciar debido al tamaño del genoma más pequeño en comparación con Eukarya. Debido a esto, existe un sesgo al informar el comportamiento de las bacterias patógenas . Independientemente de este sesgo en la presentación de informes, muchos de los eventos genómicos dinámicos son similares en todos los tipos de organismos patógenos. La evolución genómica se produce mediante la ganancia y la pérdida de genes y el reordenamiento del genoma, y estos "eventos" se observan en múltiples genomas de patógenos, y algunos patógenos bacterianos experimentan los tres. [13] Sin embargo , la patogenómica no se centra exclusivamente en comprender las interacciones patógeno-huésped . La comprensión del comportamiento individual o cooperativo de los patógenos proporciona conocimiento sobre el desarrollo o la herencia de los factores de virulencia de los patógenos. [13] A través de una comprensión más profunda de las pequeñas subunidades que causan la infección, puede ser posible desarrollar nuevas terapias que sean eficientes y rentables. [26]
Se necesitan genomas dinámicos con alta plasticidad para permitir que los patógenos, especialmente las bacterias, sobrevivan en entornos cambiantes. [19] Con la ayuda de métodos de secuenciación de alto rendimiento y tecnologías in silico , es posible detectar, comparar y catalogar muchos de estos eventos genómicos dinámicos. La diversidad genómica es importante al detectar y tratar un patógeno, ya que estos eventos pueden cambiar la función y estructura del patógeno. [27] [28] Existe la necesidad de analizar más de una única secuencia del genoma de una especie patógena para comprender los mecanismos patógenos. La genómica comparada es una metodología que permite a los científicos comparar los genomas de diferentes especies y cepas. [29] Hay varios ejemplos de estudios genómicos comparativos exitosos, entre ellos el análisis de Listeria [30] y Escherichia coli . [31] Algunos estudios han intentado abordar la diferencia entre microbios patógenos y no patógenos . Sin embargo, esta investigación resulta difícil, ya que una sola especie bacteriana puede tener muchas cepas y el contenido genómico de cada una de estas cepas varía. [31]
Las diferentes cepas de microbios y el contenido genómico son causados por diferentes fuerzas, incluidos tres eventos evolutivos específicos que tienen un impacto en la resistencia de los patógenos y su capacidad para causar enfermedades: ganancia de genes, pérdida de genes y reordenamiento del genoma. [13]
La pérdida de genes ocurre cuando se eliminan genes. La razón por la que esto ocurre aún no se comprende completamente, [32] aunque lo más probable es que implique la adaptación a un nuevo entorno o nicho ecológico. [33] [34] Algunos investigadores creen que la pérdida de genes en realidad puede aumentar la aptitud y la supervivencia entre los patógenos. [32] En un nuevo entorno, algunos genes pueden volverse innecesarios para la supervivencia, por lo que eventualmente se "permiten" mutaciones en esos genes hasta que se convierten en " pseudogenes " inactivos. [33] Estos pseudogenes se observan en organismos como Shigella flexneri , Salmonella enterica , [35] y Yersinia pestis . [33] Con el tiempo, los pseudogenes se eliminan y los organismos se vuelven completamente dependientes de su huésped como endosimbiontes o patógenos intracelulares obligados , como se observa en Buchnera , Myobacterium leprae y Chlamydia trachomatis . [33] Estos genes eliminados también se denominan genes antivirulencia (AVG), ya que se cree que pueden haber impedido que el organismo se volviera patógeno. [33] Para ser más virulento, infectar a un huésped y permanecer vivo, el patógeno tuvo que deshacerse de esos AVG. [33] El proceso inverso también puede ocurrir, como se observó durante el análisis de cepas de Listeria , que mostró que un tamaño reducido del genoma condujo a una cepa de Listeria no patógena a partir de una cepa patógena. [30] Se han desarrollado sistemas para detectar estos pseudogenes/AVG en una secuencia del genoma. [8]

Se cree que una de las fuerzas clave que impulsa la ganancia de genes es la transferencia horizontal (lateral) de genes (LGT). [36] Es de particular interés en estudios microbianos porque estos elementos genéticos móviles pueden introducir factores de virulencia en un nuevo genoma. [37] Un estudio comparativo realizado por Gill et al. en 2005 postuló que LGT puede haber sido la causa de las variaciones de patógenos entre Staphylococcus epidermidis y Staphylococcus aureus . [38] Sin embargo, todavía existe escepticismo sobre la frecuencia de LGT, su identificación y su impacto. [39] Se han utilizado metodologías nuevas y mejoradas, especialmente en el estudio de la filogenética , para validar la presencia y el efecto de LGT. [40] Los eventos de ganancia y duplicación de genes se equilibran con la pérdida de genes, de modo que a pesar de su naturaleza dinámica, el genoma de una especie bacteriana permanece aproximadamente del mismo tamaño. [41]
Las secuencias de inserción genética móviles pueden desempeñar un papel en las actividades de reordenamiento del genoma. [42] Se ha descubierto que los patógenos que no viven en un ambiente aislado contienen una gran cantidad de elementos de secuencia de inserción y varios segmentos repetitivos de ADN. [19] Se cree que la combinación de estos dos elementos genéticos ayuda a mediar la recombinación homóloga . Hay patógenos, como Burkholderia mallei , [43] y Burkholderia pseudomallei [44] que han demostrado exhibir reordenamientos en todo el genoma debido a secuencias de inserción y segmentos de ADN repetitivos. [19] En este momento, ningún estudio demuestra que eventos de reordenamiento de todo el genoma den lugar directamente a un comportamiento patógeno en un microbio. Esto no significa que no sea posible. Sin embargo, los reordenamientos de todo el genoma contribuyen a la plasticidad del genoma bacteriano, lo que puede preparar las condiciones para que otros factores introduzcan o pierdan factores de virulencia. [19]
Los polimorfismos de un solo nucleótido , o SNP, permiten una amplia gama de variaciones genéticas entre humanos y patógenos. Permiten a los investigadores estimar una variedad de factores: los efectos de las toxinas ambientales, cómo los diferentes métodos de tratamiento afectan al cuerpo y qué causa la predisposición de una persona a las enfermedades. [45] Los SNP desempeñan un papel clave en la comprensión de cómo y por qué ocurren las mutaciones. Los SNP también permiten a los científicos mapear genomas y analizar información genética. [45]

Descripción general del pangenoma La definición más reciente de especie bacteriana proviene de la era pregenómica. En 1987, se propuso que las cepas bacterianas que mostraban >70% de reasociación ADN·ADN y compartían rasgos fenotípicos característicos debían considerarse cepas de la misma especie. [46] La diversidad dentro de los genomas de los patógenos hace que sea difícil identificar el número total de genes que están asociados dentro de todas las cepas de una especie de patógeno. [46] Se ha pensado que el número total de genes asociados con una sola especie patógena puede ser ilimitado, [46] aunque algunos grupos están intentando derivar un valor más empírico. [47] Por esta razón, fue necesario introducir el concepto de pangenomas y genomas centrales. [48] La literatura sobre pangenomas y genoma central también tiende a tener un sesgo hacia la presentación de informes sobre organismos patógenos procarióticos. Es posible que sea necesario tener precaución al ampliar la definición de pangenoma o genoma central a otros organismos patógenos porque no existe evidencia formal de las propiedades de estos pangenomas. [ cita necesaria ]
Un genoma central es el conjunto de genes que se encuentran en todas las cepas de una especie patógena. [46] Un pangenoma es el acervo genético completo de esa especie patógena e incluye genes que no son compartidos por todas las cepas. [46] Los pangenomas pueden ser abiertos o cerrados dependiendo de si el análisis comparativo de múltiples cepas no revela genes nuevos (cerrados) o muchos genes nuevos (abiertos) en comparación con el genoma central de esa especie patógena. [13] En el pangenoma abierto, los genes pueden caracterizarse además como prescindibles o específicos de cepa. Los genes prescindibles son aquellos que se encuentran en más de una cepa, pero no en todas las cepas, de una especie patógena. [48] Los genes específicos de cepa son aquellos que se encuentran solo en una cepa de una especie patógena. [48] Las diferencias en los pangenomas son reflejos del estilo de vida del organismo. Por ejemplo, Streptococcus agalactiae , que existe en diversos nichos biológicos, tiene un pangenoma más amplio en comparación con el Bacillus anthracis, más aislado ambientalmente . [19] También se están utilizando enfoques de genómica comparada para comprender más sobre el pangenoma. [49] Descubrimientos recientes muestran que el número de nuevas especies continúa creciendo con un estimado de 10 31 bacteriófagos en el planeta y esos bacteriófagos infectan a otros 10 24 por segundo, el flujo continuo de material genético que se intercambia es difícil de imaginar. [46]
Múltiples elementos genéticos de patógenos que afectan al ser humano contribuyen a la transferencia de factores de virulencia: plásmidos , islas de patogenicidad , profagos , bacteriófagos, transposones y elementos integrativos y conjugativos. [13] [50] Las islas de patogenicidad y su detección son el foco de varios esfuerzos bioinformáticos involucrados en patogenómica. [51] [52] Es una creencia común que las "cepas bacterianas ambientales" carecen de la capacidad de dañar o causar daño a los humanos. Sin embargo, estudios recientes muestran que las bacterias de los ambientes acuáticos han adquirido cepas patógenas a través de la evolución. Esto permite que las bacterias tengan una gama más amplia de rasgos genéticos y pueden causar una amenaza potencial para los humanos, que tienen más resistencia a los antibióticos. [50]
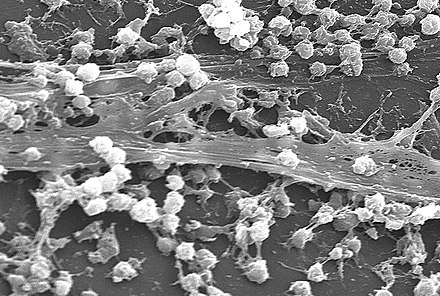
Las interacciones microbio-huésped tienden a eclipsar la consideración de las interacciones microbio-microbio. Sin embargo, las interacciones microbio-microbio pueden provocar estados crónicos de enfermedad que son difíciles de comprender y tratar. [9]
Las biopelículas son un ejemplo de interacciones microbio-microbio y se cree que están asociadas con hasta el 80% de las infecciones humanas. [53] Recientemente se ha demostrado que existen genes específicos y proteínas de la superficie celular implicados en la formación de biopelículas. [54] Estos genes y también las proteínas de superficie pueden caracterizarse mediante métodos in silico para formar un perfil de expresión de bacterias que interactúan con biopelículas. [9] Este perfil de expresión se puede utilizar en análisis posteriores de otros microbios para predecir el comportamiento de los microbios de biopelículas o para comprender cómo desmantelar la formación de biopelículas. [9]
Los patógenos tienen la capacidad de adaptarse y manipular las células huésped, aprovechando al máximo los procesos y mecanismos celulares de una célula huésped. [9]
Los huéspedes pueden influir en un microbio para que se adapte a su nuevo entorno o aprenda a evadirlo. Una comprensión de estos comportamientos proporcionará información beneficiosa para posibles terapias. El esquema más detallado de las iniciativas de interacción huésped-microbio se describe en la Agenda Europea de Investigación sobre Patogenómica. [9] Su informe destaca las siguientes características:

Se ha anunciado que la comunidad diversa dentro del intestino es vital para la salud humana. Hay varios proyectos en marcha para comprender mejor los ecosistemas del intestino. [58] La secuencia de la cepa SE11 de Escherichia coli comensal , por ejemplo, ya se ha determinado a partir de la materia fecal de un ser humano sano y promete ser el primero de muchos estudios. [59] A través del análisis genómico y también del posterior análisis de proteínas, se investigará una mejor comprensión de las propiedades beneficiosas de la flora comensal con la esperanza de comprender cómo construir una mejor terapia. [60]
La perspectiva "eco-evo" sobre las interacciones patógeno-huésped enfatiza las influencias de la ecología y el medio ambiente en la evolución de los patógenos. [13] Los factores genómicos dinámicos, como la pérdida de genes, la ganancia de genes y el reordenamiento del genoma, están fuertemente influenciados por cambios en el nicho ecológico donde reside una cepa microbiana particular. Los microbios pueden pasar de ser patógenos a no patógenos debido a los entornos cambiantes. [30] Esto se demostró durante los estudios de la plaga, Yersinia pestis , que aparentemente evolucionó de un patógeno gastrointestinal leve a un microbio altamente patógeno a través de eventos genómicos dinámicos. [61] Para que se produzca la colonización, debe haber cambios en la composición bioquímica para ayudar a la supervivencia en una variedad de entornos. Lo más probable es que esto se deba a un mecanismo que permite a la célula detectar cambios en el entorno, influyendo así en el cambio en la expresión genética. [62] Comprender cómo se producen estos cambios de cepa de ser poco patógenos o no patógenos a altamente patógenos y viceversa puede ayudar a desarrollar nuevas terapias para las infecciones microbianas. [13]
La salud humana ha mejorado enormemente y la tasa de mortalidad ha disminuido sustancialmente desde la Segunda Guerra Mundial debido a la mejora de la higiene debido a los cambios en las regulaciones de salud pública, así como a la mayor disponibilidad de vacunas y antibióticos. [63] La patogenómica permitirá a los científicos ampliar lo que saben sobre los microbios patógenos y no patógenos, permitiendo así vacunas nuevas y mejoradas. [63] La patogenómica también tiene implicaciones más amplias, incluida la prevención del bioterrorismo. [63]
La vacunación inversa es relativamente nueva. Si bien aún se realizan investigaciones, se han producido avances con patógenos como el estreptococo y la meningitis . [64] Los métodos de producción de vacunas, como los bioquímicos y serológicos, son laboriosos y poco fiables. Requieren que los patógenos estén in vitro para ser eficaces. [65] Los nuevos avances en el desarrollo genómico ayudan a predecir casi todas las variaciones de patógenos, lo que supone avances para las vacunas. [65] Se están desarrollando vacunas a base de proteínas para combatir patógenos resistentes como Staphylococcus y Chlamydia . [64]
En 2005 se completó la secuencia de la gripe española de 1918. Acompañado de un análisis filogenético , fue posible proporcionar una descripción detallada de la evolución y el comportamiento del virus, en particular de su adaptación a los humanos. [66] Tras la secuenciación de la gripe española, el patógeno también fue reconstruido. Cuando se insertó en ratones, el patógeno resultó ser increíblemente mortal. [67] [12] Los ataques con ántrax de 2001 arrojan luz sobre la posibilidad de que el bioterrorismo sea una amenaza más real que imaginada. El bioterrorismo se anticipó en la guerra de Irak, cuando los soldados fueron vacunados contra un ataque de viruela . [68] Utilizando tecnologías y conocimientos adquiridos a partir de la reconstrucción de la gripe española, puede ser posible prevenir futuros brotes mortales de enfermedades sembradas. Sin embargo, existe una fuerte preocupación ética sobre si la resurrección de virus antiguos es necesaria y si hace más daño que bien. [12] [69] La mejor vía para contrarrestar tales amenazas es coordinar con organizaciones que proporcionan inmunizaciones. Una mayor concienciación y participación disminuiría en gran medida la eficacia de una posible epidemia. Un complemento a esta medida sería monitorear los reservorios naturales de agua como base para prevenir un ataque o brote. En general, la comunicación entre laboratorios y grandes organizaciones, como la Red Global de Alerta y Respuesta a Brotes (GOARN), puede conducir a la detección temprana y prevenir brotes. [63]