El ADN ribosómico (abreviado ADNr ) consta de un grupo de ARN ribosómico que codifica genes y elementos reguladores relacionados, y está muy extendido en una configuración similar en todos los ámbitos de la vida. El ADN ribosómico codifica el ARN ribosómico no codificante , elementos estructurales integrales en el ensamblaje de los ribosomas , su importancia lo convierte en la sección de ARN más abundante que se encuentra en las células de eucariotas . [1] Además, estos segmentos incluyen secciones reguladoras , como un promotor específico de la ARN polimerasa I , así como segmentos espaciadores tanto transcritos como no transcritos.
Debido a su gran importancia en el ensamblaje de ribosomas para la biosíntesis de proteínas , los genes de ADNr generalmente están muy conservados en la evolución molecular . El número de copias puede variar considerablemente según la especie. [1] El ADN ribosómico se utiliza ampliamente para estudios filogenéticos . [2] [3]
El ADN ribosómico incluye todos los genes que codifican las moléculas de ARN ribosómico estructural no codificantes . En todos los ámbitos de la vida, estos son principalmente el ARNr 16S y 18S de la subunidad pequeña y el ARNr 23S y 28S de la subunidad grande ; el conjunto de estos últimos también incluye el ARNr 5S, así como el ARNr 5.8S adicional en eucariotas.
Los genes de ADNr suelen estar presentes con múltiples copias en el genoma, donde están organizados en grupos unidos en la mayoría de las especies, separados por un espaciador transcrito interno (ITS) y precedidos por el espaciador transcrito externo (ETS) . El ARNr 5S también está vinculado a esta región de ADNr en los procariotas, mientras que en la mayoría de los eucariotas se encuentra en regiones repetidas separadas. [4] Se transcriben juntos en un ARN precursor que luego se procesa en cantidades iguales de cada ARNr.
En bacterias , arqueas y cloroplastos , el ARNr está compuesto de diferentes unidades (más pequeñas), el ARN ribosómico grande (23S) , el ARN ribosómico 16S y el ARNr 5S.
Una cantidad notable de bacterias y arqueas divergen de la estructura canónica del operón que contiene los genes del ADNr y portan los genes "desvinculados" en diferentes lugares de su genoma. [5]
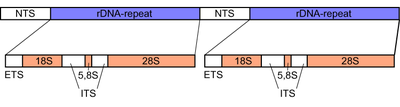

El grupo de genes de ADNr de eucariotas consta de los genes del ARNr 18S , 5.8S y 28S , separados por los dos espaciadores ITS-1 e ITS-2 . El genoma activo de los eucariotas contiene varios cientos de copias de la unidad transcripcional de ADNr en forma de repeticiones en tándem ; están organizadas en regiones organizadoras del nucléolo (NOR) , [4] que a su vez pueden estar presentes en múltiples loci del genoma. [6]
De manera similar a la estructura de los procariotas, el ARNr 5S se adjunta al grupo de ADNr en los Saccharomycetes (Hemiascomycetes) [6] , como Saccharomyces cerevisiae . [4] Sin embargo, la mayoría de los eucariotas portan el gen del ARNr 5S en repeticiones genéticas separadas en diferentes loci del genoma. [6] [4]
El ADNr 5S también está presente en repeticiones en tándem independientes como en Drosophila . [6] Como las regiones de ADN repetitivas a menudo sufren eventos de recombinación, las repeticiones de ADNr tienen muchos mecanismos reguladores que evitan que el ADN sufra mutaciones, [ se necesita un ejemplo ] , manteniendo así el ADNr conservado. [1]
En el núcleo, las regiones organizadoras del nucléolo dan lugar al nucléolo , donde las regiones de ADNr del cromosoma forman bucles cromosómicos expandidos, accesibles para la transcripción de ARNr . En el ADNr, las repeticiones en tándem se encuentran principalmente en el nucléolo; pero el ADNr heterocromático se encuentra fuera del nucléolo. Sin embargo, el ADNr transcripcionalmente activo reside dentro del propio nucléolo. [1]
El genoma humano contiene un total de 560 copias [4] de la unidad transcripcional de ADNr, repartidas en cinco cromosomas con regiones organizadoras del nucléolo . Los grupos repetidos están ubicados en los cromosomas acrocéntricos 13 ( RNR1 ), 14 ( RNR2 ), 15 ( RNR3 ), 21 ( RNR4 ) y 22 ( RNR5 ). [7]
En los ciliados , la presencia de un micronúcleo generativo junto al macronúcleo vegetativo permite la reducción de genes de ADNr en la línea germinal. El número exacto de copias en el genoma central del micronúcleo varía desde varias copias en Paramecium [8] hasta una sola copia en Tetrahymena thermophila [4] y otras especies de Tetrahymena . Durante la formación de macronúcleos , las regiones que contienen los grupos de genes de ADNr se amplifican, lo que aumenta drásticamente la cantidad de plantillas disponibles para la transcripción hasta varios miles de copias. En algunos géneros ciliados, como Tetrahymena o el género Hypotrich Oxytricha , [8] la fragmentación extensa del ADN aplificado conduce a la formación de microcromosomas, centrados en la unidad transcripcional del ADNr. [8] Se informan procesos similares en Glaucoma chattoni y, en menor medida, en Paramecium . [8]
En la gran matriz de ADNr, los polimorfismos entre las unidades repetidas de ADNr son muy bajos, lo que indica que las matrices en tándem de ADNr están evolucionando a través de una evolución concertada . [6] Sin embargo, el mecanismo de la evolución concertada es imperfecto, de modo que los polimorfismos entre repeticiones dentro de un individuo pueden ocurrir en niveles significativos y pueden confundir los análisis filogenéticos de organismos estrechamente relacionados. [9] [10]
Se compararon entre sí secuencias repetidas en tándem 5S en varias Drosophila ; El resultado reveló que las inserciones y eliminaciones se producían con frecuencia entre especies y, a menudo, estaban flanqueadas por secuencias conservadas. [11] Podrían ocurrir por deslizamiento de la cadena recién sintetizada durante la replicación del ADN o por conversión de genes. [11]
Los tractos de transcripción del ADNr tienen una baja tasa de polimorfismo entre especies, lo que permite la comparación interespecífica para dilucidar la relación filogenética utilizando solo unos pocos especímenes. Las regiones codificantes del ADNr están altamente conservadas entre las especies, pero las regiones ITS son variables debido a inserciones, eliminaciones y mutaciones puntuales. Entre especies remotas como humanos y ranas, la comparación de secuencias en sus tractos no es apropiada. [12] Las secuencias conservadas en las regiones codificantes del ADNr permiten comparaciones de especies remotas, incluso entre levaduras y humanos. El ARNr 5.8S humano tiene un 75% de identidad con el ARNr 5.8S de levadura. [13] En los casos de especies hermanas, la comparación del segmento de ADNr, incluidos sus tractos entre especies, y el análisis filogenético se realizan de manera satisfactoria. [14] [15] Las diferentes regiones codificantes de las repeticiones de ADNr generalmente muestran distintas tasas de evolución. Como resultado, este ADN puede proporcionar información filogenética de especies que pertenecen a amplios niveles sistemáticos. [2]
Un fragmento de ADNr de levadura que contiene el gen 5S, ADN espaciador no transcrito y parte del gen 35S tiene una actividad estimulante de la recombinación mitótica localizada que actúa en cis. [16] Este fragmento de ADN contiene un punto de recombinación mitótica , denominado HOT1. "HOT1 expresa actividad estimulante de la recombinación cuando se inserta en ubicaciones novedosas en el genoma de la levadura ". HOT1 incluye un promotor de transcripción de ARN polimerasa I (PolI) que cataliza la transcripción del gen de ARNr ribosómico 35S . En un mutante defectuoso de PolI, se suprime la actividad estimulante de la recombinación del punto de acceso HOT1. El nivel de transcripción de PolI en HOT1 parece determinar el nivel de recombinación . [17]
Las enfermedades pueden estar asociadas con mutaciones del ADN en las que el ADN puede expandirse, como la enfermedad de Huntington , o perderse debido a mutaciones por deleción. Lo mismo ocurre con las mutaciones que ocurren en las repeticiones del ADNr; Se ha descubierto que si los genes asociados con la síntesis de ribosomas se alteran o mutan, puede provocar diversas enfermedades asociadas con el esqueleto o la médula ósea. Además, cualquier daño o alteración de las enzimas que protegen las repeticiones en tándem del ADNr puede provocar una menor síntesis de ribosomas, lo que también conduce a otros defectos en la célula. Las enfermedades neurológicas también pueden surgir por mutaciones en las repeticiones en tándem del ADNr, como el síndrome de Bloom , que se produce cuando el número de repeticiones en tándem aumenta cerca de cien veces; comparado con el del número normal de repeticiones en tándem. También pueden nacer varios tipos de cáncer a partir de mutaciones de las repeticiones en tándem del ADN ribosómico. Las líneas celulares pueden volverse malignas debido a una reordenación de las repeticiones en tándem o a una expansión de las repeticiones en el ADNr. [18]