La química bioinorgánica es un campo que examina el papel de los metales en la biología . La química bioinorgánica incluye el estudio tanto de fenómenos naturales como el comportamiento de las metaloproteínas como de los metales introducidos artificialmente, incluidos los que no son esenciales , en medicina y toxicología . Muchos procesos biológicos, como la respiración, dependen de moléculas que pertenecen al ámbito de la química inorgánica . La disciplina también incluye el estudio de modelos inorgánicos o imitadores que imitan el comportamiento de las metaloproteínas. [1]
Como mezcla de bioquímica y química inorgánica , la química bioinorgánica es importante para dilucidar las implicaciones de las proteínas de transferencia de electrones , la unión y activación de sustratos, la química de transferencia de átomos y grupos, así como las propiedades de los metales en la química biológica. El desarrollo exitoso de un trabajo verdaderamente interdisciplinario es necesario para avanzar en la química bioinorgánica. [2]
Aproximadamente el 99% de la masa de los mamíferos son los elementos carbono , nitrógeno , calcio , sodio , cloro , potasio , hidrógeno , fósforo , oxígeno y azufre . [3] Los compuestos orgánicos ( proteínas , lípidos y carbohidratos ) contienen la mayor parte del carbono y el nitrógeno y la mayor parte del oxígeno y el hidrógeno están presentes en forma de agua. [3] El conjunto completo de biomoléculas que contienen metales en una célula se llama metaloma .
Paul Ehrlich utilizó organoarsénico (“arsenicales”) para el tratamiento de la sífilis , demostrando la relevancia de los metales, o al menos los metaloides, para la medicina, que floreció con el descubrimiento de Rosenberg de la actividad anticancerígena del cisplatino (cis-PtCl 2 (NH 3 ) 2 ). La primera proteína jamás cristalizada (ver James B. Sumner ) fue la ureasa , y más tarde se demostró que contenía níquel en su sitio activo . Dorothy Crowfoot Hodgkin demostró cristalográficamente que la vitamina B 12 , la cura para la anemia perniciosa , consiste en un cobalto en un macrociclo de corrina . La estructura Watson-Crick del ADN demostró el papel estructural clave que desempeñan los polímeros que contienen fosfato.
En la química bioinorgánica se pueden identificar varios sistemas distintos. Las áreas principales incluyen:
Se emplea una colección diversa de transportadores (p. ej., la bomba de iones NaKATPasa ), vacuolas , proteínas de almacenamiento (p. ej., ferritina ) y moléculas pequeñas (p. ej., sideróforos ) para controlar la concentración y la biodisponibilidad de iones metálicos en los organismos vivos. Fundamentalmente, muchos metales esenciales no son fácilmente accesibles para las proteínas posteriores debido a su baja solubilidad en soluciones acuosas o su escasez en el entorno celular. Los organismos han desarrollado una serie de estrategias para recolectar y transportar dichos elementos limitando al mismo tiempo su citotoxicidad .
Muchas reacciones en las ciencias de la vida involucran agua y los iones metálicos a menudo se encuentran en los centros catalíticos (sitios activos) de estas enzimas, es decir, se trata de metaloproteínas . A menudo, el agua que reacciona es un ligando (ver complejo acuoso metálico ). Ejemplos de enzimas hidrolasas son la anhidrasa carbónica , las metalofosfatasas y las metaloproteinasas . Los químicos bioinorgánicos buscan comprender y replicar la función de estas metaloproteínas.
También son comunes las proteínas de transferencia de electrones que contienen metales. Se pueden organizar en tres clases principales: proteínas de hierro y azufre (como rubredoxinas , ferredoxinas y proteínas de Rieske ), proteínas azules de cobre y citocromos . Estas proteínas transportadoras de electrones son complementarias de los transportadores de electrones no metálicos nicotinamida adenina dinucleótido (NAD) y flavina adenina dinucleótido (FAD). El ciclo del nitrógeno hace un uso extensivo de metales para las interconversiones redox.

Varios iones metálicos son tóxicos para los humanos y otros animales. Se ha revisado la química bioinorgánica del plomo en el contexto de su toxicidad. [4]
La vida aeróbica hace un uso extensivo de metales como el hierro, el cobre y el manganeso. El hemo es utilizado por los glóbulos rojos en forma de hemoglobina para el transporte de oxígeno y es quizás el sistema metálico más reconocido en biología. Otros sistemas de transporte de oxígeno incluyen mioglobina , hemocianina y hemeritrina . Las oxidasas y oxigenasas son sistemas metálicos que se encuentran en toda la naturaleza y que aprovechan el oxígeno para llevar a cabo reacciones importantes como la generación de energía en la citocromo c oxidasa o la oxidación de pequeñas moléculas en las citocromo P450 oxidasas o la metano monooxigenasa . Algunas metaloproteínas están diseñadas para proteger un sistema biológico de los efectos potencialmente dañinos del oxígeno y otras moléculas reactivas que contienen oxígeno, como el peróxido de hidrógeno . Estos sistemas incluyen peroxidasas , catalasas y superóxido dismutasas . Una metaloproteína complementaria a las que reaccionan con el oxígeno es el complejo de evolución de oxígeno presente en las plantas. Este sistema es parte de la compleja maquinaria proteica que produce oxígeno cuando las plantas realizan la fotosíntesis .

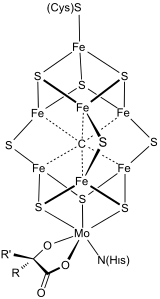
Los sistemas bioorganometálicos presentan enlaces metal-carbono como elementos estructurales o intermedios. Las enzimas y proteínas bioorganometálicas incluyen las hidrogenasas , FeMoco en la nitrogenasa y metilcobalamina . Estos compuestos organometálicos de origen natural . Esta área está más centrada en la utilización de metales por parte de organismos unicelulares. Los compuestos bioorganometálicos son importantes en la química ambiental . [5]
Varias drogas contienen metales. Este tema se basa en el estudio del diseño y mecanismo de acción de productos farmacéuticos que contienen metales y compuestos que interactúan con iones metálicos endógenos en sitios activos enzimáticos. El fármaco anticancerígeno más utilizado es el cisplatino . El agente de contraste para resonancia magnética comúnmente contiene gadolinio . El carbonato de litio se ha utilizado para tratar la fase maníaca del trastorno bipolar. Se han comercializado fármacos antiartríticos de oro, por ejemplo, auranofina . Las moléculas liberadoras de monóxido de carbono son complejos metálicos que se han desarrollado para suprimir la inflamación liberando pequeñas cantidades de monóxido de carbono. Se ha examinado la importancia cardiovascular y neuronal del óxido nítrico , incluida la enzima óxido nítrico sintasa . (Ver también: asimilación de nitrógeno .) Además, se han probado complejos de transición metálicos basados en triazolopirimidinas contra varias cepas de parásitos. [6]
La química ambiental tradicionalmente enfatiza la interacción de los metales pesados con los organismos. El metilmercurio ha causado un gran desastre llamado enfermedad de Minamata . El envenenamiento por arsénico es un problema generalizado debido en gran parte a la contaminación por arsénico de las aguas subterráneas , que afecta a muchos millones de personas en los países en desarrollo. El metabolismo de los compuestos que contienen mercurio y arsénico implica enzimas basadas en cobalamina .
La biomineralización es el proceso mediante el cual los organismos vivos producen minerales , a menudo para endurecer o endurecer los tejidos existentes. Estos tejidos se denominan tejidos mineralizados . [7] [8] [9] Los ejemplos incluyen silicatos en algas y diatomeas , carbonatos en invertebrados y fosfatos y carbonatos de calcio en vertebrados . Otros ejemplos incluyen depósitos de cobre , hierro y oro que involucran bacterias. Los minerales formados biológicamente a menudo tienen usos especiales, como sensores magnéticos en bacterias magnetotácticas (Fe 3 O 4 ), dispositivos sensores de gravedad (CaCO 3 , CaSO 4 , BaSO 4 ) y almacenamiento y movilización de hierro (Fe 2 O 3 •H 2 O en la proteína ferritina ). Debido a que el hierro extracelular [10] participa fuertemente en la inducción de la calcificación, [11] [12] su control es esencial en el desarrollo de las conchas; La proteína ferritina juega un papel importante en el control de la distribución del hierro. [13]
Los abundantes elementos inorgánicos actúan como electrolitos iónicos . Los iones más importantes son sodio , potasio , calcio , magnesio , cloruro , fosfato y bicarbonato . El mantenimiento de gradientes precisos a través de las membranas celulares mantiene la presión osmótica y el pH . [15] Los iones también son fundamentales para los nervios y los músculos , ya que los potenciales de acción en estos tejidos se producen mediante el intercambio de electrolitos entre el líquido extracelular y el citosol . [16] Los electrolitos entran y salen de las células a través de proteínas en la membrana celular llamadas canales iónicos . Por ejemplo, la contracción muscular depende del movimiento de calcio, sodio y potasio a través de canales iónicos en la membrana celular y los túbulos T. [17]
Los metales de transición suelen estar presentes como oligoelementos en los organismos, siendo el zinc y el hierro los más abundantes. [18] [19] [20] Estos metales se utilizan como cofactores de proteínas y moléculas de señalización. Muchos son esenciales para la actividad de enzimas como la catalasa y proteínas transportadoras de oxígeno como la hemoglobina . [21] Estos cofactores están estrechamente unidos a una proteína específica; Aunque los cofactores enzimáticos pueden modificarse durante la catálisis, los cofactores siempre regresan a su estado original después de que ha tenido lugar la catálisis. Los micronutrientes metálicos son absorbidos por los organismos mediante transportadores específicos y unidos a proteínas de almacenamiento como la ferritina o la metalotioneína cuando no se utilizan. [22] [23] El cobalto es esencial para el funcionamiento de la vitamina B12 . [24]
Muchos otros elementos además de los metales son bioactivos. El azufre y el fósforo son necesarios para toda vida. El fósforo existe casi exclusivamente como fosfato y sus diversos ésteres . El azufre existe en una variedad de estados de oxidación, que van desde sulfato (SO 4 2- ) hasta sulfuro (S 2- ). El selenio es un oligoelemento implicado en las proteínas que son antioxidantes. El cadmio es importante debido a su toxicidad. [25]