La espectroscopia de correlación de fluorescencia ( FCS ) es un análisis estadístico, mediante correlación temporal, de fluctuaciones estacionarias de la intensidad de fluorescencia . Su fundamento teórico surgió de la hipótesis de regresión de L. Onsager . El análisis proporciona parámetros cinéticos de los procesos físicos subyacentes a las fluctuaciones. Una de las aplicaciones interesantes de esto es el análisis de las fluctuaciones de concentración de partículas (moléculas) fluorescentes en solución. En esta aplicación, se observa la fluorescencia emitida desde un espacio muy pequeño en una solución que contiene una pequeña cantidad de partículas (moléculas) fluorescentes. La intensidad de la fluorescencia fluctúa debido al movimiento browniano de las partículas. En otras palabras, el número de partículas en el subespacio definido por el sistema óptico cambia aleatoriamente alrededor del número promedio. El análisis proporciona el número medio de partículas fluorescentes y el tiempo medio de difusión cuando la partícula atraviesa el espacio. Finalmente, se determinan tanto la concentración como el tamaño de la partícula (molécula). Ambos parámetros son importantes en la investigación bioquímica, la biofísica y la química.
FCS es una herramienta analítica muy sensible porque observa una pequeña cantidad de moléculas (concentraciones nanomolares a picomolares) en un volumen pequeño (~1 μm 3 ). [1] A diferencia de otros métodos (como el análisis HPLC ), FCS no tiene un proceso de separación física; en cambio, logra su resolución espacial a través de su óptica. Además, FCS permite la observación de moléculas marcadas con fluorescencia en la vía bioquímica en células vivas intactas. [2] Esto abre una nueva área, "bioquímica in situ o in vivo": rastrear la ruta bioquímica en células y órganos intactos. [3]
Comúnmente, FCS se emplea en el contexto de la microscopía óptica , en particular la microscopía confocal o la microscopía de excitación de dos fotones . En estas técnicas, la luz se enfoca en una muestra y las fluctuaciones medidas de la intensidad de la fluorescencia (debidas a difusión , reacciones físicas o químicas, agregación, etc.) se analizan utilizando la autocorrelación temporal. Debido a que la propiedad medida está esencialmente relacionada con la magnitud y/o la cantidad de fluctuaciones, existe un régimen de medición óptimo en el nivel cuando las especies individuales entran o salen del volumen de observación (o se encienden y apagan en el volumen). Cuando se miden demasiadas entidades al mismo tiempo, las fluctuaciones generales son pequeñas en comparación con la señal total y pueden no ser resolubles; en la otra dirección, si los eventos de fluctuación individuales son demasiado dispersos en el tiempo, una medición puede tomar demasiado tiempo. largo. FCS es en cierto modo la contraparte fluorescente de la dispersión dinámica de la luz , que utiliza dispersión de luz coherente, en lugar de fluorescencia (incoherente).
Cuando se conoce un modelo apropiado, FCS se puede utilizar para obtener información cuantitativa como
Debido a que los marcadores fluorescentes vienen en una variedad de colores y pueden unirse específicamente a una molécula particular (por ejemplo, proteínas, polímeros, complejos metálicos, etc.), es posible estudiar el comportamiento de moléculas individuales (en rápida sucesión en soluciones compuestas). . Con el desarrollo de detectores sensibles como los fotodiodos de avalancha, la detección de la señal de fluorescencia procedente de moléculas individuales en muestras muy diluidas se ha vuelto práctica. Con esto surgió la posibilidad de realizar experimentos FCS en una amplia variedad de especímenes, desde la ciencia de los materiales hasta la biología. La llegada de células diseñadas con proteínas genéticamente marcadas (como la proteína verde fluorescente ) ha convertido al FCS en una herramienta común para estudiar la dinámica molecular en células vivas. [4]
Las técnicas de correlación de señales fueron aplicadas experimentalmente por primera vez a la fluorescencia en 1972 por Magde, Elson y Webb, [5] a quienes, por lo tanto, se les atribuye comúnmente el mérito de ser los inventores del FCS. La técnica se desarrolló aún más en un grupo de artículos de estos y otros autores poco después, estableciendo los fundamentos teóricos y los tipos de aplicaciones. [6] [7] [8] Alrededor de 1990, con la capacidad de detectar un número suficientemente pequeño de partículas de fluorescencia, surgieron dos problemas: una distribución no gaussiana de la intensidad de la fluorescencia y el volumen de medición confocal tridimensional de una microscopía láser. sistema. [9] El primero condujo a un análisis de distribuciones y momentos de las señales fluorescentes para extraer información molecular, [10] [11] que eventualmente se convirtió en una colección de métodos conocidos como Análisis de Brillo. Véase Thompson (1991) [12] para una revisión de ese período.
A partir de 1993, [13] se introdujeron una serie de mejoras en las técnicas de medición (en particular el uso de microscopía confocal y luego microscopía de dos fotones) para definir mejor el volumen de medición y rechazar el fondo; mejoraron enormemente la relación señal-ruido y permitieron una sola medición. Sensibilidad molecular. [14] [15] Desde entonces, ha habido un interés renovado en FCS y, hasta agosto de 2007, se han encontrado más de 3.000 artículos que utilizan FCS en Web of Science. Véase Krichevsky y Bonnet [16] para una revisión. Además, ha habido una gran actividad para extender la FCS de varias maneras, por ejemplo, al escaneo láser y a la microscopía confocal de disco giratorio (a partir de una medición estacionaria de un solo punto), al utilizar la correlación cruzada (FCCS) entre dos canales fluorescentes. de autocorrelación y en el uso de transferencia de energía por resonancia de Förster (FRET) en lugar de fluorescencia.

La configuración típica de FCS consiste en una línea láser (longitudes de onda que generalmente oscilan entre 405 y 633 nm ( cw ) y entre 690 y 1100 nm (pulsada)), que se refleja en el objetivo de un microscopio mediante un espejo dicroico. El rayo láser se enfoca en la muestra, que contiene partículas (moléculas) fluorescentes en una dilución tan alta que solo unas pocas se encuentran dentro del punto focal (generalmente entre 1 y 100 moléculas en un fl). Cuando las partículas cruzan el volumen focal, emiten fluorescencia. Esta luz es recogida por el mismo objetivo y, debido a que está desplazada al rojo con respecto a la luz de excitación, pasa por el espejo dicroico y llega a un detector, normalmente un tubo fotomultiplicador , un detector de fotodiodos de avalancha o un detector de fotón único con nanocables superconductores . La señal electrónica resultante se puede almacenar directamente como una traza de intensidad versus tiempo para analizarla en un momento posterior, o calcularse para generar la autocorrelación directamente (lo que requiere tarjetas de adquisición especiales). La curva FCS por sí sola sólo representa un espectro de tiempo. De ahí se deben extraer conclusiones sobre los fenómenos físicos con modelos adecuados. Los parámetros de interés se encuentran después de ajustar la curva de autocorrelación a formas funcionales modeladas. [17]
El volumen de medición es una convolución de geometrías de iluminación (excitación) y detección, que resultan de los elementos ópticos involucrados. El volumen resultante se describe matemáticamente mediante la función de dispersión puntual (o PSF), y es esencialmente la imagen de una fuente puntual. El PSF se describe a menudo como un elipsoide (con límites poco nítidos) de unos pocos cientos de nanómetros de diámetro focal y casi un micrómetro a lo largo del eje óptico. La forma varía significativamente (y tiene un gran impacto en las curvas FCS resultantes) dependiendo de la calidad de los elementos ópticos (es crucial evitar el astigmatismo y comprobar la forma real del PSF en el instrumento). En el caso de la microscopía confocal y para poros pequeños (alrededor de una unidad Airy), los gaussianos se aproximan bien al PSF:
donde es la intensidad máxima, r y z son la posición radial y axial, y y son los radios radial y axial, y . Esta forma gaussiana se asume al derivar la forma funcional de la autocorrelación.
Normalmente mide entre 200 y 300 nm y es entre 2 y 6 veces más grande. [18] Una forma común de calibrar los parámetros de volumen de medición es realizar FCS en una especie con coeficiente de difusión y concentración conocidos (ver más abajo). Los coeficientes de difusión de los fluoróforos comunes en el agua se dan en una sección posterior.
La aproximación gaussiana funciona en diversos grados dependiendo de los detalles ópticos y, en ocasiones, se pueden aplicar correcciones para compensar los errores de aproximación. [19]

La función de autocorrelación (temporal) es la correlación de una serie temporal consigo misma desplazada en el tiempo , en función de :
¿Dónde está la desviación de la intensidad media? La normalización (denominador) aquí es la más comúnmente utilizada para FCS, porque entonces la correlación en , G (0), está relacionada con el número promedio de partículas en el volumen de medición.
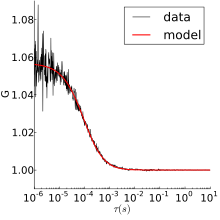
Como ejemplo, en la figura de la derecha se muestran los datos brutos de FCS y su autocorrelación para la rodamina 6G de difusión libre. El gráfico de arriba muestra la intensidad fluorescente versus el tiempo. La intensidad fluctúa a medida que la rodamina 6G entra y sale del volumen focal. En el gráfico inferior está la autocorrelación de los mismos datos. La información sobre la velocidad de difusión y la concentración se puede obtener utilizando uno de los modelos que se describen a continuación.
Para un perfil de iluminación gaussiano , la función de autocorrelación viene dada por la fórmula maestra general [20]
donde el vector denota el desplazamiento estocástico en el espacio de un fluoróforo después del tiempo . La expresión es válida si el número medio de fluoróforos en el volumen focal es bajo y si se pueden ignorar los estados oscuros, etc., del fluoróforo. En particular, no se hizo ninguna suposición sobre el tipo de movimiento de difusión investigado. La fórmula permite una interpretación de como (i) una probabilidad de retorno para parámetros de vigas pequeñas y (ii) la función generadora de momento de if varían.
Para extraer cantidades de interés, se pueden ajustar los datos de autocorrelación, normalmente utilizando un algoritmo de mínimos cuadrados no lineal . La forma funcional del ajuste depende del tipo de dinámica (y de la geometría óptica en cuestión).
Las partículas fluorescentes utilizadas en FCS son pequeñas y, por tanto, experimentan movimientos térmicos en solución. Por tanto, el experimento FCS más simple es la difusión 3D normal, para la cual la autocorrelación es:
donde es la relación entre los radios axial y radial del volumen de medición y es el tiempo de residencia característico. Esta forma se obtuvo asumiendo un volumen de medición gaussiano. Normalmente, el ajuste tendría tres parámetros libres (G(0), y) a partir de los cuales se puede obtener el coeficiente de difusión y la concentración de fluoróforo.
Con la normalización utilizada en la sección anterior, G (0) da el número medio de difusores en el volumen <N>, o de manera equivalente, conociendo el tamaño del volumen de observación, la concentración media:
donde el volumen efectivo se encuentra integrando la forma gaussiana del volumen de medición y viene dado por:
Si las partículas que se difunden se ven obstaculizadas por obstáculos o empujadas por una fuerza (motores moleculares, flujo, etc.), la dinámica a menudo no está suficientemente bien descrita por el modelo de difusión normal, donde el desplazamiento cuadrático medio (MSD) crece linealmente con el tiempo. En cambio, la difusión puede describirse mejor como difusión anómala , donde la dependencia temporal del MSD no es lineal como en la ley de potencia:
donde es un coeficiente de difusión anómalo. La "difusión anómala" comúnmente se refiere sólo a este modelo tan genérico, y no a las muchas otras posibilidades que podrían describirse como anómalas. Además, una ley potencial es, en sentido estricto, la forma esperada sólo para una gama estrecha de sistemas rigurosamente definidos, por ejemplo cuando la distribución de obstáculos es fractal . No obstante, una ley potencial puede ser una aproximación útil para una gama más amplia de sistemas.
La función de autocorrelación FCS para difusión anómala es:
donde el exponente anómalo es el mismo que el anterior y se convierte en un parámetro libre en el ajuste.
Utilizando FCS, se ha demostrado que el exponente anómalo es una indicación del grado de apiñamiento molecular (es menor que uno y más pequeño para mayores grados de apiñamiento). [21]
Si hay partículas en difusión con diferentes tamaños (coeficientes de difusión), es común ajustar a una función que sea la suma de formas de un solo componente:
donde la suma es sobre el número de diferentes tamaños de partículas, indexadas por i, y da la ponderación, que está relacionada con el rendimiento cuántico y la concentración de cada tipo. Esto introduce nuevos parámetros, lo que dificulta el ajuste ya que se debe buscar un espacio de dimensiones superiores. El ajuste de mínimos cuadrados no lineal normalmente se vuelve inestable incluso con un número pequeño de s. Un esquema de ajuste más sólido, especialmente útil para muestras polidispersas, es el Método de Máxima Entropía. [22]
Con difusión junto con un flujo uniforme con velocidad en dirección lateral, la autocorrelación es: [23]
donde es el tiempo de residencia promedio si solo hay flujo (sin difusión).
Una amplia gama de posibles experimentos de FCS implican reacciones químicas que fluctúan continuamente desde el equilibrio debido a movimientos térmicos (y luego se "relajan"). A diferencia de la difusión, que también es un proceso de relajación, las fluctuaciones provocan cambios entre estados de diferentes energías. Un sistema muy simple que muestra relajación química sería un sitio de unión estacionario en el volumen de medición, donde las partículas solo producen señales cuando se unen (por ejemplo, mediante FRET, o si el tiempo de difusión es mucho más rápido que el intervalo de muestreo). En este caso la autocorrelación es:
dónde
es el tiempo de relajación y depende de la cinética de la reacción (velocidad de encendido y apagado), y:
está relacionado con la constante de equilibrio K .
La mayoría de los sistemas con relajación química también muestran difusión mensurable, y la función de autocorrelación dependerá de los detalles del sistema. Si la difusión y la reacción química se desacoplan, la autocorrelación combinada es el producto de las autocorrelaciones química y difusiva.
Las autocorrelaciones anteriores suponen que las fluctuaciones no se deben a cambios en las propiedades fluorescentes de las partículas. Sin embargo, para la mayoría de los fluoróforos (bio)orgánicos, por ejemplo, la proteína verde fluorescente , la rodamina, los tintes Cy3 y Alexa Fluor , una fracción de las partículas iluminadas se excita a un estado triplete (u otros estados de descomposición no radiativos) y luego no emiten. fotones para un tiempo de relajación característico . Normalmente es del orden de microsegundos, que suele ser más pequeño que la dinámica de interés (p. ej. ), pero lo suficientemente grande como para medirlo. Se agrega un término multiplicativo a la autocorrelación para tener en cuenta el estado triplete. Para difusión normal:
donde es la fracción de partículas que han entrado en el estado triplete y es el tiempo de relajación correspondiente al estado triplete. Si la dinámica de interés es mucho más lenta que la relajación del estado triplete, el componente de tiempo corto de la autocorrelación puede simplemente truncarse y el término triplete es innecesario.
La especie fluorescente utilizada en FCS suele ser una biomolécula de interés que ha sido marcada con un fluoróforo (mediante inmunohistoquímica, por ejemplo), o es un fluoróforo desnudo que se utiliza para sondear algún entorno de interés (por ejemplo, el citoesqueleto de una célula). La siguiente tabla proporciona los coeficientes de difusión de algunos fluoróforos comunes en agua a temperatura ambiente y sus longitudes de onda de excitación.
FCS casi siempre se refiere a la medición de autocorrelación temporal de un solo punto, un solo canal, aunque el término "espectroscopia de correlación de fluorescencia" fuera de su contexto científico histórico no implica tal restricción. FCS ha sido ampliado en varias variaciones por diferentes investigadores, y cada extensión genera otro nombre (generalmente un acrónimo).
Mientras que FCS es una medición puntual que proporciona el tiempo de difusión en un volumen de observación determinado, svFCS es una técnica en la que el punto de observación varía para medir los tiempos de difusión en diferentes tamaños de punto. La relación entre el tiempo de difusión y el área del punto es lineal y podría representarse gráficamente para descifrar la principal contribución del confinamiento. La curva resultante se llama ley de difusión. Esta técnica se utiliza en Biología para estudiar la organización de la membrana plasmática de las células vivas.
¿Dónde está la intersección del eje y? En caso de difusión browniana, . En caso de confinamiento debido a dominios aislados, mientras que en el caso de dominios aislados, .
Estudios de svFCS sobre células vivas y artículos de simulación [32] [33] [34] [35] [36]
Espectroscopía de correlación de fluorescencia controlada por volumen de muestreo (SVC-FCS): [37]
FCS de escaneo z [38]
FCS con nanoaperturas: rompiendo la barrera de la difracción [39]
STED-FCS: [40]
A veces, el FCS se utiliza para estudiar interacciones moleculares utilizando diferencias en los tiempos de difusión (por ejemplo, el producto de una reacción de asociación será mayor y, por lo tanto, tendrá tiempos de difusión mayores que los reactivos individualmente); sin embargo, FCS es relativamente insensible a la masa molecular, como se puede ver en la siguiente ecuación que relaciona la masa molecular con el tiempo de difusión de partículas globulares (por ejemplo, proteínas):
donde es la viscosidad de la muestra y es la masa molecular de las especies fluorescentes. En la práctica, los tiempos de difusión deben ser suficientemente diferentes (un factor de al menos 1,6), lo que significa que las masas moleculares deben diferir en un factor de 4. [41] La espectroscopia de correlación cruzada de fluorescencia de color dual (FCCS) mide las interacciones mediante correlacionar dos o más canales fluorescentes (un canal para cada reactivo), lo que distingue las interacciones de manera más sensible que FCS, particularmente cuando el cambio de masa en la reacción es pequeño.
Este conjunto de métodos incluye número y brillo (N&B), [42] histograma de recuento de fotones (PCH), [43] análisis de distribución de intensidad de fluorescencia (FIDA), [44] y análisis de cumulantes. [45] y Análisis de Distribución de Intensidad Espacial. [46] También se informa sobre la combinación de múltiples métodos. [47] La espectroscopia de correlación cruzada de fluorescencia supera la débil dependencia de la velocidad de difusión de la masa molecular al observar la coincidencia multicolor. ¿Qué pasa con las homointeracciones? La solución está en el análisis del brillo. Estos métodos utilizan la heterogeneidad en la distribución de intensidad de la fluorescencia para medir el brillo molecular de diferentes especies en una muestra. Dado que los dímeros contendrán el doble de marcadores fluorescentes que los monómeros, su brillo molecular será aproximadamente el doble que el de los monómeros. De este modo, la luminosidad relativa es una medida sensible a la oligomerización. El brillo molecular promedio ( ) está relacionado con la varianza ( ) y la intensidad promedio ( ) de la siguiente manera: [48]
Aquí y están la intensidad fraccionaria y el brillo molecular, respectivamente, de las especies .
Otro enfoque basado en FCS para estudiar interacciones moleculares utiliza la transferencia de energía por resonancia de fluorescencia (FRET) en lugar de fluorescencia y se llama FRET-FCS. [49] Con FRET, hay dos tipos de sondas, como con FCCS; sin embargo, sólo hay un canal y la luz sólo se detecta cuando las dos sondas están muy cerca, lo suficientemente cerca como para garantizar una interacción. La señal FRET es más débil que con la fluorescencia, pero tiene la ventaja de que sólo hay señal durante una reacción (aparte de la autofluorescencia ).
En la espectroscopia de correlación de fluorescencia de barrido (sFCS), el volumen de medición se mueve a través de la muestra de una manera definida. La introducción del escaneo está motivada por su capacidad para aliviar o eliminar varios problemas distintos que a menudo se encuentran en FCS estándar y, por lo tanto, para ampliar el rango de aplicabilidad de los métodos de correlación de fluorescencia en sistemas biológicos. [50]
Algunas variaciones de FCS solo son aplicables a microscopios láser de barrido en serie. La espectroscopía de correlación de imágenes y sus variaciones se implementaron en un microscopio confocal de barrido o de barrido de dos fotones, pero se transfirieron a otros microscopios, como un microscopio confocal de disco giratorio. Raster ICS (RICS) [51] y FCS sensible a la posición (PSFCS) [52] incorporan el retraso de tiempo entre partes del escaneo de la imagen en el análisis. Además, los escaneos de bajas dimensiones (por ejemplo, un anillo circular) [53] , solo posibles en un sistema de escaneo, pueden acceder a escalas de tiempo entre mediciones de un solo punto y de imagen completa. También se ha creado una ruta de escaneo para seguir las partículas de forma adaptativa. [54]
Cualquiera de los métodos de espectroscopía de correlación de imágenes también se puede realizar en un microscopio confocal de disco giratorio, que en la práctica puede obtener velocidades de obtención de imágenes más rápidas en comparación con un microscopio confocal de barrido láser. Este enfoque se ha aplicado recientemente a la difusión en un entorno complejo que varía espacialmente, produciendo un mapa de resolución de píxeles de un coeficiente de difusión. [55] El mapeo espacial de la difusión con FCS se ha extendido posteriormente al sistema TIRF. [56] El mapeo espacial de la dinámica utilizando técnicas de correlación se había aplicado antes, pero solo en puntos dispersos [57] o con una resolución aproximada. [58]
Cuando el movimiento es lento (en biología, por ejemplo, la difusión en una membrana), obtener estadísticas adecuadas de un experimento de FCS de un solo punto puede llevar un tiempo prohibitivamente largo. Se pueden obtener más datos realizando el experimento en múltiples puntos espaciales en paralelo, utilizando un microscopio confocal de barrido láser. Este enfoque se ha denominado espectroscopia de correlación de imágenes (ICS). [59] Las mediciones pueden entonces promediarse juntas.
Otra variación de ICS realiza una autocorrelación espacial en imágenes, lo que proporciona información sobre la concentración de partículas. [60] La correlación luego se promedia en el tiempo. Si bien el ruido blanco de la cámara no se autocorrelaciona en el tiempo, sí lo hace en el espacio; esto crea una amplitud de ruido blanco en la función de autocorrelación espacial que debe tenerse en cuenta al ajustar la amplitud de autocorrelación para encontrar la concentración de moléculas fluorescentes.
Una extensión natural de las versiones de correlación temporal y espacial es el ICS espacio-temporal (STICS). [58] En STICS no existe un promedio explícito en el espacio o el tiempo (sólo el promedio inherente a la correlación). En sistemas con movimiento no isotrópico (por ejemplo, flujo dirigido, difusión asimétrica), STICS puede extraer la información direccional. Una variación que está estrechamente relacionada con STICS (por la transformada de Fourier) es la espectroscopia de correlación de imágenes en el espacio k (kICS). [61]
También existen versiones de ICS de correlación cruzada, que pueden producir la concentración, distribución y dinámica de moléculas fluorescentes colocalizadas. [59] Las moléculas se consideran colocalizadas cuando las contribuciones de fluorescencia individuales son indistinguibles debido a la superposición de funciones de dispersión puntual de las intensidades de fluorescencia.
Fuente: [62]
PICS es una poderosa herramienta de análisis que resuelve correlaciones en la longitud nanométrica y la escala de tiempo de milisegundos. Adaptado de métodos de espectroscopía de correlación de imágenes espacio-temporal, [58] explota la alta precisión posicional del seguimiento de una sola partícula. Mientras que los métodos de seguimiento convencionales fallan si se cruzan múltiples trayectorias de partículas, este método funciona en principio para densidades de moléculas y parámetros dinámicos arbitrariamente grandes (por ejemplo, coeficientes de difusión, velocidades), siempre que se puedan identificar moléculas individuales. Es computacionalmente barato y robusto y permite identificar y cuantificar movimientos (por ejemplo, difusión, transporte activo, difusión confinada) dentro de un conjunto de partículas, sin ningún conocimiento a priori sobre la dinámica.
Se encuentra disponible una extensión de espectroscopia de correlación cruzada de imágenes de partículas (PICCS) para procesos biológicos que involucran múltiples compañeros de interacción, como se puede observar mediante microscopía de dos colores. [63]
Las imágenes de fluctuación óptica de superresolución (SOFI) son una técnica de superresolución que logra resoluciones espaciales por debajo del límite de difracción mediante análisis de posprocesamiento con ecuaciones de correlación, similar a FCS. Si bien los informes originales de SOFI utilizaron fluctuaciones del parpadeo estacionario de fluoróforos, FCS se ha combinado con SOFI, donde las fluctuaciones se producen a partir de sondas en difusión para producir mapas espaciales de súper resolución de coeficientes de difusión. [64] Esto se ha aplicado para comprender la difusión y las propiedades espaciales de materiales porosos y confinados. Esto incluye agarosa [64] e hidrogeles de PNIPAM sensibles a la temperatura, [65] cristales líquidos, [64] y polímeros de fases separadas y condensados de ARN/proteína. [66]
La fluorescencia de reflexión interna total (TIRF) es un método de microscopía que solo es sensible a una capa delgada cerca de la superficie de un cubreobjetos, lo que minimiza en gran medida la fluorescencia de fondo. FCS se ha extendido a ese tipo de microscopio y se denomina TIR-FCS. [67] Debido a que la intensidad de la fluorescencia en TIRF cae exponencialmente con la distancia desde el cubreobjetos (en lugar de como un gaussiano con un confocal), la función de autocorrelación es diferente.
La microscopía de fluorescencia de lámina de luz o microscopía de imágenes planas selectivas (SPIM) utiliza una iluminación que se realiza perpendicularmente a la dirección de observación, mediante el uso de una fina lámina de luz (láser). Bajo ciertas condiciones, este principio de iluminación se puede combinar con la espectroscopia de correlación de fluorescencia, para permitir imágenes resueltas espacialmente de la movilidad y las interacciones de partículas fluorescentes, como proteínas marcadas con GFP, dentro de muestras biológicas vivas. [68]
Existen dos alternativas principales de no correlación al FCS que se utilizan ampliamente para estudiar la dinámica de especies fluorescentes.
En FRAP , una región se expone brevemente a una luz intensa, fotoblanqueando irremediablemente los fluoróforos, y se obtienen imágenes de la recuperación de la fluorescencia debido a la difusión de los fluoróforos cercanos (no blanqueados). Una ventaja principal de FRAP sobre FCS es la facilidad de interpretar experimentos cualitativos comunes en biología celular. Las diferencias entre líneas celulares, o regiones de una célula, o antes y después de la aplicación de un fármaco, a menudo pueden caracterizarse mediante una simple inspección de las películas. Los experimentos FCS requieren un nivel de procesamiento y son más sensibles a influencias potencialmente confusas como: difusión rotacional, vibraciones, fotoblanqueo, dependencia de la iluminación y el color de fluorescencia, estadísticas inadecuadas, etc. Es mucho más fácil cambiar el volumen de medición en FRAP, lo que permite mayor control. En la práctica, los volúmenes suelen ser mayores que en FCS. Si bien los experimentos FRAP suelen ser más cualitativos, algunos investigadores están estudiando FRAP cuantitativamente e incluyen dinámicas vinculantes. [69] Una desventaja de FRAP en biología celular es la perturbación de la célula por radicales libres causada por el fotoblanqueo. También es menos versátil, ya que no puede medir la concentración, la difusión rotacional o la colocalización. FRAP requiere una concentración significativamente mayor de fluoróforos que FCS.
En el seguimiento de partículas, se miden las trayectorias de un conjunto de partículas, normalmente aplicando algoritmos de seguimiento de partículas a las películas.[1] El seguimiento de partículas tiene la ventaja de que toda la información dinámica se mantiene en la medición, a diferencia del FCS, donde la correlación promedia la dinámica en una única curva suave. La ventaja es evidente en sistemas que muestran difusión compleja, donde calcular directamente el desplazamiento cuadrático medio permite una comparación directa con la difusión normal o de ley potencial. Para aplicar el seguimiento de partículas, las partículas deben ser distinguibles y, por lo tanto, tener una concentración menor que la requerida para FCS. Además, el seguimiento de partículas es más sensible al ruido, lo que a veces puede afectar los resultados de forma impredecible.
Los avances recientes en la nanofotónica ultravioleta han llevado al desarrollo del estudio de una sola molécula en proteínas sin etiquetas excitándolas con luz ultravioleta profunda y estudiando los procesos dinámicos. [70] [71] [72]
Varias ventajas tanto en la resolución espacial como en la minimización del fotodaño/fotoblanqueo en muestras orgánicas y/o biológicas se obtienen mediante FCS de excitación de dos o tres fotones. [73] [74] [75] [76] [77]