La espectroscopia de correlación cruzada de fluorescencia ( FCCS ) es una técnica espectroscópica que examina las interacciones de partículas fluorescentes de diferentes colores a medida que se difunden aleatoriamente a través de un volumen de detección microscópico a lo largo del tiempo, en condiciones estables. [1]
Eigen y Rigler introdujeron por primera vez el método de espectroscopia de correlación cruzada de fluorescencia (FCCS) en 1994. Más tarde, en 1997, Schwille implementó este método experimentalmente. [2] [3]
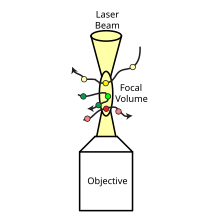
La FCCS es una extensión del método de espectroscopia de correlación de fluorescencia (FCS) que utiliza dos moléculas fluorescentes en lugar de una que emite colores diferentes. La técnica mide fluctuaciones coincidentes de intensidad verde y roja de moléculas distintas que se correlacionan si las partículas marcadas con verde y rojo se mueven juntas a través de un volumen confocal predefinido. [2] La FCCS utiliza dos especies que están marcadas de forma independiente con dos sondas fluorescentes diferentes de diferentes colores. Estas sondas fluorescentes se excitan y detectan mediante dos fuentes de luz láser y detectores diferentes, normalmente etiquetados como "verde" y "rojo". Al combinar la FCCS con un microscopio confocal , se destacan las capacidades de la técnica, ya que se hace posible detectar moléculas de fluorescencia en volúmenes de femtolitros dentro del rango nanomolar, con una alta relación señal-ruido y en una escala de tiempo de microsegundos. [4]
La función de correlación cruzada normalizada se define para dos especies fluorescentes, G y R, que son canales verde y rojo independientes, respectivamente:
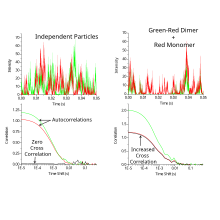
donde las señales fluorescentes diferenciales en un momento específico y en un tiempo de retardo se correlacionan posteriormente entre sí. En ausencia de filtración espectral (cuando la señal de fluorescencia de un canal adyacente es visible en el canal que se observa), la función de correlación cruzada es cero para las partículas que no interactúan. A diferencia del FCS, la función de correlación cruzada aumenta con un número creciente de partículas que interactúan.
La FCCS se utiliza principalmente para estudiar interacciones biomoleculares tanto en células vivas como in vitro. [5] [2] Permite medir estequiometrías moleculares simples y constantes de unión. [3] Es una de las pocas técnicas que pueden proporcionar información sobre las interacciones proteína-proteína en un momento y ubicación específicos dentro de una célula viva. A diferencia de la transferencia de energía de resonancia de fluorescencia , la FCCS no tiene un límite de distancia para las interacciones, lo que la hace adecuada para sondear complejos grandes. Sin embargo, la FCCS requiere la difusión activa de los complejos a través del foco del microscopio en una escala de tiempo relativamente corta, típicamente segundos.
La función matemática utilizada para modelar las curvas de correlación cruzada en FCCS es ligeramente más compleja en comparación con la utilizada en FCS. Una de las principales diferencias es el volumen efectivo de observación superpuesto, denotado como en el que los canales G y R forman un único volumen de observación:
donde y son parámetros radiales y y son los parámetros axiales para los canales G y R respectivamente.
Por lo tanto , el tiempo de difusión para una especie doblemente fluorescente (G y R) se describe de la siguiente manera:
donde es el coeficiente de difusión de la partícula doblemente fluorescente.
La curva de correlación cruzada generada a partir de la difusión de partículas fluorescentes doblemente marcadas se puede modelar en canales separados de la siguiente manera:
En el caso ideal, la función de correlación cruzada es proporcional a la concentración del complejo fluorescente doblemente marcado:
con
La amplitud de correlación cruzada es directamente proporcional a la concentración de especies doblemente marcadas (rojas y verdes). [4] [6]
La FCCS mide las fluctuaciones coincidentes de intensidad de verde y rojo de moléculas distintas que se correlacionan si las partículas marcadas con verde y rojo se mueven juntas a través de un volumen confocal predefinido. Para realizar la espectroscopia de correlación cruzada de fluorescencia (FCCS), las muestras de interés se marcan primero con sondas fluorescentes de diferentes colores. La configuración de la FCCS generalmente incluye un microscopio confocal, dos fuentes láser y dos detectores. El microscopio confocal se utiliza para enfocar los rayos láser y recolectar las señales de fluorescencia. Luego, las señales de los detectores se recopilan y registran a lo largo del tiempo. [6] [7] El análisis de datos implica la correlación cruzada de las señales para determinar el grado de correlación entre las dos sondas fluorescentes. Esta información se puede utilizar para extraer datos sobre la estequiometría y las constantes de unión de los complejos moleculares, así como el momento y la ubicación de las interacciones dentro de las células vivas. [6]
La espectroscopia de correlación cruzada de fluorescencia (FCCS) tiene varias aplicaciones en el campo de la biofísica y la bioquímica . La espectroscopia de correlación cruzada de fluorescencia (FCCS) es una técnica poderosa que permite la investigación de interacciones entre varios tipos de biomoléculas , incluidas proteínas , ácidos nucleicos y lípidos . [8]
La FCCS es una de las pocas técnicas que pueden proporcionar información sobre las interacciones proteína-proteína en un momento y lugar específicos dentro de una célula viva. La FCCS se puede utilizar para estudiar la dinámica de las biomoléculas en células vivas, incluidas sus tasas de difusión y localización. [9]
Esto puede proporcionar información sobre la función y la regulación de los procesos celulares. A diferencia de la transferencia de energía por resonancia de Förster , el FCCS no tiene un límite de distancia para las interacciones, lo que lo hace adecuado para sondear complejos grandes. Sin embargo, el FCCS requiere la difusión activa de los complejos a través del foco del microscopio en una escala de tiempo relativamente corta, típicamente segundos. El FCCS permite medir estequiometrías moleculares simples y constantes de enlace . [9]