La quimiosmosis es el movimiento de iones a través de una estructura unida a una membrana semipermeable , en dirección contraria a su gradiente electroquímico . Un ejemplo importante es la formación de trifosfato de adenosina (ATP) mediante el movimiento de iones de hidrógeno (H + ) a través de una membrana durante la respiración celular o la fotosíntesis .
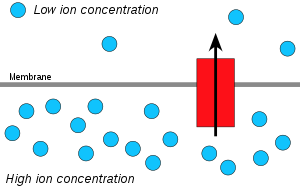
Los iones de hidrógeno, o protones , se difundirán desde una región de alta concentración de protones a una región de menor concentración de protones, y se puede aprovechar un gradiente de concentración electroquímica de protones a través de una membrana para producir ATP. Este proceso está relacionado con la ósmosis , el movimiento del agua a través de una membrana selectiva, por lo que se denomina "quimiosmosis".
La ATP sintasa es la enzima que produce ATP por quimiosmosis. Permite que los protones pasen a través de la membrana y utiliza la diferencia de energía libre para convertir el fosforilado adenosín difosfato (ADP) en ATP. La ATP sintasa contiene dos partes: CF0 (presente en la membrana tilacoide) y CF1 (sobresale en la superficie exterior de la membrana tilacoide). La ruptura del gradiente de protones conduce a un cambio conformacional en CF1, proporcionando suficiente energía en el proceso para convertir ADP en ATP. La generación de ATP por quimiosmosis ocurre en las mitocondrias y los cloroplastos , así como en la mayoría de las bacterias y arqueas . Por ejemplo, en los cloroplastos durante la fotosíntesis, una cadena de transporte de electrones bombea iones H + (protones) en el estroma (fluido) a través de la membrana tilacoide hasta los espacios tilacoides. La energía almacenada se utiliza para fotofosforilar ADP, produciendo ATP, a medida que los protones se mueven a través de la ATP sintasa.
Peter D. Mitchell propuso la hipótesis quimiosmótica en 1961. [1] En resumen, la hipótesis era que la mayor parte de la síntesis de trifosfato de adenosina (ATP) en las células que respiran proviene del gradiente electroquímico a través de las membranas internas de las mitocondrias mediante el uso de la energía del NADH y FADH 2 formados durante la descomposición oxidativa de moléculas ricas en energía como la glucosa .
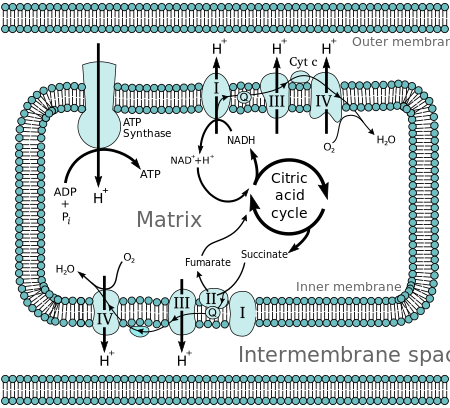
Moléculas como la glucosa se metabolizan para producir acetil CoA como un intermediario bastante rico en energía. La oxidación de la acetil coenzima A (acetil-CoA) en la matriz mitocondrial está acoplada a la reducción de una molécula transportadora como el dinucleótido de nicotinamida y adenina (NAD) y el dinucleótido de flavina y adenina (FAD). [2] Los transportadores pasan electrones a la cadena de transporte de electrones (CTE) en la membrana mitocondrial interna , que a su vez los pasa a otras proteínas en la CTE. La energía en cada paso de transferencia redox se utiliza para bombear protones desde la matriz al espacio intermembrana, almacenando energía en forma de un gradiente electroquímico transmembrana . Los protones regresan a través de la membrana interna a través de la enzima ATP sintasa . El flujo de protones de regreso a la matriz de la mitocondria a través de la ATP sintasa proporciona suficiente energía para que el ADP se combine con fosfato inorgánico para formar ATP.
Esta fue una propuesta radical en su momento y no fue bien aceptada. La opinión predominante era que la energía de la transferencia de electrones se almacenaba como un intermediario estable de alto potencial, un concepto químicamente más conservador. El problema con el paradigma más antiguo es que nunca se encontró un intermediario de alta energía, y la evidencia del bombeo de protones por los complejos de la cadena de transferencia de electrones se hizo demasiado grande para ser ignorada. Finalmente, el peso de la evidencia comenzó a favorecer la hipótesis quimiosmótica, y en 1978 Peter D. Mitchell recibió el Premio Nobel de Química . [3]
El acoplamiento quimiosmótico es importante para la producción de ATP en las mitocondrias , los cloroplastos [4] y muchas bacterias y arqueas . [5]
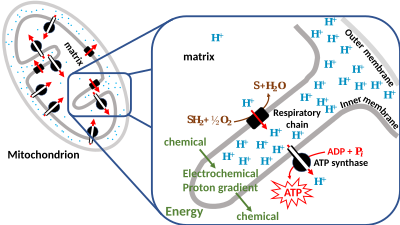
El movimiento de iones a través de la membrana depende de una combinación de dos factores:
Estos dos gradientes tomados en conjunto pueden expresarse como un gradiente electroquímico .
Sin embargo, las bicapas lipídicas de las membranas biológicas son barreras para los iones. Por eso, la energía se puede almacenar como una combinación de estos dos gradientes a través de la membrana. Solo las proteínas de membrana especiales, como los canales iónicos, pueden permitir a veces que los iones se muevan a través de la membrana (véase también: Transporte de membrana ). En la hipótesis quimiosmótica, una ATP sintasa transmembrana es fundamental para convertir la energía del flujo espontáneo de protones a través de ellas en energía química de los enlaces ATP.
Por ello, los investigadores crearon el término fuerza protón-motriz (PMF), derivado del gradiente electroquímico mencionado anteriormente. Puede describirse como la medida de la energía potencial almacenada ( potencial quimiosmótico ) como una combinación de gradientes de protones y voltaje (potencial eléctrico) a través de una membrana. El gradiente eléctrico es una consecuencia de la separación de cargas a través de la membrana (cuando los protones H + se mueven sin un contraión , como el cloruro Cl − ).
En la mayoría de los casos, la fuerza protón-motriz es generada por una cadena de transporte de electrones que actúa como una bomba de protones, utilizando la energía libre de Gibbs de las reacciones redox para bombear protones (iones de hidrógeno) a través de la membrana, separando la carga a través de la membrana. En las mitocondrias, la energía liberada por la cadena de transporte de electrones se utiliza para mover protones desde la matriz mitocondrial (lado N) al espacio intermembrana (lado P). Mover los protones fuera de la mitocondria crea una menor concentración de protones cargados positivamente en su interior, lo que resulta en un exceso de carga negativa en el interior de la membrana. El gradiente de potencial eléctrico es de aproximadamente -170 mV [6] , negativo en el interior (N). Estos gradientes, la diferencia de carga y la diferencia de concentración de protones, crean un gradiente electroquímico combinado a través de la membrana, a menudo expresado como la fuerza protón-motriz (PMF). En las mitocondrias, el PMF está formado casi en su totalidad por el componente eléctrico, pero en los cloroplastos el PMF está formado principalmente por el gradiente de pH porque la carga de los protones H + se neutraliza por el movimiento de Cl− y otros aniones. En cualquier caso, el PMF debe ser mayor que unos 460 mV (45 kJ/mol) para que la ATP sintasa pueda fabricar ATP.
La fuerza protón-motriz se deriva de la energía libre de Gibbs . Sea N el interior de una célula y P el exterior. Entonces [6]
dónde
El cambio de energía libre de Gibbs molar se interpreta frecuentemente como un potencial iónico electroquímico molar .
Para un gradiente electroquímico de protones y como consecuencia:
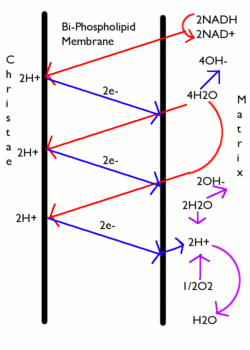
dónde
Mitchell definió la fuerza protón-motriz (PMF) como
Por ejemplo, implica . En esta ecuación toma la forma:
.
Tenga en cuenta que la importación espontánea de protones desde el lado P (relativamente más positivo y ácido) al lado N (relativamente más negativo y alcalino), es negativa (similar a ), mientras que el PMF es positivo (similar al potencial de celda redox ).
Vale la pena señalar que, como en cualquier proceso de transporte transmembrana, la PMF es direccional. El signo de la diferencia de potencial eléctrico transmembrana se elige para representar el cambio en la energía potencial por unidad de carga que fluye hacia la célula como se indicó anteriormente. Además, debido al bombeo de protones impulsado por rédox por los sitios de acoplamiento, el gradiente de protones siempre es interno-alcalino. Por ambas razones, los protones fluyen espontáneamente, desde el lado P al lado N; la energía libre disponible se utiliza para sintetizar ATP (ver más abajo). Por esta razón, la PMF se define para la importación de protones, que es espontánea. La PMF para la exportación de protones, es decir, el bombeo de protones catalizado por los sitios de acoplamiento, es simplemente el negativo de PMF(importación).
La espontaneidad de la importación de protones (del lado P al lado N) es universal en todas las membranas bioenergéticas. [8] Este hecho no se reconoció antes de la década de 1990, porque el lumen del tilacoide del cloroplasto se interpretó como una fase interior, pero de hecho es topológicamente equivalente al exterior del cloroplasto. Azzone et al. destacaron que la fase interior (lado N de la membrana) es el citoplasma bacteriano, la matriz mitocondrial o el estroma del cloroplasto; el lado exterior (P) es el espacio periplásmico bacteriano, el espacio intermembrana mitocondrial o el lumen del cloroplasto. Además, la tomografía 3D de la membrana interna mitocondrial muestra que sus extensas invaginaciones están apiladas, de manera similar a los discos tilacoides; por lo tanto, el espacio intermembrana mitocondrial es topológicamente bastante similar al lumen del cloroplasto: [9]
La energía expresada aquí como energía libre de Gibbs, gradiente electroquímico de protones o fuerza protón-motriz (PMF), es una combinación de dos gradientes a través de la membrana:
Cuando un sistema alcanza el equilibrio, no obstante, las concentraciones a ambos lados de la membrana no tienen por qué ser iguales. El movimiento espontáneo a través de la membrana de potencial está determinado tanto por los gradientes de concentración como de potencial eléctrico.
La energía libre de Gibbs molar de la síntesis de ATP
También se denomina potencial de fosforilación. La relación de concentración de equilibrio se puede calcular comparando y , por ejemplo en el caso de la mitocondria de los mamíferos: [9]
H + / ATP = ΔG p / (Δp / 10,4 kJ·mol −1 /mV) = 40,2 kJ·mol −1 / (173,5 mV / 10,4 kJ·mol −1 /mV) = 40,2 / 16,7 = 2,4. La relación real entre el número de copias de la subunidad c que se une al protón y la subunidad beta que sintetiza ATP es 8/3 = 2,67, lo que demuestra que, en estas condiciones, la mitocondria funciona con una eficiencia del 90 % (2,4/2,67). [9]
De hecho, la eficiencia termodinámica es en su mayoría menor en las células eucariotas porque el ATP debe exportarse desde la matriz al citoplasma, y el ADP y el fosfato deben importarse desde el citoplasma. Esto "cuesta" la importación de un protón "extra" por ATP, [6] [7] por lo que la eficiencia real es solo del 65% (= 2,4/3,67).

La descomposición completa de la glucosa liberando su energía se denomina respiración celular . Los últimos pasos de este proceso ocurren en las mitocondrias. Las moléculas reducidas NADH y FADH 2 se generan mediante el ciclo de Krebs , la glucólisis y el procesamiento del piruvato . Estas moléculas pasan electrones a una cadena de transporte de electrones , que libera la energía del oxígeno para crear un gradiente de protones a través de la membrana mitocondrial interna . La ATP sintasa luego utiliza la energía almacenada en este gradiente para fabricar ATP. Este proceso se denomina fosforilación oxidativa porque utiliza la energía liberada por la oxidación de NADH y FADH 2 para fosforilar ADP en ATP .
Las reacciones luminosas de la fotosíntesis generan ATP por la acción de la quimiosmosis. Los fotones de la luz solar son recibidos por el complejo de antena del Fotosistema II , que excita a los electrones a un nivel de energía más alto . Estos electrones viajan por una cadena de transporte de electrones , lo que hace que los protones sean bombeados activamente a través de la membrana tilacoide hacia el lumen tilacoide . Estos protones luego fluyen por su gradiente de potencial electroquímico a través de una enzima llamada ATP-sintasa, creando ATP por la fosforilación de ADP a ATP. Los electrones de la reacción luminosa inicial llegan al Fotosistema I , luego son elevados a un nivel de energía más alto por la energía de la luz y luego recibidos por un aceptor de electrones y reducen NADP + a NADPH . Los electrones perdidos del Fotosistema II son reemplazados por la oxidación del agua, que se "divide" en protones y oxígeno por el complejo generador de oxígeno (OEC, también conocido como WOC, o complejo oxidante de agua). Para generar una molécula de oxígeno diatómico, se deben absorber 10 fotones por los fotosistemas I y II, cuatro electrones deben moverse a través de los dos fotosistemas y se generan 2 NADPH (utilizados posteriormente para la fijación del dióxido de carbono en el ciclo de Calvin).
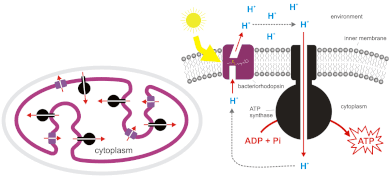
Las bacterias y las arqueas también pueden utilizar la quimiosmosis para generar ATP. Las cianobacterias , las bacterias verdes del azufre y las bacterias púrpuras sintetizan ATP mediante un proceso llamado fotofosforilación . [6] [7] Estas bacterias utilizan la energía de la luz para crear un gradiente de protones utilizando una cadena de transporte de electrones fotosintética . Las bacterias no fotosintéticas como E. coli también contienen ATP sintasa . De hecho, las mitocondrias y los cloroplastos son el producto de la endosimbiosis y se remontan a los procariotas incorporados. Este proceso se describe en la teoría endosimbiótica . El origen de la mitocondria desencadenó el origen de los eucariotas, y el origen del plástido el origen de los Archaeplastida, uno de los principales supergrupos eucariotas. [ cita requerida ]
La fosforilación quimiosmótica es la tercera vía que produce ATP a partir de fosfato inorgánico y una molécula de ADP. Este proceso forma parte de la fosforilación oxidativa.
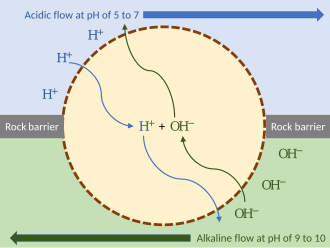
Un modelo escalonado para el surgimiento de la quimiosmosis, un elemento clave en el origen de la vida en la Tierra, propone que los organismos primordiales utilizaron el ciclo térmico como fuente de energía (termosíntesis), funcionando esencialmente como un motor térmico: [11]
Los respiraderos hidrotermales de aguas profundas , que emitían agua caliente ácida o alcalina, habrían creado gradientes externos de protones, que proporcionaron energía que los organismos primigenios podrían haber aprovechado. Para mantener separados los flujos, un organismo de este tipo podría haberse encajado en la roca del respiradero hidrotermal, expuesto al flujo hidrotermal por un lado y al agua más alcalina por el otro. Mientras la membrana del organismo (o los canales iónicos pasivos dentro de ella) sean permeables a los protones, el mecanismo puede funcionar sin bombas de iones. Un protoorganismo de este tipo podría haber desarrollado mecanismos adicionales, como bombas de iones y ATP sintasa. [10]
Una fuente alternativa propuesta para la energía quimiosmótica que se desarrolla a través de las estructuras membranosas es que si un aceptor de electrones, el ferricianuro, está dentro de una vesícula y el donante de electrones está afuera, las quinonas transportadas por meteoritos carbonosos recogen electrones y protones del donante. Liberarían electrones a través de la membrana lipídica por difusión al ferricianuro dentro de las vesículas y liberarían protones, lo que produce gradientes por encima de pH 2; el proceso es propicio para el desarrollo de gradientes de protones. [12] [13]