La geometría piramidal cuadrada describe la forma de ciertos compuestos químicos con la fórmula ML 5 donde L es un ligando . Si los átomos del ligando estuvieran conectados, la forma resultante sería la de una pirámide con una base cuadrada . La simetría del grupo puntual involucrada es del tipo C 4v . La geometría es común para ciertos compuestos del grupo principal que tienen un par solitario estereoquímicamente activo , como se describe en la teoría VSEPR . Ciertos compuestos cristalizan tanto en la estructura bipiramidal trigonométrica como en la estructura piramidal cuadrada, en particular [Ni(CN) 5 ] 3− . [1]
A medida que una molécula bipiramidal trigonal experimenta una pseudorrotación de Berry , pasa por una etapa intermedia con la geometría piramidal cuadrada. Por lo tanto, aunque la geometría rara vez se considera como el estado fundamental, se accede a ella mediante una distorsión de baja energía de una bipirámide trigonal.
La pseudorrotación también se produce en moléculas piramidales cuadradas. Las moléculas con esta geometría, a diferencia de las bipiramidales trigonales, presentan una vibración más intensa. El mecanismo utilizado es similar al mecanismo de Berry.
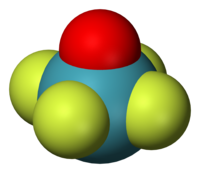
Algunos compuestos moleculares que adoptan una geometría piramidal cuadrada son XeOF 4 , [2] y varios pentafluoruros de halógeno (XF 5 , donde X = Cl, Br, I). [3] [4] Los complejos de vanadio (IV), como el acetilacetonato de vanadilo , [VO(acac) 2 ], son piramidales cuadradas (acac = acetilacetonato, el anión desprotonado de la acetilacetona (2,4-pentanodiona)).