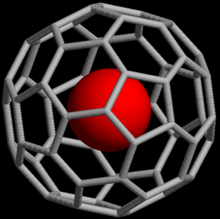

Los fullerenos endoédricos , también llamados endofullerenos , son fullerenos que tienen átomos , iones o grupos adicionales encerrados dentro de sus esferas internas. El primer complejo de lantano C 60 llamado La@C 60 se sintetizó en 1985. [2] La @ ( arroba ) en el nombre refleja la noción de una pequeña molécula atrapada dentro de una capa. Existen dos tipos de complejos endoédricos: metalofullerenos endoédricos y fullerenos dopados no metálicos .
En una notación de fórmula química tradicional, un buckminsterfullereno (C 60 ) con un átomo (M) se representaba simplemente como MC 60 independientemente de si M estaba dentro o fuera del fullereno. Para permitir discusiones más detalladas con una mínima pérdida de información, en 1991 se propuso una notación más explícita, [2] donde los átomos enumerados a la izquierda del signo @ están situados dentro de la red compuesta por los átomos enumerados a la derecha. . El ejemplo anterior se denotaría entonces como M@C 60 si M estuviera dentro de la red de carbono. Un ejemplo más complejo es K 2 (K@C 59 B), que denota "una jaula de fullereno de 60 átomos con un átomo de boro sustituido por un carbono en la red geodésica, un único potasio atrapado en su interior y dos átomos de potasio adheridos a la red geodésica". afuera." [2]
Los autores han explicado que la elección del símbolo es concisa, fácil de imprimir y transmitir electrónicamente (la arroba está incluida en ASCII , en el que se basan la mayoría de los esquemas de codificación de caracteres modernos), y los aspectos visuales que sugieren la estructura de un endoédrico. fullereno.
El dopado de fullerenos con metales electropositivos se realiza en un reactor de arco o mediante evaporación láser. Los metales pueden ser metales de transición como escandio , itrio y lantánidos como lantano y cerio . También son posibles complejos endoédricos con elementos de metales alcalinotérreos como bario y estroncio , metales alcalinos como potasio y metales tetravalentes como uranio , circonio y hafnio . Sin embargo, la síntesis en el reactor de arco es inespecífica. Además de los fullerenos sin carga, los metalofullerenos endoédricos se desarrollan con diferentes tamaños de jaula, como La@C 60 o La@C 82 , y como diferentes jaulas de isómeros. Además de la presencia dominante de jaulas monometálicas, también se aislaron numerosos complejos endoédricos dimetálicos y fullerenos de carburo trimetálico como Sc 3 C 2 @C 80 .
En 1999 un descubrimiento llamó mucho la atención. Con la síntesis del Sc 3 N@C 80 por Harry Dorn y sus colaboradores, se logró por primera vez la inclusión de un fragmento de molécula en una jaula de fullereno. Este compuesto se puede preparar mediante vaporización por arco a temperaturas de hasta 1100 °C de varillas de grafito empaquetadas con nitruro de hierro de óxido de escandio (III) y polvo de grafito en un generador de KH en una atmósfera de nitrógeno a 300 Torr . [3]
Los metalofullerenos endoédricos se caracterizan por el hecho de que los electrones se transferirán del átomo metálico a la jaula del fullereno y que el átomo metálico ocupa una posición descentrada en la jaula. El tamaño de la transferencia de carga no siempre es sencillo de determinar. En la mayoría de los casos es entre 2 y 3 unidades de carga , en el caso del La 2 @C 80 sin embargo puede ser incluso alrededor de 6 electrones como en Sc 3 N@C 80 que se describe mejor como [Sc 3 N] + 6 @[C 80 ] −6 . Estas jaulas de fullerenos aniónicos son moléculas muy estables y no tienen la reactividad asociada con los fullerenos vacíos ordinarios. Son estables en el aire hasta temperaturas muy altas (600 a 850 °C).
La falta de reactividad en las reacciones de Diels-Alder se utiliza en un método para purificar compuestos [C 80 ] −6 a partir de una mezcla compleja de fullerenos vacíos y parcialmente llenos de diferentes tamaños de jaula. [3] En este método, la resina Merrifield se modifica como una resina de ciclopentadienilo y se usa como fase sólida frente a una fase móvil que contiene la mezcla compleja en una operación de cromatografía en columna . Sólo los fullerenos muy estables como [Sc 3 N] +6 @[C 80 ] −6 pasan a través de la columna sin reaccionar.
En Ce 2 @C 80 los dos átomos metálicos exhiben una interacción no enlazada. [4] Dado que todos los anillos de seis miembros en C 80 -I h son iguales [4] los dos átomos de Ce encapsulados exhiben un movimiento aleatorio tridimensional. [5] Esto se evidencia por la presencia de sólo dos señales en el espectro de 13 C- NMR . Es posible forzar a los átomos metálicos a detenerse en el ecuador, como lo muestra la cristalografía de rayos X, cuando el fullereno se funcionaliza exaédricamente mediante un grupo sililo de donación de electrones en una reacción de Ce 2 @C 80 con 1,1,2,2. -tetrakis(2,4,6-trimetilfenil)-1,2-disilirano.
Gd@C 82 (OH) 22 , un metalofluorenol endoédrico, puede inhibir competitivamente la activación del dominio WW en el oncogén YAP1 . Fue desarrollado originalmente como un agente de contraste para resonancias magnéticas . [6] [7]
Los complejos endoédricos He@C 60 y Ne@C 60 se preparan presurizando C 60 hasta ca. 3 bar en atmósfera de gases nobles. [8] En estas condiciones, aproximadamente una de cada 650.000 jaulas de C 60 estaba dopada con un átomo de helio . También se demostró la formación de complejos endoédricos con helio , neón , argón , criptón y xenón , así como numerosos aductos del compuesto He@C 60 [9] con presiones de 3 kbar y una incorporación de hasta el 0,1% de los gases nobles.
Mientras que los gases nobles son químicamente muy inertes y comúnmente existen como átomos individuales, este no es el caso del nitrógeno y el fósforo , por lo que la formación de los complejos endoédricos N@C 60 , N@C 70 y P@C 60 es más sorprendente. El átomo de nitrógeno se encuentra en su estado inicial electrónico ( 4 S 3/2 ) y es muy reactivo. Sin embargo, N@C 60 es suficientemente estable para que sea posible una derivatización exoédrica del aducto mono al hexa del éster etílico del ácido malónico . En estos compuestos no se produce ninguna transferencia de carga del átomo de nitrógeno del centro a los átomos de carbono de la jaula. Por lo tanto, los 13 acoplamientos de C , que se observan muy fácilmente en los metalofullerenos endoédricos, sólo se pudieron observar en el N@C 60 en un espectro de alta resolución como hombros de la línea central.
El átomo central de estos complejos endoédricos se encuentra en el centro de la jaula. Mientras que otras trampas atómicas requieren equipos complejos, por ejemplo, enfriamiento por láser o trampas magnéticas , los fullerenos endoédricos representan una trampa atómica que es estable a temperatura ambiente y durante un tiempo arbitrariamente largo. Las trampas atómicas o de iones son de gran interés ya que las partículas están presentes libres de interacción (significativa) con su entorno, lo que permite explorar fenómenos mecánicos cuánticos únicos. Por ejemplo, la compresión de la función de onda atómica como consecuencia del empaquetamiento en la jaula podría observarse con espectroscopía ENDOR . El átomo de nitrógeno se puede utilizar como sonda para detectar los cambios más pequeños en la estructura electrónica de su entorno.
A diferencia de los compuestos metaloendoédricos, estos complejos no pueden formarse en forma de arco. Los átomos se implantan en el material de partida del fullereno mediante descarga de gas (complejos de nitrógeno y fósforo) o mediante implantación directa de iones . Alternativamente, los fullerenos de hidrógeno endoédricos se pueden producir abriendo y cerrando un fullereno mediante métodos de química orgánica . Un ejemplo reciente de fullerenos endoédricos incluye moléculas individuales de agua encapsuladas en C60 . [10]
Se predice que los endofullerenos de gases nobles exhiben una polarizabilidad inusual. Así, los valores calculados de la polarizabilidad media de Ng@C 60 no son iguales a la suma de la polarizabilidad de la jaula del fullereno y del átomo atrapado, es decir, hay una exaltación de la polarizabilidad. [11] [12] El signo de la exaltación de la polarizabilidad Δ α depende del número de átomos en una molécula de fullereno: para fullerenos pequeños ( ), es positivo; para los más grandes ( ), es negativo (depresión de la polarizabilidad). Se ha propuesto la siguiente fórmula, que describe la dependencia de Δα con respecto a n: Δ α = α Ng (2 e −0,06( n – 20) −1). Describe las polarizabilidades medias calculadas por DFT de endofullerenos Ng @ C 60 con suficiente precisión. Los datos calculados permiten utilizar fullereno C 60 como jaula de Faraday, [13] que aísla el átomo encapsulado del campo eléctrico externo. Las relaciones mencionadas deberían ser típicas de las estructuras endoédricas más complicadas (por ejemplo, C 60 @C 240 [14] y "cebollas" gigantes que contienen fullereno [15] ).
Se han sintetizado fullerenos cerrados que encapsulan pequeñas moléculas. Son representativas la síntesis del endofullereno de dihidrógeno H 2 @C 60 , el endofullereno de agua H 2 O @ C 60 , el endofullereno de fluoruro de hidrógeno HF @ C 60 y el endofullereno de metano CH 4 @ C 60 . [16] [17] [18] [19] Las moléculas encapsuladas muestran propiedades físicas inusuales que han sido estudiadas mediante una variedad de métodos físicos. [20] Como se muestra teóricamente, [21] la compresión de endofullerenos moleculares (por ejemplo, H 2 @C 60 ) puede conducir a la disociación de las moléculas encapsuladas y la reacción de sus fragmentos con el interior de la jaula del fullereno. Estas reacciones deberían dar lugar a aductos endoédricos de fullereno, que actualmente se desconocen.