
La electroforesis en gel es un método de separación y análisis de biomacromoléculas ( ADN , ARN , proteínas , etc.) y sus fragmentos, en función de su tamaño y carga. Se utiliza en química clínica para separar proteínas por carga o tamaño (agarosa IEF, esencialmente independiente del tamaño) y en bioquímica y biología molecular para separar una población mixta de fragmentos de ADN y ARN por longitud, para estimar el tamaño de fragmentos de ADN y ARN o para separar proteínas por carga. [1]
Las moléculas de ácido nucleico se separan aplicando un campo eléctrico para mover las moléculas cargadas negativamente a través de una matriz de agarosa u otras sustancias. Las moléculas más cortas se mueven más rápido y migran más lejos que las más largas porque las moléculas más cortas migran más fácilmente a través de los poros del gel. Este fenómeno se llama tamizado. [2] Las proteínas se separan mediante la carga en agarosa porque los poros del gel son demasiado grandes para tamizar las proteínas. La electroforesis en gel también se puede utilizar para la separación de nanopartículas .
La electroforesis en gel utiliza un gel como medio anticonvectivo o medio de tamizado durante la electroforesis, el movimiento de una partícula cargada en una corriente eléctrica. Los geles suprimen la convección térmica provocada por la aplicación del campo eléctrico y también pueden actuar como medio tamiz, retardando el paso de las moléculas; Los geles también pueden servir simplemente para mantener la separación finalizada de modo que se pueda aplicar una tinción posterior a la electroforesis. [3] La electroforesis en gel de ADN generalmente se realiza con fines analíticos, a menudo después de la amplificación del ADN mediante la reacción en cadena de la polimerasa (PCR), pero puede usarse como técnica preparativa antes del uso de otros métodos como la espectrometría de masas , RFLP , PCR y clonación. , secuenciación de ADN o transferencia Southern para una mayor caracterización.

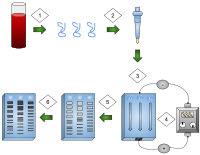
La electroforesis es un proceso que permite clasificar moléculas según su carga, tamaño o forma. Utilizando un campo eléctrico, se puede hacer que moléculas (como el ADN) se muevan a través de un gel hecho de agarosa o poliacrilamida . El campo eléctrico consta de una carga negativa en un extremo que empuja las moléculas a través del gel y una carga positiva en el otro extremo que empuja las moléculas a través del gel. Las moléculas que se clasifican se dispensan en un pocillo del material de gel. El gel se coloca en una cámara de electroforesis, que luego se conecta a una fuente de energía. Cuando se aplica el campo eléctrico, las moléculas más grandes se mueven más lentamente a través del gel mientras que las moléculas más pequeñas se mueven más rápido. Las moléculas de diferentes tamaños forman bandas distintas en el gel. [4]
El término " gel " en este caso se refiere a la matriz utilizada para contener y luego separar las moléculas diana. En la mayoría de los casos, el gel es un polímero reticulado cuya composición y porosidad se eligen en función del peso específico y la composición del objetivo a analizar. Al separar proteínas o pequeños ácidos nucleicos ( ADN , ARN u oligonucleótidos ), el gel suele estar compuesto por diferentes concentraciones de acrilamida y un reticulante , lo que produce redes de malla de poliacrilamida de diferentes tamaños. Al separar ácidos nucleicos más grandes (más de unos pocos cientos de bases ), la matriz preferida es la agarosa purificada. En ambos casos, el gel forma una matriz sólida pero porosa. La acrilamida, a diferencia de la poliacrilamida, es una neurotoxina y debe manipularse tomando las precauciones de seguridad adecuadas para evitar intoxicaciones. La agarosa se compone de largas cadenas no ramificadas de carbohidratos sin carga y sin entrecruzamientos, lo que da como resultado un gel con poros grandes que permite la separación de macromoléculas y complejos macromoleculares . [5]
La electroforesis se refiere a la fuerza electromotriz (EMF) que se utiliza para mover las moléculas a través de la matriz del gel. Al colocar las moléculas en pocillos del gel y aplicar un campo eléctrico, las moléculas se moverán a través de la matriz a diferentes velocidades, determinadas en gran medida por su masa cuando la relación carga-masa (Z) de todas las especies es uniforme. Sin embargo, cuando no todas las cargas son uniformes, el campo eléctrico generado por el procedimiento de electroforesis hará que las moléculas migren de manera diferencial según la carga. Las especies que tienen carga neta positiva migrarán hacia el cátodo que tiene carga negativa (porque se trata de una celda electrolítica en lugar de galvánica ), mientras que las especies que tienen carga neta negativa migrarán hacia el ánodo con carga positiva. La masa sigue siendo un factor en la velocidad con la que estas moléculas cargadas de manera no uniforme migran a través de la matriz hacia sus respectivos electrodos. [6]
Si se han cargado varias muestras en pocillos adyacentes del gel, correrán paralelas en carriles individuales. Dependiendo del número de moléculas diferentes, cada carril muestra la separación de los componentes de la mezcla original como una o más bandas distintas, una banda por componente. La separación incompleta de los componentes puede dar lugar a bandas superpuestas o manchas indistinguibles que representan múltiples componentes no resueltos. [ cita necesaria ] Las bandas en diferentes carriles que terminan a la misma distancia desde la parte superior contienen moléculas que pasaron a través del gel a la misma velocidad, lo que generalmente significa que son aproximadamente del mismo tamaño. Hay marcadores de tamaño de peso molecular disponibles que contienen una mezcla de moléculas de tamaños conocidos. Si dicho marcador se ejecutara en un carril del gel paralelo a las muestras desconocidas, las bandas observadas se pueden comparar con las de las muestras desconocidas para determinar su tamaño. La distancia que recorre una banda es aproximadamente inversamente proporcional al logaritmo del tamaño de la molécula (alternativamente, esto se puede afirmar que la distancia recorrida es inversamente proporcional al logaritmo del peso molecular de las muestras). [7]
Existen límites para las técnicas electroforéticas. Dado que pasar una corriente a través de un gel provoca calentamiento, los geles pueden derretirse durante la electroforesis. La electroforesis se realiza en soluciones tampón para reducir los cambios de pH debido al campo eléctrico, lo cual es importante porque la carga del ADN y el ARN depende del pH, pero funcionar durante demasiado tiempo puede agotar la capacidad tampón de la solución. También existen limitaciones a la hora de determinar el peso molecular mediante SDS-PAGE, especialmente cuando se intenta encontrar el PM de una proteína desconocida. Ciertas variables biológicas son difíciles o imposibles de minimizar y pueden afectar la migración electroforética. Dichos factores incluyen la estructura de las proteínas, las modificaciones postraduccionales y la composición de aminoácidos. Por ejemplo, la tropomiosina es una proteína ácida que migra de forma anormal en geles SDS-PAGE. Esto se debe a que los residuos ácidos son repelidos por el SDS cargado negativamente, lo que provoca una relación masa-carga y una migración inexactas. [8] Además, es posible que diferentes preparaciones de material genético no migren consistentemente entre sí, por razones morfológicas o de otro tipo.
Los tipos de gel más utilizados son los geles de agarosa y poliacrilamida. Cada tipo de gel se adapta bien a diferentes tipos y tamaños de analito. Los geles de poliacrilamida se utilizan habitualmente para proteínas y tienen un poder de resolución muy alto para pequeños fragmentos de ADN (5-500 pb). Los geles de agarosa, por otro lado, tienen un menor poder de resolución para el ADN, pero tienen un mayor rango de separación y, por lo tanto, se utilizan para fragmentos de ADN de tamaño habitual de 50 a 20 000 pb, pero la resolución de más de 6 Mb es posible con campo pulsado. electroforesis en gel (PFGE). [9] Los geles de poliacrilamida se ejecutan en una configuración vertical, mientras que los geles de agarosa generalmente se ejecutan horizontalmente en modo submarino. También difieren en su metodología de fundición, ya que la agarosa fragua térmicamente, mientras que la poliacrilamida se forma en una reacción de polimerización química.

Los geles de agarosa están hechos de polímeros de polisacáridos naturales extraídos de algas marinas . Los geles de agarosa se moldean y manipulan fácilmente en comparación con otras matrices porque el fraguado del gel es un cambio físico más que químico. Las muestras también se recuperan fácilmente. Una vez finalizado el experimento, el gel resultante se puede guardar en una bolsa de plástico en el frigorífico.
Los geles de agarosa no tienen un tamaño de poro uniforme, pero son óptimos para la electroforesis de proteínas de más de 200 kDa. [10] La electroforesis en gel de agarosa también se puede utilizar para la separación de fragmentos de ADN que van desde 50 pares de bases hasta varias megabases (millones de bases), [11] los más grandes de los cuales requieren aparatos especializados. La distancia entre bandas de ADN de diferentes longitudes está influenciada por el porcentaje de agarosa en el gel; porcentajes más altos requieren tiempos de ejecución más prolongados, a veces días. En lugar de ello, los geles de agarosa con un alto porcentaje deben procesarse con electroforesis de campo pulsado (PFE) o electroforesis de inversión de campo.
"La mayoría de los geles de agarosa se elaboran con entre un 0,7 % (buena separación o resolución de fragmentos grandes de ADN de 5 a 10 kb) y un 2 % (buena resolución para fragmentos pequeños de 0,2 a 1 kb) de agarosa disuelta en tampón de electroforesis. Se puede utilizar hasta un 3 % para separar fragmentos muy pequeños, pero un gel de poliacrilamida vertical es más apropiado en este caso. Los geles de bajo porcentaje son muy débiles y pueden romperse cuando se intenta levantarlos. Los geles de alto porcentaje suelen ser quebradizos y no se fijan uniformemente. muchas aplicaciones." [12]
La electroforesis en gel de poliacrilamida (PAGE) se utiliza para separar proteínas con tamaños de 5 a 2000 kDa debido al tamaño de poro uniforme proporcionado por el gel de poliacrilamida. El tamaño de los poros se controla modulando las concentraciones de acrilamida y bisacrilamida en polvo utilizadas para crear un gel. Se debe tener cuidado al crear este tipo de gel, ya que la acrilamida es una potente neurotoxina en sus formas líquida y en polvo.
Las técnicas tradicionales de secuenciación de ADN , como los métodos de Maxam-Gilbert o Sanger, utilizaban geles de poliacrilamida para separar fragmentos de ADN que diferían en un único par de bases de longitud para poder leer la secuencia. La mayoría de los métodos modernos de separación de ADN utilizan ahora geles de agarosa, excepto para fragmentos de ADN especialmente pequeños. Actualmente se utiliza con mayor frecuencia en el campo de la inmunología y el análisis de proteínas, y a menudo se utiliza para separar diferentes proteínas o isoformas de la misma proteína en bandas separadas. Estos se pueden transferir a una membrana de nitrocelulosa o PVDF para sondearlos con anticuerpos y marcadores correspondientes, como en una transferencia Western .
Normalmente, los geles resolutivos se elaboran al 6%, 8%, 10%, 12% o 15%. Se vierte gel de apilamiento (5%) sobre el gel de resolución y se inserta un peine de gel (que forma los pocillos y define los carriles donde se colocarán las proteínas, el tampón de muestra y las escaleras). El porcentaje elegido depende del tamaño de la proteína que se desea identificar o sondear en la muestra. Cuanto menor sea el peso conocido, mayor será el porcentaje que se debe utilizar. Los cambios en el sistema tampón del gel pueden ayudar a resolver aún más proteínas de tamaños muy pequeños. [13]
El almidón de patata parcialmente hidrolizado constituye otro medio no tóxico para la electroforesis de proteínas. Los geles son ligeramente más opacos que la acrilamida o la agarosa. Las proteínas no desnaturalizadas se pueden separar según su carga y tamaño. Se visualizan mediante tinción con negro naftal o negro amido. Las concentraciones típicas de gel de almidón son del 5% al 10%. [14] [15] [16]
Los geles desnaturalizantes se procesan en condiciones que alteran la estructura natural del analito, lo que hace que se desarrolle en una cadena lineal. Por tanto, la movilidad de cada macromolécula depende únicamente de su longitud lineal y de su relación masa-carga. Por tanto, los niveles secundario, terciario y cuaternario de la estructura biomolecular se alteran, dejando sólo la estructura primaria por analizar.
Los ácidos nucleicos a menudo se desnaturalizan incluyendo urea en el tampón, mientras que las proteínas se desnaturalizan usando dodecilsulfato de sodio , generalmente como parte del proceso SDS-PAGE . Para la desnaturalización completa de las proteínas, también es necesario reducir los enlaces disulfuro covalentes que estabilizan su estructura terciaria y cuaternaria , método llamado PAGE reductora. Las condiciones reductoras suelen mantenerse mediante la adición de beta-mercaptoetanol o ditiotreitol . Para un análisis general de muestras de proteínas, la PAGE reductora es la forma más común de electroforesis de proteínas .
Las condiciones desnaturalizantes son necesarias para una estimación adecuada del peso molecular del ARN. El ARN es capaz de formar más interacciones intramoleculares que el ADN, lo que puede provocar cambios en su movilidad electroforética . La urea , el DMSO y el glioxal son los agentes desnaturalizantes más utilizados para alterar la estructura del ARN. Originalmente, el hidróxido de metilmercurio altamente tóxico se usaba a menudo en la electroforesis desnaturalizante del ARN, [17] pero puede ser el método de elección para algunas muestras. [18]
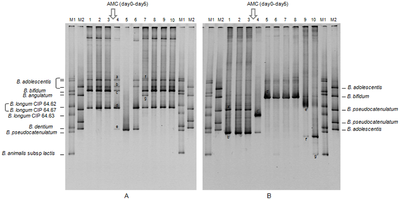
La electroforesis en gel desnaturalizante se utiliza en los métodos basados en patrones de bandas de ADN y ARN, electroforesis en gel con gradiente de temperatura (TGGE) [19] y electroforesis en gel con gradiente desnaturalizante (DGGE). [20]

Los geles nativos se procesan en condiciones no desnaturalizantes para mantener la estructura natural del analito. Esto permite que el tamaño físico del complejo plegado o ensamblado afecte la movilidad, lo que permite el análisis de los cuatro niveles de la estructura biomolecular. Para muestras biológicas, los detergentes se utilizan sólo en la medida en que sean necesarios para lisar las membranas lipídicas de la célula . Los complejos permanecen, en su mayor parte, asociados y plegados como lo estarían en la célula. Sin embargo, una desventaja es que es posible que los complejos no se separen de manera limpia o predecible, ya que es difícil predecir cómo la forma y el tamaño de la molécula afectarán su movilidad. Abordar y resolver este problema es uno de los objetivos principales de PAGE nativo preparativo .
A diferencia de los métodos desnaturalizantes, la electroforesis en gel nativo no utiliza un agente desnaturalizante cargado . Por lo tanto , las moléculas que se separan (normalmente proteínas o ácidos nucleicos ) no sólo difieren en la masa molecular y la carga intrínseca, sino también en el área de la sección transversal y, por lo tanto, experimentan diferentes fuerzas electroforéticas que dependen de la forma de la estructura general. En el caso de las proteínas, dado que permanecen en su estado nativo, pueden visualizarse no sólo mediante reactivos de tinción de proteínas generales sino también mediante tinción ligada a enzimas específicas.
Un ejemplo experimental específico de una aplicación de electroforesis en gel nativo es verificar la actividad enzimática para verificar la presencia de la enzima en la muestra durante la purificación de proteínas. Por ejemplo, para la proteína fosfatasa alcalina, la solución de tinción es una mezcla de sal de 4-cloro-2-2metilbencenodiazonio con ácido 3-fosfo-2-naftoico-2'-4'-dimetilanilina en tampón Tris. Este tinte se vende comercialmente como un kit para teñir geles. Si la proteína está presente, el mecanismo de la reacción se desarrolla en el siguiente orden: comienza con la desfosforilación del ácido 3-fosfo-2-naftoico-2'-4'-dimetilanilina por la fosfatasa alcalina (se necesita agua para la reacción). El grupo fosfato se libera y se reemplaza por un grupo alcohol del agua. El electrófilo 4-cloro-2-2 metilbencenodiazonio (sal de diazonio Fast Red TR) desplaza el grupo alcohol formando el producto final colorante rojo azoico. Como su nombre lo indica, este es el producto final de color rojo visible de la reacción. En la experimentación académica de pregrado sobre purificación de proteínas, el gel generalmente se procesa junto a muestras purificadas comerciales para visualizar los resultados y concluir si la purificación fue exitosa o no. [22]
La electroforesis en gel nativo se utiliza normalmente en proteómica y metalómica . Sin embargo, la PAGE nativa también se utiliza para escanear genes (ADN) en busca de mutaciones desconocidas, como en el polimorfismo de conformación monocatenario .
Los tampones en la electroforesis en gel se utilizan para proporcionar iones que transportan una corriente y mantener el pH a un valor relativamente constante. Estos amortiguadores contienen muchos iones, necesarios para el paso de la electricidad a través de ellos. Algo como el agua destilada o el benceno contiene pocos iones, lo que no es ideal para su uso en electroforesis. [23] Hay varios tampones que se utilizan para la electroforesis. Los más comunes son, para los ácidos nucleicos, Tris/Acetato/EDTA (TAE), Tris/Borato/EDTA (TBE). Se han propuesto muchos otros tampones, por ejemplo, borato de litio , que rara vez se utiliza, basándose en citas de Pubmed (LB), histidina isoeléctrica, tampones de productos emparejados pK, etc.; en la mayoría de los casos, el supuesto fundamento es una menor movilidad de iones combinados con corriente más baja (menos calor), lo que conduce a una vida útil más larga del buffer. El borato es problemático; El borato puede polimerizarse o interactuar con dioles cis como los que se encuentran en el ARN. TAE tiene la capacidad de amortiguación más baja pero proporciona la mejor resolución para ADN más grande. Esto significa un voltaje más bajo y más tiempo, pero un mejor producto. LB es relativamente nuevo y es ineficaz para resolver fragmentos de más de 5 kbp; Sin embargo, debido a su baja conductividad, se podría utilizar un voltaje mucho más alto (hasta 35 V/cm), lo que significa un tiempo de análisis más corto para la electroforesis de rutina. Una diferencia de tamaño tan pequeña como un par de bases podría resolverse en gel de agarosa al 3% con un medio de conductividad extremadamente baja (borato de litio 1 mM). [24]
La mayoría de las separaciones de proteínas SDS-PAGE se realizan utilizando un sistema tampón "discontinuo" (o DISC) que mejora significativamente la nitidez de las bandas dentro del gel. Durante la electroforesis en un sistema de gel discontinuo, se forma un gradiente de iones en la etapa inicial de la electroforesis que hace que todas las proteínas se concentren en una sola banda afilada en un proceso llamado isotacoforesis . La separación de las proteínas por tamaño se logra en la región inferior de "resolución" del gel. El gel de resolución suele tener un tamaño de poro mucho más pequeño, lo que conduce a un efecto de tamizado que ahora determina la movilidad electroforética de las proteínas.
Una vez completada la electroforesis, las moléculas del gel se pueden teñir para hacerlas visibles. El ADN se puede visualizar usando bromuro de etidio que, cuando se intercala en el ADN, emite fluorescencia bajo luz ultravioleta , mientras que las proteínas se pueden visualizar usando tinción de plata o tinte azul brillante de Coomassie . También se pueden utilizar otros métodos para visualizar la separación de los componentes de la mezcla en el gel. Si las moléculas a separar contienen radiactividad , por ejemplo en un gel de secuenciación de ADN , se puede registrar un autorradiograma del gel. Se pueden tomar fotografías de geles, a menudo utilizando un sistema Gel Doc . Luego, los geles suelen etiquetarse para su presentación y registros científicos en el popular sitio web de creación de figuras, SciUGo.
Después de la separación, se puede utilizar un método de separación adicional, como el enfoque isoeléctrico o SDS-PAGE . Luego se cortará físicamente el gel y se extraerán los complejos proteicos de cada porción por separado. Luego, cada extracto se puede analizar, por ejemplo mediante huellas dactilares de masa peptídica o secuenciación de péptidos de novo después de la digestión en gel . Esto puede proporcionar una gran cantidad de información sobre las identidades de las proteínas de un complejo.
La electroforesis en gel se utiliza en medicina forense , biología molecular , genética , microbiología y bioquímica . Los resultados se pueden analizar cuantitativamente visualizando el gel con luz ultravioleta y un dispositivo de imágenes de gel. La imagen se registra con una cámara operada por computadora y la intensidad de la banda o punto de interés se mide y se compara con estándares o marcadores cargados en el mismo gel. La medición y el análisis se realizan principalmente con software especializado.
Dependiendo del tipo de análisis que se realice, a menudo se implementan otras técnicas junto con los resultados de la electroforesis en gel, lo que proporciona una amplia gama de aplicaciones específicas de campo.
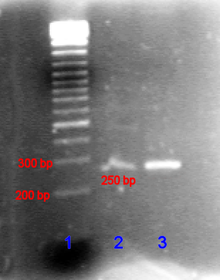
En el caso de los ácidos nucleicos, la dirección de la migración, de electrodos negativos a positivos, se debe a la carga negativa natural que lleva su columna vertebral de azúcar y fosfato . [25]
Los fragmentos de ADN de doble cadena se comportan naturalmente como varillas largas, por lo que su migración a través del gel es relativa a su tamaño o, en el caso de fragmentos cíclicos, a su radio de giro . El ADN circular, como los plásmidos , sin embargo, puede mostrar múltiples bandas; la velocidad de migración puede depender de si está relajado o superenrollado. El ADN o ARN monocatenario tiende a plegarse en moléculas con formas complejas y migrar a través del gel de una manera complicada según su estructura terciaria. Por tanto, se utilizan agentes que rompen los enlaces de hidrógeno , como el hidróxido de sodio o la formamida , para desnaturalizar los ácidos nucleicos y hacer que vuelvan a comportarse como largas varillas. [26]
La electroforesis en gel de ADN o ARN de gran tamaño generalmente se realiza mediante electroforesis en gel de agarosa. Consulte la página " método de terminación de cadena " para ver un ejemplo de gel de secuenciación de ADN de poliacrilamida. La caracterización mediante interacción de ligandos de ácidos nucleicos o fragmentos se puede realizar mediante electroforesis de afinidad por cambio de movilidad .
La electroforesis de muestras de ARN se puede utilizar para comprobar la contaminación del ADN genómico y también la degradación del ARN. El ARN de organismos eucariotas muestra bandas distintas de ARNr de 28 y 18, siendo la banda de 28 aproximadamente dos veces más intensa que la banda de 18. El ARN degradado tiene bandas menos definidas, una apariencia manchada y la relación de intensidad es inferior a 2:1.
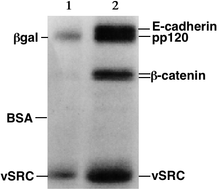
Las proteínas , a diferencia de los ácidos nucleicos, pueden tener cargas variables y formas complejas, por lo que es posible que no migren al gel de poliacrilamida a velocidades similares, o todas, cuando se coloca un EMF de negativo a positivo en la muestra. Por lo tanto, las proteínas suelen desnaturalizarse en presencia de un detergente como el dodecilsulfato de sodio (SDS) que recubre las proteínas con una carga negativa. [3] Generalmente, la cantidad de SDS unida es relativa al tamaño de la proteína (generalmente 1,4 g de SDS por gramo de proteína), de modo que las proteínas desnaturalizadas resultantes tienen una carga negativa general y todas las proteínas tienen una carga similar. relación masa. Dado que las proteínas desnaturalizadas actúan como varillas largas en lugar de tener una forma terciaria compleja, la velocidad a la que las proteínas recubiertas de SDS resultantes migran en el gel es relativa únicamente a su tamaño y no a su carga o forma. [3]
Las proteínas generalmente se analizan mediante electroforesis en gel de poliacrilamida con dodecilsulfato de sodio ( SDS-PAGE ), mediante electroforesis en gel nativo , mediante electroforesis en gel nativo preparativo ( QPNC-PAGE ) o mediante electroforesis 2-D .
La caracterización mediante interacción de ligandos se puede realizar mediante electrotransferencia o electroforesis de afinidad en agarosa o mediante electroforesis capilar para la estimación de constantes de unión y la determinación de características estructurales como el contenido de glucanos mediante la unión de lectina .
Una aplicación novedosa para la electroforesis en gel es la separación o caracterización de nanopartículas de metal u óxido metálico (por ejemplo, Au, Ag, ZnO, SiO2) con respecto al tamaño, la forma o la química de la superficie de las nanopartículas. [27] El objetivo es obtener una muestra más homogénea (por ejemplo, una distribución de tamaño de partícula más estrecha), que luego pueda utilizarse en otros productos/procesos (por ejemplo, procesos de autoensamblaje). Para la separación de nanopartículas dentro de un gel, el parámetro clave es la relación entre el tamaño de partícula y el tamaño de malla, por lo que se identificaron dos mecanismos de migración: el mecanismo no restringido, donde el tamaño de partícula << tamaño de malla, y el mecanismo restringido, donde El tamaño de las partículas es similar al tamaño de la malla. [28]
Un libro de 1959 sobre electroforesis escrito por Milan Bier cita referencias del siglo XIX. [33] Sin embargo, Oliver Smithies hizo contribuciones significativas. Bier afirma: "El método de Smithies... está encontrando una amplia aplicación debido a su poder separatorio único". Tomado en contexto, Bier implica claramente que el método de Smithies es una mejora.