En química y termodinámica , la entalpía estándar de formación o calor estándar de formación de un compuesto es el cambio de entalpía durante la formación de 1 mol de la sustancia a partir de sus elementos constituyentes en su estado de referencia , con todas las sustancias en sus estados estándar . El valor de presión estándar p ⦵ = 10 5 Pa (= 100 kPa = 1 bar ) es recomendado por la IUPAC , aunque antes de 1982 se utilizaba el valor 1,00 atm (101,325 kPa). [1] No existe una temperatura estándar. Su símbolo es Δ f H ⦵ . El superíndice Plimsoll sobre este símbolo indica que el proceso ha ocurrido en condiciones estándar a la temperatura especificada (normalmente 25 °C o 298,15 K).
Los estados estándar se definen para varios tipos de sustancias. Para un gas, es el estado hipotético que asumiría el gas si obedeciera la ecuación de los gases ideales a una presión de 1 bar. Para un soluto gaseoso o sólido presente en una solución ideal diluida , el estado estándar es el estado hipotético de concentración del soluto de exactamente un mol por litro (1 M ) a una presión de 1 bar extrapolado a partir de una dilución infinita. Para una sustancia pura o un disolvente en estado condensado (un líquido o un sólido), el estado estándar es el líquido o sólido puro bajo una presión de 1 bar.
En el caso de los elementos que tienen múltiples alótropos , el estado de referencia suele elegirse como la forma en la que el elemento es más estable bajo una presión de 1 bar. Una excepción es el fósforo , para el cual la forma más estable a 1 bar es el fósforo negro , pero se elige el fósforo blanco como el estado de referencia estándar para una entalpía de formación cero. [2]
Por ejemplo, la entalpía estándar de formación de dióxido de carbono es la entalpía de la siguiente reacción en las condiciones anteriores:
Todos los elementos se escriben en sus estados estándar y se forma un mol de producto. Esto es válido para todas las entalpías de formación.
La entalpía estándar de formación se mide en unidades de energía por cantidad de sustancia, generalmente expresada en kilojulios por mol (kJ mol −1 ), pero también en kilocalorías por mol , julios por mol o kilocalorías por gramo (cualquier combinación de estas unidades conforme a las pautas de energía por masa o cantidad).
Todos los elementos en sus estados de referencia ( oxígeno gaseoso, carbono sólido en forma de grafito , etc.) tienen una entalpía estándar de formación de cero, ya que no hay ningún cambio involucrado en su formación.
La reacción de formación es un proceso a presión y temperatura constantes. Dado que la presión de la reacción de formación estándar se fija en 1 bar, la entalpía de formación estándar o el calor de reacción es una función de la temperatura. Para fines de tabulación, las entalpías de formación estándar se dan todas a una sola temperatura: 298 K, representada por el símbolo Δ f H⦵
298 mil.
Para muchas sustancias, la reacción de formación puede considerarse como la suma de una serie de reacciones más simples, ya sean reales o ficticias. La entalpía de reacción puede entonces analizarse aplicando la Ley de Hess , que establece que la suma de los cambios de entalpía para una serie de pasos de reacción individuales es igual al cambio de entalpía de la reacción general. Esto es cierto porque la entalpía es una función de estado , cuyo valor para un proceso general depende solo de los estados inicial y final y no de ningún estado intermedio. Se dan ejemplos en las siguientes secciones.
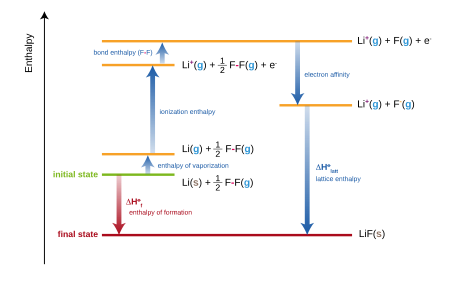
Para los compuestos iónicos, la entalpía estándar de formación es equivalente a la suma de varios términos incluidos en el ciclo de Born-Haber . Por ejemplo, la formación de fluoruro de litio ,
puede considerarse como la suma de varios pasos, cada uno con su propia entalpía (o energía, aproximadamente):
La suma de estas entalpías da la entalpía estándar de formación ( Δ f H ) del fluoruro de litio:
En la práctica, la entalpía de formación del fluoruro de litio se puede determinar experimentalmente, pero la energía reticular no se puede medir directamente. Por lo tanto, la ecuación se reordena para evaluar la energía reticular: [3]
Las reacciones de formación de la mayoría de los compuestos orgánicos son hipotéticas. Por ejemplo, el carbono y el hidrógeno no reaccionan directamente para formar metano ( CH4 ), por lo que la entalpía estándar de formación no se puede medir directamente. Sin embargo, la entalpía estándar de combustión se puede medir fácilmente utilizando calorimetría de bomba . La entalpía estándar de formación se determina luego utilizando la ley de Hess . La combustión del metano:
es equivalente a la suma de la descomposición hipotética en elementos seguida de la combustión de los elementos para formar dióxido de carbono ( CO 2 ) y agua ( H 2 O ):
Aplicando la ley de Hess,
Resolviendo el estándar de entalpía de formación,
Se determina que el valor de es −74,8 kJ/mol. El signo negativo muestra que la reacción, si tuviera lugar, sería exotérmica ; es decir, el metano es entálpicamente más estable que el gas hidrógeno y el carbono.
Es posible predecir los calores de formación para compuestos orgánicos simples no deformados con el método de aditividad del grupo de calor de formación .
El cambio de entalpía estándar de cualquier reacción se puede calcular a partir de las entalpías estándar de formación de reactivos y productos utilizando la ley de Hess. Una reacción dada se considera como la descomposición de todos los reactivos en elementos en sus estados estándar, seguida de la formación de todos los productos. El calor de reacción es entonces menos la suma de las entalpías estándar de formación de los reactivos (cada una multiplicada por su respectivo coeficiente estequiométrico, ν ) más la suma de las entalpías estándar de formación de los productos (cada una también multiplicada por su respectivo coeficiente estequiométrico), como se muestra en la siguiente ecuación: [4]
Si la entalpía estándar de los productos es menor que la entalpía estándar de los reactivos, la entalpía estándar de reacción es negativa. Esto implica que la reacción es exotérmica. Lo inverso también es cierto: la entalpía estándar de reacción es positiva para una reacción endotérmica. Este cálculo tiene un supuesto tácito de solución ideal entre reactivos y productos donde la entalpía de mezcla es cero.
Por ejemplo, para la combustión de metano, :
Sin embargo, es un elemento en su estado estándar, por lo que , y el calor de reacción se simplifica a
cual es la ecuación de la sección anterior para la entalpía de combustión .
Propiedades termoquímicas de sustancias seleccionadas a 298,15 K y 1 atm