Cas9 ( proteína 9 asociada a CRISPR , anteriormente llamada Cas5 , Csn1 o Csx12 ) es una proteína de 160 kilodaltons que desempeña un papel vital en la defensa inmunológica de ciertas bacterias contra virus de ADN y plásmidos , y se utiliza ampliamente en aplicaciones de ingeniería genética . Su función principal es cortar el ADN y así alterar el genoma de una célula. La técnica de edición del genoma CRISPR-Cas9 contribuyó de manera importante a que el Premio Nobel de Química en 2020 fuera otorgado a Emmanuelle Charpentier y Jennifer Doudna . [2]
Más técnicamente, Cas9 es una enzima endonucleasa de ADN guiada por ARN dual asociada con el sistema inmunológico adaptativo de repeticiones palindrómicas cortas agrupadas regularmente interespaciadas ( CRISPR ) en Streptococcus pyogenes . [3] [4] [5] S. pyogenes utiliza CRISPR para memorizar y Cas9 para luego interrogar y escindir ADN extraño, como el ADN de bacteriófago invasor o el ADN plasmídico. [4] [6] [7] [8] Cas9 realiza esta interrogación desenrollando ADN extraño y buscando sitios complementarios a la región espaciadora de 20 nucleótidos del ARN guía (ARNg). Si el sustrato del ADN es complementario al ARN guía, Cas9 escinde el ADN invasor. En este sentido, el mecanismo CRISPR-Cas9 tiene varios paralelos con el mecanismo de interferencia de ARN (ARNi) en eucariotas.
Además de su función original en la inmunidad bacteriana, la proteína Cas9 se ha utilizado intensamente como herramienta de ingeniería genómica para inducir roturas de doble hebra dirigidas al sitio en el ADN. Estas roturas pueden conducir a la inactivación de genes o la introducción de genes heterólogos mediante la unión de extremos no homólogos y la recombinación homóloga, respectivamente, en muchos organismos modelo de laboratorio. La investigación sobre el desarrollo de diversas variantes de cas9 ha sido una forma prometedora de superar la limitación de la edición del genoma CRISPR-Cas9 . Algunos ejemplos incluyen Cas9 nickasa (Cas9n), una variante que induce roturas monocatenarias (SSB) o variantes que reconocen diferentes secuencias de PAM . [9] Junto con las nucleasas de dedos de zinc y las proteínas nucleasas efectoras similares a activadoras de la transcripción (TALEN), Cas9 se está convirtiendo en una herramienta destacada en el campo de la edición del genoma.
Cas9 ha ganado terreno en los últimos años porque puede escindir casi cualquier secuencia complementaria al ARN guía. [4] Debido a que la especificidad objetivo de Cas9 proviene de la complementariedad del ARN guía:ADN y no de modificaciones a la proteína en sí (como los TALEN y los dedos de zinc ), diseñar Cas9 para apuntar a ADN nuevo es sencillo. [10] Las versiones de Cas9 que se unen pero no escinden el ADN afín se pueden usar para localizar activadores o represores transcripcionales en secuencias de ADN específicas para controlar la activación y represión transcripcional. [11] [12] El Cas9 nativo requiere un ARN guía compuesto por dos ARN dispares que se asocian: el ARN CRISPR (ARNcr) y el ARNcr transactivador ( ARNtracr ). [3] La focalización de Cas9 se ha simplificado mediante la ingeniería de un ARN guía único quimérico (ARNchi). Los científicos han sugerido que los impulsores genéticos basados en Cas9 pueden ser capaces de editar los genomas de poblaciones enteras de organismos. [13] En 2015, Cas9 se utilizó para modificar el genoma de embriones humanos por primera vez. [14]
Para sobrevivir en una variedad de hábitats desafiantes e inhóspitos que están llenos de bacteriófagos , bacterias y arqueas, se han desarrollado métodos para evadir y defenderse de los virus depredadores . Esto incluye el sistema CRISPR de inmunidad adaptativa. En la práctica, los sistemas CRISPR/Cas actúan como enzimas de restricción autoprogramables. Los loci CRISPR se componen de repeticiones palindrómicas cortas que ocurren a intervalos regulares compuestos por repeticiones CRISPR alternativas y espaciadores CRISPR variables de entre 24 y 48 nucleótidos de largo. Estos loci CRISPR suelen ir acompañados de genes adyacentes asociados a CRISPR (cas). En 2005, tres grupos separados descubrieron que las regiones espaciadoras eran homólogas a elementos extraños del ADN, incluidos plásmidos y virus. Estos informes proporcionaron la primera evidencia biológica de que CRISPR podría funcionar como un sistema inmunológico.
Cas9 se ha utilizado a menudo como herramienta de edición del genoma. Cas9 se ha utilizado en desarrollos recientes para evitar que los virus manipulen el ADN del huésped. Dado que CRISPR-Cas9 se desarrolló a partir de sistemas de genoma bacteriano, se puede utilizar para atacar el material genético de los virus. El uso de la enzima Cas9 puede ser una solución para muchas infecciones virales. Cas9 posee la capacidad de atacar virus específicos al apuntar a hebras específicas de la información genética viral. Más específicamente, la enzima Cas9 se dirige a determinadas secciones del genoma viral que impiden que el virus lleve a cabo su función normal. [15] Cas9 también se ha utilizado para alterar la cadena perjudicial de ADN y ARN que causa enfermedades y cadenas de ADN mutadas. Cas9 ya se ha mostrado prometedor a la hora de interrumpir los efectos del VIH-1. Se ha demostrado que Cas9 suprime la expresión de las repeticiones terminales largas en el VIH-1. Cuando se introdujo en el genoma del VIH-1, Cas9 demostró la capacidad de mutar hebras del VIH-1. [16] [17] Cas9 también se ha utilizado en el tratamiento de la hepatitis B dirigiéndose a los extremos de ciertas repeticiones terminales largas en el genoma viral de la hepatitis B. [18] Cas9 se ha utilizado para reparar las mutaciones que causan cataratas en ratones.
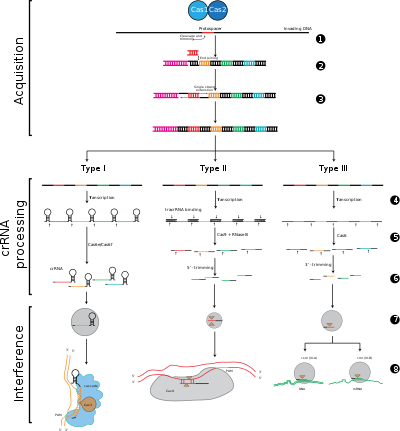
Los sistemas CRISPR-Cas se dividen en tres tipos principales (tipo I, tipo II y tipo III) y doce subtipos, que se basan en su contenido genético y diferencias estructurales. Sin embargo, las características principales que definen todos los sistemas CRISPR-Cas son los genes cas y sus proteínas: cas1 y cas2 son universales en todos los tipos y subtipos, mientras que cas3 , cas9 y cas10 son genes característicos del tipo I, tipo II y tipo III. , respectivamente.
La adaptación implica el reconocimiento y la integración de espaciadores entre dos repeticiones adyacentes en el locus CRISPR. El "Protospacer" se refiere a la secuencia del genoma viral que corresponde al espaciador. Existe un tramo corto de nucleótidos conservados proximal al protoespaciador, que se denomina motivo adyacente al protoespaciador (PAM). El PAM es un motivo de reconocimiento que se utiliza para adquirir el fragmento de ADN. [8] En el tipo II, Cas9 reconoce el PAM durante la adaptación para garantizar la adquisición de espaciadores funcionales. [6]
Aranaz et al. también han observado pérdida de espaciadores e incluso grupos de varios. 2004 y Pourcel et al. 2007. Esto probablemente ocurre mediante la recombinación homóloga del material entre repeticiones. [19]
La expresión CRISPR incluye la transcripción de una transcripción primaria llamada ARN CRISPR (pre-ARNcr), que se transcribe desde el locus CRISPR mediante la ARN polimerasa. Luego, las endoribonucleasas específicas escinden los pre-ARNcr en pequeños ARN CRISPR (ARNcr). [20]
La interferencia involucra a los crRNA dentro de un complejo multiproteico llamado CASCADE, que puede reconocer y emparejar específicamente bases con regiones de inserción de ADN extraño complementario. Luego se escinde el complejo crRNA-ácido nucleico extraño; sin embargo, si hay discrepancias entre el espaciador y el ADN diana, o si hay mutaciones en el PAM, entonces no se iniciará la escisión. En el último escenario, el ADN extraño no es el objetivo del ataque de la célula, por lo que la replicación del virus continúa y el huésped no es inmune a la infección viral. La etapa de interferencia puede ser mecánica y temporalmente distinta de la adquisición y expresión de CRISPR, pero para que funcione completamente como sistema de defensa, las tres fases deben ser funcionales. [21]
Etapa 1: integración del espaciador CRISPR. Los protoespaciadores y los motivos asociados a protoespaciadores (que se muestran en rojo) se adquieren en el extremo "líder" de una matriz CRISPR en el ADN del huésped. La matriz CRISPR está compuesta de secuencias espaciadoras (que se muestran en cuadros de colores) flanqueadas por repeticiones (diamantes negros). Este proceso requiere Cas1 y Cas2 (y Cas9 en el tipo II [6] ), que están codificados en el locus cas, que generalmente se encuentran cerca de la matriz CRISPR.
Etapa 2: expresión CRISPR. El pre-crRNA se transcribe comenzando en la región líder por la ARN polimerasa del huésped y luego las proteínas Cas lo escinden en crRNA más pequeños que contienen un único espaciador y una repetición parcial (que se muestra como una estructura en horquilla con espaciadores de colores).
Etapa 3: interferencia CRISPR. El crRNA con un espaciador que tiene una fuerte complementariedad con el ADN extraño entrante comienza un evento de escisión (representado con tijeras), que requiere proteínas Cas. La escisión del ADN interfiere con la replicación viral y proporciona inmunidad al huésped. La etapa de interferencia puede ser funcional y temporalmente distinta de la adquisición y expresión de CRISPR (representada por una línea blanca que divide la célula).
dCas9 , también conocido como Cas9 deficiente en endonucleasa, se puede utilizar para editar la expresión génica cuando se aplica al sitio de unión de la transcripción de la sección deseada de un gen. La función óptima de dCas9 se atribuye a su modo de acción. La expresión genética se inhibe cuando ya no se agregan nucleótidos a la cadena de ARN y, por lo tanto, se termina el alargamiento de esa cadena y, como resultado, afecta el proceso de transcripción. Este proceso ocurre cuando dCas9 se produce en masa, por lo que puede afectar la mayoría de los genes en un momento dado a través de una molécula de ARN guía de secuencia específica. Dado que dCas9 parece regular negativamente la expresión genética, esta acción se amplifica aún más cuando se usa junto con dominios modificadores de cromatina represivos. [22] La proteína dCas9 tiene otras funciones fuera de la regulación de la expresión genética. Se puede agregar un promotor a la proteína dCas9 que les permita trabajar entre sí para volverse eficientes al iniciar o detener la transcripción en diferentes secuencias a lo largo de una cadena de ADN. Estas dos proteínas son específicas en cuanto a dónde actúan sobre un gen. Esto prevalece en ciertos tipos de procariotas cuando un promotor y dCas9 se alinean para impedir la capacidad de elongación del polímero de nucleótidos que se unen para formar una pieza de ADN transcrita. Sin el promotor, la proteína dCas9 no tiene el mismo efecto por sí sola o con un cuerpo genético. [23]
Al examinar más a fondo los efectos de la represión de la transcripción, H3K27, un aminoácido componente de una histona, se metila mediante la interacción de dCas9 y un péptido llamado FOG1. Esencialmente, esta interacción provoca la represión genética en la sección terminal C + N del complejo de aminoácidos en la unión específica del gen y, como resultado, finaliza la transcripción. [24]
dCas9 también demuestra ser eficaz a la hora de alterar determinadas proteínas que pueden provocar enfermedades. Cuando el dCas9 se une a una forma de ARN llamada ARN guía, previene la proliferación de codones repetidos y secuencias de ADN que podrían ser perjudiciales para el genoma de un organismo. Esencialmente, cuando se producen múltiples codones repetidos, se provoca una respuesta o se recluta una gran cantidad de dCas9 para combatir la sobreproducción de esos codones y se produce la interrupción de la transcripción. dCas9 funciona sinérgicamente con gRNA y afecta directamente a la ADN polimerasa II para que no continúe la transcripción.
Se puede encontrar una explicación más detallada de cómo funciona la proteína dCas9 en su utilización de genomas de plantas mediante la regulación de la producción de genes en las plantas para aumentar o disminuir ciertas características. El sistema CRISPR-CAS9 tiene la capacidad de regular hacia arriba o hacia abajo genes. Las proteínas dCas9 son un componente del sistema CRISPR-CAS9 y estas proteínas pueden reprimir ciertas áreas de un gen vegetal. Esto sucede cuando dCAS9 se une a dominios represores y, en el caso de las plantas, se produce la desactivación de un gen regulador como AtCSTF64. [25]
Las bacterias también son otro foco del uso de proteínas dCas9. Dado que los eucariotas tienen una composición de ADN y un genoma más grandes; las bacterias mucho más pequeñas son fáciles de manipular. Como resultado, los eucariotas utilizan dCas9 para inhibir que la ARN polimerasa continúe con el proceso de transcripción del material genético. [26]

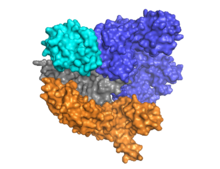
Cas9 presenta una arquitectura bilobulada con el ARN guía ubicado entre el lóbulo alfa-helicoidal (azul) y el lóbulo de la nucleasa (cian, naranja y gris). Estos dos lóbulos están conectados a través de un único puente de hélice. Hay dos dominios de nucleasa ubicados en el lóbulo de nucleasa de múltiples dominios, el RuvC (gris) que escinde la cadena de ADN no objetivo y el dominio de nucleasa HNH (cian) que escinde la cadena de ADN objetivo. El dominio RuvC está codificado por sitios secuencialmente dispares que interactúan en la estructura terciaria para formar el dominio de escisión de RuvC (consulte la figura de la derecha).
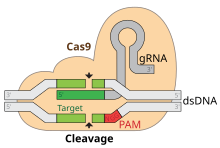
Una característica clave del ADN objetivo es que debe contener un motivo adyacente protoespaciador (PAM) que consta de la secuencia de tres nucleótidos: NGG. Este PAM es reconocido por el dominio que interactúa con PAM (dominio PI, naranja) ubicado cerca del extremo C-terminal de Cas9. Cas9 sufre distintos cambios conformacionales entre los estados apo, guía de ARN unido y guía de ARN: ADN unido.
Cas9 reconoce la arquitectura vástago-bucle inherente al locus CRISPR, que media en la maduración del complejo de ribonucleoproteína crRNA-tracrRNA . [28] Cas9 en complejo con ARN CRISPR (ARNcr) y ARNcr transactivador (ARNtracr) reconoce y degrada aún más el ADNbc objetivo. [29] En la estructura cocristalina que se muestra aquí, el complejo crRNA-tracrRNA se reemplaza por un ARN quimérico de guía única (sgRNA, en rojo) que se ha demostrado que tiene la misma función que el complejo de ARN natural. [4] La base de sgRNA emparejada con el ssDNA objetivo está anclada por Cas9 como una arquitectura en forma de T. Esta estructura cristalina de la enzima Cas9 unida al ADN revela distintos cambios conformacionales en el lóbulo alfa-helicoidal con respecto al lóbulo de la nucleasa, así como la ubicación del dominio HNH. La proteína consta de un lóbulo de reconocimiento (REC) y un lóbulo de nucleasa (NUC). Todas las regiones, excepto HNH, forman estrechas interacciones entre sí y con el complejo sgRNA-ssDNA, mientras que el dominio HNH forma pocos contactos con el resto de la proteína. En otra conformación del complejo Cas9 observada en el cristal, el dominio HNH no es visible. Estas estructuras sugieren la flexibilidad conformacional del dominio HNH.
Hasta la fecha, se han estudiado y publicado al menos tres estructuras cristalinas. Uno que representa una conformación de Cas9 en el estado apo, [27] y dos que representan Cas9 en el estado unido al ADN. [30] [1]
En el complejo sgRNA-Cas9, según la estructura cristalina, los dominios REC1, BH y PI tienen contactos importantes con la columna vertebral o bases tanto en la región repetida como en la espaciadora. [1] [30] Se han probado varios mutantes de Cas9, incluida la eliminación de los dominios REC1 o REC2 y las mutaciones de residuos en BH. Los mutantes relacionados con REC1 y BH muestran actividad menor o nula en comparación con el tipo salvaje, lo que indica que estos dos dominios son cruciales para el reconocimiento de sgRNA en la secuencia repetida y la estabilización de todo el complejo. Aunque las interacciones entre la secuencia espaciadora y Cas9, así como el dominio PI y la región repetida necesitan más estudios, el cocristal demuestra una interfaz clara entre Cas9 y sgRNA.

Análisis de secuencia y estudios bioquímicos anteriores han postulado que Cas9 contiene dos dominios de nucleasa: un dominio de nucleasa HNH similar a McrA y un dominio de nucleasa similar a RuvC. [31] Estos dominios de nucleasa tipo HNH y RuvC son responsables de la escisión de las cadenas de ADN complementaria/objetivo y no complementaria/no objetivo, respectivamente. [4] A pesar de la baja similitud de secuencia, la secuencia similar a la RNasa H tiene un pliegue RuvC (un miembro de la familia RNase H) y la región HNH se pliega como T4 Endo VII (un miembro de la familia de endonucleasas HNH). [ cita necesaria ]
S. pyogenes Cas9 de tipo salvaje requiere cofactores de magnesio (Mg 2+ ) para la escisión del ADN mediada por ARN; sin embargo, se ha demostrado que Cas9 exhibe niveles variables de actividad en presencia de otros iones metálicos divalentes . [4] Por ejemplo, se ha demostrado que Cas9 en presencia de manganeso (Mn 2+ ) es capaz de escindir el ADN de forma independiente del ARN. [32] La cinética de la escisión del ADN por Cas9 ha sido de gran interés para la comunidad científica, ya que estos datos proporcionan información sobre las complejidades de la reacción. Si bien se ha demostrado que la escisión del ADN por Cas9 unido al ARN es relativamente rápida ( k ≥ 700 s −1 ), la liberación de los productos de la escisión es muy lenta ( t 1/2 = ln(2)/ k ≈ 43– 91 h), esencialmente convirtiendo a Cas9 en una enzima de recambio único . [33] Estudios adicionales sobre la cinética de Cas9 han demostrado que el Cas9 diseñado es eficaz para reducir los efectos fuera del objetivo al modificar la velocidad de la reacción. [34] [35]
La eficacia de escisión de Cas9 depende de numerosos factores. Un requisito clave es la presencia de una PAM válida en los 3 nucleótidos de la cadena no objetivo aguas abajo del sitio de escisión. [36] La secuencia PAM canónica para S. Pyogenes Cas9 es NGG, pero se toleran motivos alternativos con menor actividad de escisión. Los motivos PAM alternativos más eficientes para S. Pyogenes Cas9 de tipo salvaje son NAG y NGA. [37] [38] La composición de la secuencia en el sitio del ADN objetivo complementario a la región espaciadora de 20 nucletodos del ARNg también afecta la eficiencia de la escisión. Las propiedades de composición de nucleótidos más relevantes que impactan la eficiencia son aquellas en la región proximal de PAM. [39] [40] [38] Los cambios de energía libre de los ácidos nucleicos también son muy relevantes para definir la actividad de escisión. [41] Los ARN guía que se unen al ADN formando un dúplex que cae en un rango restringido de cambios de energía libre de unión que excluye las uniones extremadamente débiles o estables generalmente funcionan de manera eficiente. [38] Las conformaciones de plegamiento del ARN guía estable también pueden afectar la escisión. [42]
La mayoría de las arqueas y bacterias se niegan obstinadamente a permitir que Cas9 edite su genoma. Esto se debe a que pueden incorporar ADN extraño, que no les afecta, a su genoma. Otra forma en que estas células desafían a Cas9 es mediante el proceso del sistema de modificación de restricción (RM). Cuando un bacteriófago ingresa a una bacteria o arquea, es atacado por el sistema RM. Luego, el sistema RM corta el ADN de los bacteriófagos en pedazos separados mediante enzimas de restricción y utiliza endonucleasas para destruir aún más las hebras de ADN. Esto plantea un problema para la edición de Cas9 porque el sistema RM también se dirige a los genes extraños agregados por el proceso Cas9. [43]
Debido a la capacidad única de Cas9 para unirse prácticamente a cualquier secuencia del complemento en cualquier genoma , los investigadores querían utilizar esta enzima para reprimir la transcripción de varios loci genómicos . Para lograr esto, los dos residuos catalíticos cruciales del dominio RuvC y HNH se pueden mutar a alanina , aboliendo toda la actividad endonucleasa de Cas9. La proteína resultante, denominada Cas9 "muerta" o "dCas9" para abreviar, todavía puede unirse firmemente al ADNbc. Esta variante de Cas9 catalíticamente inactiva se ha utilizado tanto para estudios mecanicistas sobre la unión interrogativa del ADN de Cas9 como como un complejo general de proteína y ARN de unión al ADN programable.
La interacción de dCas9 con el dsDNA objetivo es tan estrecha que el desnaturalizante de la proteína de urea de alta molaridad no puede disociar completamente el complejo dCas9 ARN-proteína del dsDNA objetivo. [44] dCas9 se ha dirigido con ARN guía únicos diseñados a sitios de inicio de la transcripción de cualquier loci donde dCas9 pueda competir con la ARN polimerasa en los promotores para detener la transcripción. [45] Además, dCas9 puede dirigirse a la región codificante de los loci de modo que la inhibición de la ARN polimerasa se produzca durante la fase de elongación de la transcripción. [45] En eucariotas, el silenciamiento de la expresión génica se puede ampliar dirigiendo dCas9 a secuencias potenciadoras, donde dCas9 puede bloquear el ensamblaje de factores de transcripción que conducen al silenciamiento de la expresión génica específica. [12] Además, los ARN guía proporcionados a dCas9 pueden diseñarse para incluir desajustes específicos con su secuencia afín complementaria que debilitarán cuantitativamente la interacción de dCas9 con su secuencia afín programada, lo que permitirá a un investigador ajustar el grado de silenciamiento génico aplicado a un gen. de interés. [45] Esta tecnología es similar en principio a la ARNi , de modo que la expresión genética se modula a nivel de ARN. Sin embargo, el enfoque dCas9 ha ganado mucha fuerza ya que existen menos efectos fuera del objetivo y, en general, efectos de silenciamiento más grandes y reproducibles mediante el uso de dCas9 en comparación con las pantallas de ARNi. [46] Además, debido a que el enfoque dCas9 para el silenciamiento de genes se puede controlar cuantitativamente, un investigador ahora puede controlar con precisión el grado en que se reprime un gen de interés, lo que permite responder más preguntas sobre la regulación genética y la estequiometría genética.
Más allá de la unión directa de dCas9 a posiciones de loci transcripcionalmente sensibles, dCas9 se puede fusionar con una variedad de dominios de proteínas moduladoras para llevar a cabo una gran variedad de funciones. Recientemente, dCas9 se ha fusionado con proteínas remodeladoras de la cromatina (HDAC/HAT) para reorganizar la estructura de la cromatina alrededor de varios loci. [45] Esto es importante para apuntar a varios genes eucariotas de interés, ya que las estructuras de heterocromatina dificultan la unión de Cas9. Además, debido a que Cas9 puede reaccionar con la heterocromatina , se teoriza que esta enzima se puede aplicar más al estudio de la estructura de la cromatina de varios loci. [45] Además, dCas9 se ha empleado en exámenes de represión genética en todo el genoma. Mediante el empleo de grandes bibliotecas de ARN guía capaces de apuntar a miles de genes, se han realizado análisis genéticos de todo el genoma utilizando dCas9. [47]
Otro método para silenciar la transcripción con Cas9 es escindir directamente los productos de ARNm con la enzima Cas9 catalíticamente activa. [48] Este enfoque es posible mediante la hibridación de ssDNA con una secuencia de complemento PAM a ssRNA, lo que permite un sitio PAM de dsDNA-RNA para la unión de Cas9. Esta tecnología pone a disposición la capacidad de aislar transcripciones de ARN endógeno en células sin la necesidad de inducir modificaciones químicas en el ARN o en los métodos de etiquetado de ARN.
A diferencia de los genes silenciadores, dCas9 también se puede utilizar para activar genes cuando se fusionan con factores activadores de la transcripción. [45] Estos factores incluyen subunidades de la ARN polimerasa II bacteriana y factores de transcripción tradicionales en eucariotas. Recientemente, también se han realizado exámenes de activación de la transcripción en todo el genoma utilizando fusiones de dCas9 denominadas 'CRISPRa' para la activación. [47]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )