El 11-desoxicortisol , también conocido como cortodoxona ( DCI ), cortexolona [1] [2] [3] [4] así como 17α,21-dihidroxiprogesterona o 17α,21-dihidroxipregn-4-eno-3,20-diona , [5] es una hormona esteroide glucocorticoide endógena y un intermediario metabólico hacia el cortisol . Fue descrito por primera vez por Tadeusz Reichstein en 1938 como Sustancia S, [6] por lo que también se lo ha denominado Sustancia S de Reichstein [5] o Compuesto S. [ 7] [8]
El 11-desoxicortisol actúa como un glucocorticoide , aunque es menos potente que el cortisol . [10]
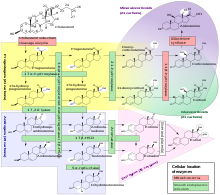
El 11-desoxicortisol se sintetiza a partir de 17α-hidroxiprogesterona por la 21-hidroxilasa y se convierte en cortisol por la 11β-hidroxilasa .
El 11-desoxicortisol en mamíferos tiene una actividad biológica limitada y actúa principalmente como intermediario metabólico dentro de la vía de los glucocorticoides , dando lugar al cortisol . [11] Sin embargo, en las lampreas marinas , una especie temprana de pez sin mandíbula que se originó hace más de 500 millones de años, el 11-desoxicortisol juega un papel crucial como la hormona glucocorticoide primaria y última con propiedades mineralocorticoides; el 11-desoxicortisol también participa, al unirse a receptores de corticosteroides específicos, en la osmorregulación intestinal en la lamprea marina en la metamorfosis , durante la cual desarrollan tolerancia al agua de mar antes de la migración río abajo. [12] Las lampreas marinas no poseen la enzima 11β-hidroxilasa ( CYP11B1 ) responsable de convertir el 11-desoxicortisol en cortisol y la 11-desoxicorticosterona en corticosterona , como se observa en los mamíferos. La ausencia de esta enzima en las lampreas marinas indica la existencia de una vía de señalización de corticosteroides compleja y altamente específica que surgió hace al menos 500 millones de años con la llegada de los primeros vertebrados. La falta de cortisol y corticosterona en las lampreas marinas sugiere que la presencia de la enzima 11β-hidroxilasa puede haber estado ausente durante las primeras etapas de la evolución de los vertebrados. [13] La ausencia de cortisol y corticosterona en las lampreas marinas sugiere que la enzima 11β-hidroxilasa puede no haber estado presente en las primeras etapas de la evolución de los vertebrados. [14]
El 11-desoxicortisol en los mamíferos tiene una actividad glucocorticoide limitada, pero es el precursor directo del principal glucocorticoide mamífero, el cortisol. [15] Como resultado, el nivel de 11-desoxicortisol se mide para diagnosticar una síntesis alterada de cortisol, para descubrir la deficiencia enzimática que causa el deterioro a lo largo de la vía hacia el cortisol y para diferenciar los trastornos suprarrenales. [16]
En la deficiencia de 11β-hidroxilasa , los niveles de 11-desoxicortisol y 11-desoxicorticosterona aumentan, y el exceso de 11-desoxicorticosterona conduce a hipertensión basada en mineralocorticoides [17] (a diferencia de la deficiencia de 21-hidroxilasa , en la que los pacientes tienen presión arterial baja por falta de mineralocorticoides ). Los niveles bajos de cortisol pueden afectar la presión arterial al causar una disminución en la retención de sodio y la expansión del volumen. Esto se debe a que el cortisol juega un papel en la regulación del equilibrio de agua y electrolitos en el cuerpo. Cuando los niveles de cortisol son bajos, hay menos reabsorción de sodio por los riñones, lo que lleva a una mayor excreción de sodio a través de la orina. Esto en última instancia reduce el volumen sanguíneo y baja la presión arterial. Por otro lado, los niveles altos de cortisol también pueden afectar la presión arterial al causar un aumento en la retención de sodio y la expansión del volumen. La hipertensión inducida por cortisol se acompaña de una retención significativa de sodio, lo que lleva a un aumento en el volumen de líquido extracelular y sodio intercambiable. Esto produce un aumento del volumen sanguíneo y, posteriormente, aumenta la presión arterial. Los mecanismos subyacentes de estos efectos implican varios factores, como la supresión del sistema de óxido nítrico, alteraciones en la respuesta vascular a los agonistas presores como la adrenalina, aumento del gasto cardíaco o del volumen sistólico debido a la expansión del volumen plasmático y posible desregulación de los receptores de glucocorticoides o de la actividad de la enzima 11β-hidroxilasa . Es importante señalar que estos mecanismos pueden ser relevantes no solo para la hipertensión inducida por cortisol, sino también para afecciones como el síndrome de Cushing (producción excesiva de cortisol), el exceso aparente de mineralocorticoides (relacionado con defectos en las enzimas 11β-hidroxilasa ), el abuso de regaliz ( ácido glicirretínico que afecta al receptor de ácido glicirretínico), [18] insuficiencia renal crónica (vida media prolongada del cortisol debido a la actividad reducida de la 11β-hidroxilasa ) e incluso la hipertensión esencial, donde puede haber anomalías con la actividad de la 11β-hidroxilasa o variaciones del receptor de glucocorticoides. [19] [20] [21] Los niveles bajos de cortisol conducen a una reducción del tono vascular.El cortisol ayuda a mantener el tono vascular normal al promover la vasoconstricción. Los niveles bajos de cortisol pueden conducir a una disminución de la vasoconstricción, lo que resulta en vasos sanguíneos relajados y una presión arterial general más baja. Además, los niveles bajos de cortisol conducen a un equilibrio hídrico deteriorado, ya que el cortisol afecta el equilibrio hídrico al influir en la reabsorción de sodio y agua en los riñones. Cuando los niveles de cortisol son bajos, la absorción de sodio puede reducirse, lo que lleva a una mayor excreción de sodio en la orina y la posterior disminución del volumen sanguíneo y la presión arterial. Además, los niveles bajos de cortisol causan un sistema renina-angiotensina desregulado, ya que el cortisol interactúa con el sistema renina-angiotensina, que regula la presión arterial a través de la vasoconstricción y el equilibrio hídrico. Los niveles bajos de cortisol pueden alterar este sistema, lo que lleva a una producción alterada de angiotensina, una secreción reducida de aldosterona y, posteriormente, una presión arterial más baja. Por el contrario, los niveles altos de cortisol conducen a un tono vascular aumentado, una mayor retención de sodio y un aumento de la actividad simpática. La liberación inducida por el estrés de glucocorticoides de alto nivel, como el cortisol, activa el sistema nervioso simpático (SNS). El SNS controla la frecuencia cardíaca, el gasto cardíaco y el tono vasomotor, lo que provoca constricción y, por lo tanto, aumenta la resistencia arterial periférica, lo que da como resultado un aumento de la presión arterial. [22] En la deficiencia de 11β-hidroxilasa , el 11-desoxicortisol también puede convertirse en androstenediona en una vía que podría explicar el aumento de los niveles de androstenediona en esta afección. [23]
En la deficiencia de 21-hidroxilasa , los niveles de 11-desoxicortisol son bajos. [24]
En 1934, el bioquímico Tadeus Reichstein , que trabajaba en Suiza , comenzó a investigar extractos de glándulas suprarrenales animales con el fin de aislar compuestos fisiológicamente activos . [25] Fue publicando los resultados de sus hallazgos a lo largo del camino. En 1944, ya había aislado y dilucidado la estructura química de 29 sustancias puras. [26] Estaba asignando nombres que consistían en la palabra "Sustancia" y una letra del alfabeto latino a las sustancias recién encontradas. En 1938, publicó un artículo sobre la "Sustancia R" y la "Sustancia S" describiendo sus estructuras químicas y propiedades. [6] La Sustancia S desde aproximadamente 1955 se conoció como 11-Desoxicortisol. [27]
En 1949, el químico investigador estadounidense Percy Lavon Julian , al buscar formas de producir cortisona , anunció la síntesis del compuesto S, a partir de la pregnenolona barata y fácilmente disponible (sintetizada a partir del esterol del aceite de soja estigmasterol ). [28] [29]
El 5 de abril de 1952, el bioquímico Durey Peterson y el microbiólogo Herbert Murray en Upjohn publicaron el primer informe de un proceso de fermentación innovador para la 11α-oxigenación microbiana de esteroides (por ejemplo, progesterona ) en un solo paso por mohos comunes del orden Mucorales . [30] La 11α-oxigenación del Compuesto S produce 11α-hidrocortisona, que puede oxidarse químicamente a cortisona o convertirse mediante pasos químicos adicionales en 11β-hidrocortisona ( cortisol ).
El nuevo método del Dr. Julian para sintetizar el compuesto antiartritis, la cortisona, es menos costoso que los métodos actuales, porque elimina la necesidad de utilizar tetróxido de osmio, una sustancia química rara y cara, declaró la compañía Glidden... Pero ni él ni la compañía Glidden quisieron revelar si el Dr. Julian también ha sintetizado cortisona a partir de soja.
Cita: Percy L. Julian, director de investigación de la división de productos de soja de Glidden Co., Chicago, ha anunciado una nueva síntesis de cortisona que elimina la necesidad del costoso tetróxido de osmio y la síntesis de otros tres compuestos relacionados con la cortisona que podrían ser útiles en el tratamiento de la artritis. No se ha hecho ninguna declaración sobre los detalles de la nueva síntesis, pero se ha revelado que no se trata de productos de soja... los tres [otros compuestos] se elaboran a partir de esteroles de soja.