
Los colorantes azoicos son compuestos orgánicos que llevan el grupo funcional R−N=N−R′, en el que R y R′ son normalmente grupos arilo y arilo sustituido. Son una familia de compuestos azoicos de importancia comercial , es decir, compuestos que contienen el enlace CN=NC. [1] Los colorantes azoicos son colorantes sintéticos y no se producen de forma natural. [2] [3] La mayoría de los colorantes azoicos contienen sólo un grupo azoico, pero hay algunos que contienen dos o tres grupos azoicos, denominados "colorantes diazoicos" y "colorantes triazoicos", respectivamente. Los colorantes azoicos comprenden el 60-70% de todos los colorantes utilizados en las industrias alimentaria y textil . [3] Los colorantes azoicos se utilizan ampliamente para tratar textiles , artículos de cuero y algunos alimentos. Los derivados químicamente relacionados de los colorantes azoicos incluyen los pigmentos azoicos, que son insolubles en agua y otros disolventes. [4] [5]
Se conocen muchos tipos de colorantes azoicos y existen varios sistemas de clasificación. Algunas clases incluyen colorantes dispersos, colorantes de complejos metálicos , colorantes reactivos y colorantes sustantivos . También llamados colorantes directos, los colorantes sustantivos se emplean para textiles a base de celulosa, que incluyen el algodón. Los colorantes se unen al tejido mediante fuerzas no electrostáticas. En otra clasificación, los colorantes azoicos se pueden clasificar según el número de grupos azo.

Como consecuencia de la deslocalización π , los compuestos arilo azo tienen colores vivos, especialmente rojos, naranjas y amarillos. Un ejemplo es el naranja disperso 1. Algunos compuestos azo, por ejemplo, el naranja de metilo , se utilizan como indicadores ácido-base . La mayoría de los discos DVD-R / +R y algunos CD-R utilizan colorante azo azul como capa de grabación.

Los colorantes azoicos son sólidos. La mayoría son sales, y el componente coloreado suele ser el anión, aunque se conocen algunos colorantes azoicos catiónicos. El carácter aniónico de la mayoría de los colorantes surge de la presencia de 1-3 grupos de ácido sulfónico, que están completamente ionizados al pH del artículo teñido:
La mayoría de las proteínas son catiónicas, por lo que el teñido del cuero y la lana corresponde a una reacción de intercambio iónico . El colorante aniónico se adhiere a estos artículos mediante fuerzas electrostáticas. Los colorantes azoicos catiónicos suelen contener centros de amonio cuaternario .
La mayoría de los colorantes azoicos se preparan mediante acoplamiento azoico , que implica una reacción de sustitución electrofílica de un catión de aril diazonio con otro compuesto, el socio de acoplamiento. Generalmente, los socios de acoplamiento son otros compuestos aromáticos con grupos donadores de electrones: [7]
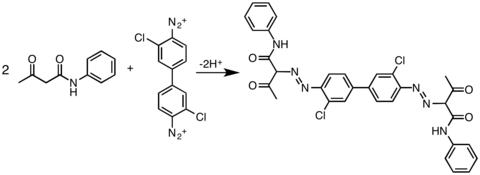
En la práctica, las amidas acetoacéticas se utilizan ampliamente como socios de acoplamiento:
Los colorantes azoicos también se preparan mediante la condensación de compuestos aromáticos nitrados con anilinas seguida de la reducción del intermedio azoxi resultante :
Para el teñido de textiles, un compañero de acoplamiento nitro típico sería el 4,4′-dinitrostilbeno-2,2′-disulfonato disódico . Los compañeros de anilina típicos se muestran a continuación. Dado que las anilinas se preparan a partir de compuestos nitro, algunos colorantes azoicos se producen por reducción parcial de compuestos nitro aromáticos. [5]
Muchos colorantes azoicos se producen mediante reacciones a partir de compuestos azoicos preexistentes. Las reacciones típicas incluyen la formación de complejos metálicos y la acilación.
Los pigmentos azoicos tienen una estructura química similar a la de los colorantes azoicos, pero carecen de grupos solubilizantes. Como son prácticamente insolubles en todos los disolventes, no se purifican fácilmente y, por lo tanto, requieren precursores altamente purificados.
Los pigmentos azoicos son importantes en una variedad de plásticos, cauchos y pinturas (incluidas las pinturas para artistas). Tienen excelentes propiedades colorantes, principalmente en el rango del amarillo al rojo, así como una buena resistencia a la luz . La resistencia a la luz depende no solo de las propiedades del compuesto azoico orgánico, sino también de la forma en que se han absorbido en el portador del pigmento.
Los pigmentos azoicos son los más antiguos y también los más utilizados entre los pigmentos alimentarios. Fueron descubiertos por Peter Griess en 1858. [8]
Para que los colorantes sean útiles, deben poseer un alto grado de estabilidad química y fotolítica. Como resultado de esta estabilidad, la fotólisis no se considera una vía de degradación para los colorantes azoicos. Para prolongar la vida útil de los productos teñidos con colorantes azoicos, es esencial garantizar la estabilidad frente al ataque microbiano, y las pruebas han demostrado que los colorantes azoicos se biodegradan de manera insignificante en pruebas a corto plazo en condiciones aeróbicas. Sin embargo, en condiciones anaeróbicas, se puede observar decoloración como consecuencia de la biodegradación. [9]
Muchos pigmentos azoicos no son tóxicos, aunque algunos, como el naranja de dinitroanilina , el naranja de orto-nitroanilina o el pigmento naranja 1, 2 y 5, son mutagénicos y cancerígenos . [10] [11]
Los colorantes azoicos derivados de la bencidina son carcinógenos ; la exposición a ellos se ha asociado clásicamente con el cáncer de vejiga . [12] En consecuencia, la producción de colorantes azoicos derivados de la bencidina se interrumpió en la década de 1980 en muchos países occidentales. [5]
Algunos colorantes azoicos se degradan en condiciones reductoras y liberan cualquiera de un grupo de aminas aromáticas definidas . Desde septiembre de 2003, la Unión Europea ha prohibido la fabricación o venta de bienes de consumo que contengan las aminas enumeradas. Dado que sólo un pequeño número de colorantes producían esas aminas, relativamente pocos productos se vieron realmente afectados. [4]