La dispersión de luz estática es una técnica de química física que mide la intensidad de la luz dispersada para obtener el peso molecular promedio M w de una macromolécula como un polímero o una proteína en solución. La medición de la intensidad de dispersión en muchos ángulos permite calcular el radio cuadrático medio, también llamado radio de giro R g . Midiendo la intensidad de dispersión para muchas muestras de diversas concentraciones, se puede calcular el segundo coeficiente virial , A2 . [1] [2] [3] [4] [5]
La dispersión de luz estática también se utiliza comúnmente para determinar el tamaño de suspensiones de partículas en los rangos sub-μm y supra-μm, a través de los formalismos de difracción de Lorenz-Mie (ver Dispersión de Mie ) y Fraunhofer , respectivamente.
Para los experimentos de dispersión de luz estática, se lanza una luz monocromática de alta intensidad, generalmente un láser, a una solución que contiene las macromoléculas. Se utilizan uno o varios detectores para medir la intensidad de dispersión en uno o varios ángulos. La dependencia angular es necesaria para obtener mediciones precisas tanto de la masa molar como del tamaño de todas las macromoléculas con un radio superior al 1-2% de la longitud de onda incidente. Por lo tanto, las mediciones simultáneas en varios ángulos con respecto a la dirección de la luz incidente, conocidas como dispersión de luz multiángulo (MALS) o dispersión de luz láser multiángulo (MALLS), generalmente se consideran la implementación estándar de dispersión de luz estática. Se pueden encontrar detalles adicionales sobre la historia y la teoría de MALS en Dispersión de luz multiángulo .
Para medir el peso molecular promedio directamente sin calibración a partir de la intensidad de dispersión de la luz, es necesario conocer la intensidad del láser, la eficiencia cuántica del detector y el volumen de dispersión total y el ángulo sólido del detector. Dado que esto no es práctico, todos los instrumentos comerciales se calibran utilizando un dispersor fuerte y conocido como el tolueno , ya que la relación de Rayleigh del tolueno y algunos otros disolventes se midieron utilizando un instrumento de dispersión de luz absoluta.
Para un instrumento de dispersión de luz compuesto por muchos detectores colocados en varios ángulos, todos los detectores deben responder de la misma manera. Por lo general, los detectores tendrán una eficiencia cuántica ligeramente diferente , diferentes ganancias y observarán diferentes volúmenes de dispersión geométrica. En este caso es absolutamente necesaria una normalización de los detectores. Para normalizar los detectores, primero se realiza una medición de un disolvente puro. Luego se añade un dispersor isotrópico al disolvente. Dado que los dispersores isotrópicos dispersan la misma intensidad en cualquier ángulo, la eficiencia y la ganancia del detector se pueden normalizar con este procedimiento. Es conveniente normalizar todos los detectores al detector de ángulo de 90°.
donde I R (90) es la intensidad de dispersión medida para el dispersor Rayleigh por el detector de ángulo de 90°.
La ecuación más común para medir el peso molecular promedio en peso, Mw , es la ecuación de Zimm [5] (el lado derecho de la ecuación de Zimm se proporciona incorrectamente en algunos textos, como señalaron Hiemenz y Lodge): [ 6 ]
dónde
y
con
y el vector de dispersión de la luz polarizada verticalmente es
con n 0 el índice de refracción del disolvente, λ la longitud de onda de la fuente de luz, N A la constante de Avogadro , c la concentración de la solución y d n /d c el cambio en el índice de refracción de la solución con el cambio de concentración. La intensidad del analito medida en un ángulo es I A (θ) . En estas ecuaciones, el subíndice A es para el analito (la solución) y T es para el tolueno con la relación de Rayleigh de tolueno, siendo RT 1,35×10 −5 cm −1 para un láser de HeNe . Como se describió anteriormente, el radio de giro, R g , y el segundo coeficiente virial, A 2 , también se calculan a partir de esta ecuación. El incremento del índice de refracción dn/dc caracteriza el cambio del índice de refracción n con la concentración c y se puede medir con un refractómetro diferencial.
Un gráfico de Zimm se construye a partir de una doble extrapolación hasta el ángulo cero y la concentración cero desde muchos ángulos y muchas mediciones de concentración. En su forma más simple, la ecuación de Zimm se reduce a:
para mediciones realizadas en ángulo bajo y dilución infinita ya que P (0) = 1.
Por lo general, se desarrollan varios análisis para analizar la dispersión de partículas en solución para derivar las características físicas de las partículas antes mencionadas. Un experimento simple de dispersión de luz estática implica que la intensidad promedio de la muestra que se corrige por la dispersión del solvente producirá la relación de Rayleigh, R , en función del ángulo o el vector de onda q, de la siguiente manera:
La intensidad dispersada se puede representar gráficamente en función del ángulo para dar información sobre el R g que se puede calcular simplemente utilizando la aproximación de Guinier de la siguiente manera:
donde ln(ΔR(θ)) = lnP(θ) también conocido como factor de forma con q = 4πn 0 sin(θ/2)/λ . Por lo tanto, una gráfica de la relación de Rayleigh corregida, ΔR(θ) vs sen 2 (θ/2) o q 2 producirá una pendiente R g 2 /3 . Sin embargo, esta aproximación sólo es cierta para qR g < 1 . Tenga en cuenta que para un gráfico de Guinier, no se necesitan el valor de dn/dc ni la concentración.
El diagrama de Kratky se utiliza normalmente para analizar la conformación de proteínas , pero se puede utilizar para analizar el modelo de paseo aleatorio de polímeros . Se puede hacer un diagrama de Kratky trazando sen 2 (θ/2)ΔR(θ) vs sin(θ/2) o q 2 ΔR(θ) vs q .
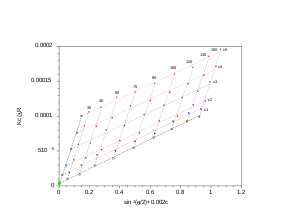
Para polímeros y complejos poliméricos que son monodispersos ( ) según lo determinado por dispersión de luz estática, un diagrama de Zimm es un medio convencional para derivar parámetros como R g , masa molecular M w y el segundo coeficiente virial A 2 .
Hay que tener en cuenta que si no se implementa la constante del material K , un gráfico de Zimm solo arrojará R g . Por lo tanto, implementar K producirá la siguiente ecuación:
El análisis realizado con el gráfico de Zimm utiliza una doble extrapolación a concentración cero y ángulo de dispersión cero, lo que da como resultado un gráfico romboidal característico. Como la información angular está disponible, también es posible obtener el radio de giro ( R g ). Los experimentos se realizan en varios ángulos que cumplan la condición y al menos 4 concentraciones. La realización de un análisis Zimm en una única concentración se conoce como análisis Zimm parcial y solo es válido para soluciones diluidas de dispersores puntuales fuertes. El Zimm parcial sin embargo no arroja el segundo coeficiente virial , debido a la ausencia de la concentración variable de la muestra. Más específicamente, se supone que el valor del segundo coeficiente virial es igual a cero o se ingresa como un valor conocido para realizar el análisis parcial de Zimm.

Si las partículas medidas son más pequeñas que λ/20, el factor de forma P(θ) puede despreciarse ( P(θ) →1). Por lo tanto, la ecuación de Zimm se simplifica a la ecuación de Debye, de la siguiente manera:
Tenga en cuenta que esto también es el resultado de una extrapolación al ángulo de dispersión cero. Al adquirir datos sobre la concentración y la intensidad de dispersión, el gráfico de Debye se construye trazando Kc / ΔR(θ) frente a la concentración. La intersección de la línea ajustada da la masa molecular, mientras que la pendiente corresponde al segundo coeficiente virial.
Como el gráfico de Debye es una simplificación de la ecuación de Zimm, se aplican las mismas limitaciones de esta última, es decir, las muestras deben presentar una naturaleza monodispersa. Para muestras polidispersas, la masa molecular resultante de una medición estática de dispersión de luz representará un valor promedio. Una ventaja del gráfico de Debye es la posibilidad de determinar el segundo coeficiente virial. Este parámetro describe la interacción entre las partículas y el disolvente. En soluciones de macromoléculas, por ejemplo, puede asumir valores negativos (se favorecen las interacciones entre partículas), cero o positivos (se favorecen las interacciones entre partículas). [8]
La dispersión estática de la luz supone que cada fotón detectado sólo se ha dispersado exactamente una vez. Por lo tanto, el análisis según los cálculos indicados anteriormente solo será correcto si la muestra se ha diluido lo suficiente como para garantizar que la muestra no disperse los fotones varias veces antes de ser detectados. La interpretación precisa se vuelve extremadamente difícil para sistemas con contribuciones no despreciables de dispersión múltiple. En muchos instrumentos comerciales donde el análisis de la señal de dispersión se realiza automáticamente, es posible que el usuario nunca note el error. Particularmente para partículas más grandes y aquellas con alto contraste de índice de refracción, esto limita la aplicación de la dispersión de luz estática estándar a concentraciones de partículas muy bajas. Por otro lado, para las macromoléculas solubles que exhiben un contraste de índice de refracción relativamente bajo frente al solvente, incluida la mayoría de los polímeros y biomoléculas en sus respectivos solventes, la dispersión múltiple rara vez es un factor limitante, incluso en concentraciones que se acercan a los límites de solubilidad.
Sin embargo, como lo muestra Schaetzel, [9] es posible suprimir la dispersión múltiple en experimentos de dispersión de luz estática mediante un enfoque de correlación cruzada. La idea general es aislar la luz dispersada individualmente y suprimir las contribuciones no deseadas de la dispersión múltiple en un experimento de dispersión de luz estática. Se han desarrollado y aplicado diferentes implementaciones de dispersión de luz por correlación cruzada. Actualmente, el esquema más utilizado es el llamado método de dispersión de luz dinámica 3D. [10] [11] El mismo método también se puede utilizar para corregir datos dinámicos de dispersión de luz para múltiples contribuciones de dispersión. [12]
Es posible que las muestras que cambian sus propiedades después de la dilución no se analicen mediante dispersión de luz estática en términos del modelo simple presentado aquí como ecuación de Zimm. Un análisis más sofisticado conocido como 'dispersión de luz estática (o multiángulo) de gradiente de composición' (CG-SLS o CG-MALS) es una clase importante de métodos para investigar las interacciones proteína-proteína , las propiedades coligativas y otras interacciones macromoleculares como proporciona, además del tamaño y el peso molecular, información sobre la afinidad y estequiometría de complejos moleculares formados por una o más especies macromoleculares/biomoleculares asociadas. En particular, la dispersión de la luz estática de una serie de diluciones se puede analizar para cuantificar la autoasociación, la oligomerización reversible y la atracción o repulsión no específica, mientras que la dispersión de la luz estática de mezclas de especies se puede analizar para cuantificar la heteroasociación. [13]
Una de las principales aplicaciones de la dispersión de luz estática para la determinación de la masa molecular es en el campo de las macromoléculas, como proteínas y polímeros, [14] [15] [16] ya que es posible medir la masa molecular de las proteínas sin ninguna suposición sobre su forma. La dispersión de luz estática generalmente se combina con otras técnicas de caracterización de partículas, como la cromatografía de exclusión por tamaño (SEC), la dispersión de luz dinámica (DLS) y la dispersión de luz electroforética (ELS).