El ácido cinámico es un compuesto orgánico con la fórmula C 6 H 5 -CH=CH- COOH . Es un compuesto cristalino blanco que es ligeramente soluble en agua y libremente soluble en muchos solventes orgánicos. [4] Clasificado como un ácido carboxílico insaturado , se encuentra de forma natural en varias plantas. Existe tanto como isómero cis como trans , aunque este último es más común. [5]
El ácido cinámico es un intermediario central en la biosíntesis de una gran variedad de productos naturales, entre ellos los lignoles (precursores de la lignina y la lignocelulosa ), flavonoides , isoflavonoides , cumarinas , auronas , estilbenos , catequinas y fenilpropanoides . Su biosíntesis implica la acción de la enzima fenilalanina amonia-liasa (PAL) sobre la fenilalanina . [6]
Se obtiene del aceite de canela o de bálsamos como el estoraque . [4] También se encuentra en la manteca de karité . [ cita requerida ] El ácido cinámico tiene un olor parecido al de la miel ; [2] y su éster etílico más volátil, el cinamato de etilo , es un componente del sabor en el aceite esencial de canela , en el que el cinamaldehído relacionado es el componente principal. También se encuentra en la madera de muchas especies de árboles diversas. [7]
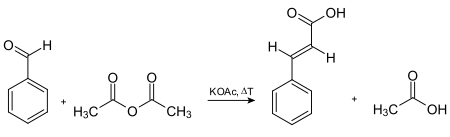
El ácido cinámico se sintetizó por primera vez mediante la condensación catalizada por una base de cloruro de acetilo y benzaldehído , seguida de la hidrólisis del producto de cloruro de ácido . [5] En 1890, Rainer Ludwig Claisen describió la síntesis de cinamato de etilo mediante la reacción de acetato de etilo con benzaldehído en presencia de sodio como base. [8] Otra forma de preparar ácido cinámico es mediante la reacción de condensación de Knoevenagel . [9] Los reactivos para esto son benzaldehído y ácido malónico en presencia de una base débil, seguido de una descarboxilación catalizada por ácido . También se puede preparar por oxidación de cinamaldehído , condensación de cloruro de benzal y acetato de sodio (seguida de hidrólisis ácida) y la reacción de Perkin . La ruta comercialmente utilizada más antigua para el ácido cinámico implica la reacción de Perkin , que se da en el siguiente esquema [5]
El ácido cinámico, obtenido a partir de la autooxidación del cinamaldehído , se metaboliza en benzoato de sodio en el hígado. [11]
El ácido cinámico se utiliza en aromas, índigo sintético y ciertos productos farmacéuticos . Un uso importante es como precursor para producir cinamato de metilo , cinamato de etilo y cinamato de bencilo para la industria del perfume. [4] El ácido cinámico es un precursor del edulcorante aspartamo a través de la aminación catalizada por enzimas con fenilalanina . [5] El ácido cinámico puede dimerizarse en disolventes no polares, lo que da lugar a diferentes relaciones de energía libre lineal . [12]
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )