Un complejo de carbeno de metal de transición es un compuesto organometálico que presenta un ligando de carbono divalente , también llamado carbeno . [1] Los complejos de carbeno se han sintetizado a partir de la mayoría de los metales de transición y metales del bloque f , [2] utilizando muchas rutas sintéticas diferentes, como la adición nucleofílica y la abstracción de alfa-hidrógeno. [1] El término ligando de carbeno es un formalismo ya que muchos no se derivan directamente de los carbenos y la mayoría son mucho menos reactivos que los carbenos solitarios. [2] Descritos a menudo como =CR 2 , los ligandos de carbeno son intermedios entre alquilos (-CR 3 ) y carbinos (≡CR) . En la síntesis se utilizan muchos reactivos diferentes a base de carbeno, como el reactivo de Tebbe . También aparecen en reacciones catalíticas, especialmente en la metátesis de alquenos , y son valiosos en catálisis industrial heterogénea y homogénea para la preparación de productos químicos finos a escala industrial y de laboratorio. [1] [3] [4]
Los complejos de carbeno metálico a menudo se clasifican en dos tipos. Los carbenos de Fischer, que llevan el nombre de Ernst Otto Fischer , presentan fuertes aceptores π en el metal y son electrófilos en el átomo de carbono del carbeno. Los carbenos Schrock , que llevan el nombre de Richard R. Schrock , se caracterizan por tener centros de carbono carbeno más nucleofílicos; Estas especies suelen presentar metales con un estado de oxidación (valencia) más alto. Los carbenos N -heterocíclicos (NHC) se popularizaron tras el aislamiento de Arduengo de un carbeno libre estable en 1991. [5] Como reflejo del crecimiento del área, ahora se conocen complejos de carbeno con una amplia gama de diferentes reactividades y diversos sustituyentes. A menudo no es posible clasificar un complejo de carbeno únicamente con respecto a su electrofilia o nucleofilicidad. [1]

Las características comunes de los carbenos Fisher son: [6]
Los ejemplos incluyen (CO) 5W =COMePh y (OC) 5Cr =C(NR2 ) Ph .

Los complejos de carbeno de Fisher están relacionados con la forma singlete de los carbenos, donde ambos electrones ocupan el mismo orbital sp 2 en el carbono. Este par solitario se dona a un orbital d vacío de base metálica, formando un enlace σ. Es posible el enlace π desde un orbital d de metal lleno al orbital p vacío del átomo de carbono. Sin embargo, esta interacción es generalmente débil ya que los átomos donantes alfa también donan a este orbital. Como tales, los carbenos de Fisher se caracterizan por tener un carácter de doble enlace parcial. Las principales estructuras de resonancia de los carbenos de Fisher colocan la carga negativa en el centro del metal y la positiva en el átomo de carbono, haciéndolo electrófilo. [6]

Los carbenos de Fischer pueden compararse con las cetonas, siendo el átomo de carbono del carbeno electrófilo, como el átomo de carbono carbonílico de una cetona. Esto se puede ver en las estructuras de resonancia , donde hay una contribución significativa de la estructura que lleva un centro de carbono positivo. [6] Al igual que las cetonas, las especies de carbeno de Fischer pueden sufrir reacciones similares a las del aldólico . Los átomos de hidrógeno unidos al átomo de carbono α al átomo de carbono del carbeno son ácidos y pueden ser desprotonados por una base como el n -butillitio , para dar un nucleófilo, que puede sufrir reacciones adicionales. [7]

Los carbenos Schrock no tienen ligandos receptores de π en el centro metálico. A menudo se les llama complejos de alquilideno . Normalmente, este subconjunto de complejos de carbeno se encuentra con: [6]
Los ejemplos incluyen ((CH3 ) 3CCH2 ) Ta =CHC(CH3 ) 3 [ 9] y Os ( PPh3 ) 2 (NO)Cl(= CH2 ) . [10]

El enlace en tales complejos puede verse como el acoplamiento de un metal en estado triplete y un carbeno triplete, formando un verdadero doble enlace. Tanto el átomo de metal como el de carbono donan 2 electrones, uno a cada enlace. Dado que no hay donación al átomo de carbeno de los grupos adyacentes, el grado de enlace pi es mucho mayor, lo que da un doble enlace fuerte. Estos enlaces están débilmente polarizados hacia el carbono y por tanto el átomo de carbeno es un nucleófilo. Además, las principales estructuras de resonancia del carbeno de Schrock ponen la carga negativa en el átomo de carbono, haciéndolo nucleofílico. [6] Los complejos con el ligando metilideno ( =CH 2 ) son los carbenos de tipo Schrock más simples.

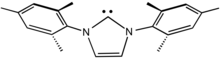
Los carbenos N -heterocíclicos (NHC) son ligandos de carbeno particularmente comunes. [11] Son populares porque se preparan más fácilmente que los carbenos de Schrock y Fischer. De hecho, muchos NHC se aíslan como ligando libre, ya que son carbenos persistentes . [12] [13] Al estar fuertemente estabilizados por sustituyentes donadores de π, los NHC son potentes donantes de σ, pero el enlace π con el metal es débil. [14] Por esta razón, el enlace entre el carbono y el centro metálico a menudo se representa mediante un enlace dativo simple, mientras que los carbenos de Fischer y Schrock generalmente se representan con dobles enlaces al metal. Siguiendo con esta analogía, los NHC a menudo se comparan con ligandos de trialquilfosfina . Al igual que las fosfinas, los NHC sirven como ligandos espectadores que influyen en la catálisis mediante una combinación de efectos electrónicos y estéricos, pero no se unen directamente a sustratos. [15] [16]
Un ejemplo temprano de este modo de enlace lo proporcionó [C 5 Me 5 Mn(CO) 2 ] 2 (μ−CO) preparado a partir de diazometano :
Otro ejemplo de esta familia de compuestos es el reactivo de Tebbe . Cuenta con un puente de metileno que une titanio y aluminio . [17]
Los complejos de carbeno metálico tienen aplicaciones en catálisis heterogénea y homogénea y como reactivos para reacciones orgánicas.

La aplicación dominante de los carbenos metálicos no involucra ninguna de las clases de compuestos anteriores, sino catalizadores heterogéneos utilizados para la metátesis de alquenos para la síntesis de alquenos superiores. Se utilizan diversas reacciones relacionadas para interconvertir alquenos ligeros, por ejemplo, butenos, propileno y etileno. [18] Los complejos de carbeno se invocan como intermediarios en la ruta Fischer-Tropsch hacia los hidrocarburos. [3]
Se han utilizado una variedad de catalizadores de carbeno homogéneos, especialmente los catalizadores de rutenio de Grubbs y molibdeno-imido de Schrock para la metátesis de olefinas en la síntesis a escala de laboratorio de productos naturales y ciencia de materiales . [4]
Se pueden utilizar complejos de carbeno homogéneos de tipo Schrock, como el reactivo de Tebbe, para la olefinación de carbonilos, reemplazando el átomo de oxígeno por un grupo metilideno. El átomo de carbono nucleofílico se comporta de manera similar al átomo de carbono del iluro de fósforo en la reacción de Wittig , atacando al átomo de carbonilo electrófilo de una cetona, seguido de la eliminación de un óxido metálico. [1]

En la reacción de abstracción nucleófila , se puede extraer un grupo metilo del grupo donante de un carbeno de Fischer, convirtiéndolo en un nucleófilo fuerte para reacciones posteriores. [6]

Los compuestos diazo como el fenildiazoacetato de metilo se pueden utilizar para la ciclopropanación o para insertarse en enlaces CH de sustratos orgánicos. Estas reacciones están catalizadas por tetraacetato de dirodio o derivados quirales relacionados. Se supone que dicha catálisis se produce mediante la intermediación de complejos de carbeno. [19]

Los carbenos de Fischer se utilizan con alquinos como reactivos de partida para la reacción de Wulff-Dötz , formando fenoles. [20]


El primer complejo de carbeno metálico que se informó fue la sal roja de Chugaev , sintetizada por primera vez ya en 1925, aunque nunca se identificó como un complejo de carbeno. [21] La caracterización de (CO)5W(COCH3(Ph)) en la década de 1960 se cita a menudo como el punto de partida del área y Ernst Otto Fischer , por este y otros logros en química organometálica, recibió el Premio Nobel de 1973 en Química . [22] En 1968, Hans-Werner Wanzlick y Karl Öfele informaron por separado sobre carbenos N-heterocíclicos unidos a metales. [6] [23] [24] La síntesis y caracterización de ((CH 3 ) 3 CCH 2 )Ta=CHC(CH 3 ) 3 por Richard R. Schrock en 1974 marcó el primer complejo de alquilideno metálico. [9] En 1991, Anthony J. Arduengo sintetizó y cristalizó el primer carbeno persistente , un NHC con grandes grupos alquilo de adamantano , acelerando el campo de ligandos de N-heterocarbeno hasta su uso actual. [5] [6]