
Un ion carbenio es un ion positivo con la estructura RR′R″C + , es decir, una especie química con un átomo de carbono que tiene tres enlaces covalentes y lleva una carga formal +1 . Pero la IUPAC confunde el número de coordinación con la valencia y considera incorrectamente que el carbono del carbenio es trivalente. [1]
En la literatura más antigua, el nombre ion carbonio se usaba para esta clase, pero ahora se refiere exclusivamente a otra familia de carbocationes , los iones carbonio , donde la IUPAC considera incorrectamente que el carbono cargado es pentavalente , [1] pero está pentacoordinado, no pentavalente. , porque el número de coordinación y la valencia son dos cosas diferentes. Las definiciones actuales fueron propuestas por el químico George Andrew Olah en 1972 [2] y ahora son ampliamente aceptadas.
Los iones carbenio son generalmente muy reactivos debido a que tienen un octeto de electrones incompleto; sin embargo, ciertos iones carbenio, como el ion tropilio , son relativamente estables debido a que la carga positiva se deslocaliza entre los átomos de carbono.
Los iones de carbenio se clasifican en primarios , secundarios o terciarios dependiendo de si el número de átomos de carbono unidos al carbono ionizado es 1, 2 o 3. (Iones con cero carbonos unidos al carbono ionizado, como el metenio , CH+
3, generalmente se incluyen en la clase primaria).
La estabilidad suele aumentar con el número de grupos alquilo unidos al carbono que lleva la carga. Los carbocationes terciarios son más estables (y se forman más fácilmente) que los carbocationes secundarios, porque se estabilizan mediante hiperconjugación . Los carbocationes primarios son muy inestables. Por lo tanto, reacciones como la reacción S N 1 y la reacción de eliminación E1 normalmente no ocurren si se formara un carbenio primario.
Sin embargo, un carbono con doble enlace con el carbono ionizado puede estabilizar el ion por resonancia . Cationes como el catión alilo , CH
2=CH-CH+
2, y el catión bencilo , C
6h
5−CH+
2, son más estables que la mayoría de los otros carbocationes. Las moléculas que pueden formar carbenios alílicos o bencílicos son especialmente reactivas. Los iones carbenio también pueden estabilizarse mediante heteroátomos . [3]
Los iones carbenio pueden sufrir reacciones de reordenamiento desde estructuras menos estables a otras igualmente estables o más estables con constantes de velocidad superiores a 10 9 s −1 . Este hecho complica las vías sintéticas de muchos compuestos. Por ejemplo, cuando el pentan-3-ol se calienta con HCl acuoso, el carbocatión 3-pentilo formado inicialmente se reorganiza en una mezcla estadística de 3-pentilo y 2-pentilo. Estos cationes reaccionan con el ion cloruro para producir 3-cloropentano y 2-cloropentano en una proporción de aproximadamente 1:2.
Los iones carbenio se pueden preparar directamente a partir de alcanos eliminando un anión hidruro , H−
, con un ácido fuerte. Por ejemplo, el ácido mágico , una mezcla de pentafluoruro de antimonio ( SbF
5) y ácido fluorosulfúrico ( FSO
3H ), convierte el isobutano en el catión trimetilcarbenio, (CH
3)
3C+
. [4]
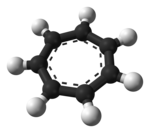
El ion tropilio es una especie aromática con la fórmula C
7h+
7. [5] Su nombre deriva de la molécula tropina (llamada a su vez por la molécula atropina ). Las sales del catión tropilio pueden ser estables, por ejemplo, tetrafluoroborato de tropilio . Puede elaborarse a partir de cicloheptatrieno (tropilideno) y bromo o pentacloruro de fósforo . [6]
Es un ion heptagonal , cíclico y plano; también tiene 6 electrones π (4 n + 2, donde n = 1), lo que cumple la regla de aromaticidad de Hückel . Puede coordinarse como ligando de átomos metálicos .
La estructura que se muestra es un compuesto de siete contribuyentes de resonancia en los que cada carbono lleva parte de la carga positiva.
En 1891, G. Merling obtuvo una sal soluble en agua a partir de una reacción de cicloheptatrieno y bromo. [7] La estructura fue aclarada por Eggers Doering y Knox en 1954. [8] [9]
Otro ion carbenio aromático es el ciclopropenilo o ion ciclopropenio , C
3h+
3, obtenido por Ronald Breslow y John T. Groves en 1970. [10] Aunque menos estable que el catión tropilio, este ion carbenio también puede formar sales a temperatura ambiente. Breslow y Groves descubrieron que las soluciones de tales sales tenían propiedades espectroscópicas y químicas que coincidían con las expectativas de un ion carbenio aromático.
El catión trifenilcarbenio o trifenilmetilo, [C(C
6h
5)
3]+
, es especialmente estable porque la carga positiva se puede distribuir entre 10 de los átomos de carbono (los 3 átomos de carbono en las posiciones orto y para de cada uno de los tres grupos fenilo, más el átomo de carbono central). Existe en los compuestos hexafluorofosfato de trifenilmetilo [C(C
6h
5)
3]+
[FP
6]−
, tetrafluoroborato de trifenilmetilo [C(C
6h
5)
3]+
[novio
4]−
, y perclorato de trifenilmetilo [C(C
6h
5)
3]+
[ClO
4]−
. [11] Entre sus derivados se encuentran los colorantes triarilmetano .

Un ion arenio es un catión ciclohexadienilo que aparece como un intermedio reactivo en la sustitución aromática electrófila . [12] Por razones históricas, este complejo también se denomina intermedio de Wheland , [13] o complejo σ .
Dos átomos de hidrógeno unidos a un carbono se encuentran en un plano perpendicular al anillo de benceno. [14] El ion arenio ya no es una especie aromática; sin embargo, es relativamente estable debido a la deslocalización: la carga positiva se deslocaliza en 5 átomos de carbono a través del sistema π , como se muestra en las siguientes estructuras de resonancia :
Otra contribución a la estabilidad de los iones de arenio es la ganancia de energía resultante del fuerte enlace entre el benceno y el electrófilo complejado.
El ion arenio más pequeño es el benceno protonado , C
6h+
7. El ion bencenio se puede aislar como un compuesto estable cuando el benceno es protonado por el superácido carborano , H(CB 11 H(CH 3 ) 5 Br 6 ). [15] La sal de bencenio es cristalina y tiene estabilidad térmica hasta 150 °C. Las longitudes de enlace deducidas de la cristalografía de rayos X son consistentes con una estructura de catión ciclohexadienilo.
Un ion acilio es un catión con la fórmula RCO + . [16] La estructura se describe como R−C≡O + o R−= O. Es el equivalente sintético y reactivo de un carbocatión acilo, pero la estructura real tiene el oxígeno y el carbono unidos por un triple enlace. Estas especies son intermediarios reactivos comunes, por ejemplo, en las acilaciones de Friedel-Crafts y en muchas otras reacciones orgánicas , como el reordenamiento de Hayashi . Las sales que contienen iones de acilo se pueden generar mediante la eliminación del haluro de los haluros de acilo :
La distancia C-O en estos cationes es cercana a 1,1 ångströms , incluso más corta que la del monóxido de carbono . [17] Los cationes acylium son fragmentos característicos observados en los espectros de masas EI de las cetonas .