La bradicardia , también llamada bradiarritmia , es una frecuencia cardíaca en reposo inferior a 60 latidos por minuto (BPM). [1] Si bien la bradicardia puede ser el resultado de una variedad de procesos patológicos, comúnmente es una respuesta fisiológica al acondicionamiento cardiovascular o se debe a un bloqueo auriculoventricular tipo 1 asintomático . Las frecuencias cardíacas en reposo inferiores a 50 BPM suelen ser normales durante el sueño en adultos jóvenes y sanos y en atletas . [2] En grandes estudios poblacionales de adultos sin enfermedad cardíaca subyacente, las frecuencias cardíacas en reposo de 45 a 50 BPM parecen ser los límites inferiores de lo normal, dependiendo de la edad y el sexo. [3] [4] La bradicardia es más probable que se descubra en personas mayores, ya que tanto la edad como la progresión de la enfermedad cardíaca subyacente contribuyen a su desarrollo. [5]
La bradicardia puede estar asociada con síntomas de fatiga , disnea , mareos , confusión y síncope franco debido a la reducción del flujo sanguíneo hacia el cerebro, los pulmones y el músculo esquelético. [6] Los tipos de síntomas a menudo dependen de la etiología de la frecuencia cardíaca lenta, clasificada por la ubicación anatómica de una disfunción dentro del sistema de conducción cardíaca . [7] Generalmente, estas clasificaciones involucran las categorías amplias de disfunción del nodo sinusal (SND), bloqueo auriculoventricular y otras enfermedades del tejido de conducción. [8] Sin embargo, la bradicardia también puede producirse sin disfunción del sistema de conducción nativo, y surge como consecuencia de medicamentos que incluyen betabloqueantes , bloqueadores de los canales de calcio , antiarrítmicos y otros fármacos colinérgicos . El exceso de actividad del nervio vago o la hipersensibilidad del seno carotídeo son causas neurológicas de bradicardia sintomática transitoria. El hipotiroidismo y los trastornos metabólicos son otras causas extrínsecas comunes de bradicardia. [6]
El tratamiento de la bradicardia generalmente se reserva para pacientes con síntomas, independientemente de la frecuencia cardíaca mínima durante el sueño o la presencia de anomalías concomitantes del ritmo cardíaco (Ver: pausa sinusal ), que son comunes en esta afección. [6] Se ha demostrado que la SND no tratada aumenta el riesgo futuro de insuficiencia cardíaca y síncope, lo que a veces justifica un tratamiento definitivo con un marcapasos implantado . [9] [8] En las causas auriculoventriculares de bradicardia, a menudo se requiere la implantación de un marcapasos permanente cuando no se encuentran causas reversibles de la enfermedad. [6] [7] Tanto en la SND como en el bloqueo auriculoventricular, el tratamiento médico tiene poca importancia a menos que el paciente esté hemodinámicamente inestable , lo que puede requerir el uso de medicamentos como atropina , isoproterenol e intervenciones como estimulación transcutánea , hasta el momento. que se pueda realizar un diagnóstico adecuado y seleccionar un tratamiento a largo plazo. [7] Si bien las bradicardias asintomáticas rara vez requieren tratamiento, se recomienda consultar con un médico, especialmente en los ancianos. [ cita necesaria ]
El término "bradicardia relativa" puede referirse a una frecuencia cardíaca inferior a la esperada en un estado patológico particular, a menudo una enfermedad febril. [10] La "incompetencia cronotrópica" (IC) se refiere a un aumento inadecuado de la frecuencia cardíaca durante períodos de mayor demanda, a menudo debido al ejercicio, y es un signo importante de SND y una indicación para la implantación de un marcapasos. [8] [7]
La palabra "bradicardia" proviene del griego βραδύς bradys "lento" y καρδία kardia "corazón". [11]
El corazón es un tipo de músculo especializado que contiene unidades repetidas de cardiomiocitos o células del músculo cardíaco. Como la mayoría de las células, los cardiomiocitos mantienen un voltaje negativo altamente regulado en reposo y son capaces de propagar potenciales de acción , de manera muy similar a las neuronas. [12] Mientras está en reposo, el voltaje celular negativo de un cardiomiocito puede elevarse por encima de un cierto umbral (llamado despolarización ) mediante un potencial de acción entrante, lo que hace que el miocito se contraiga . Cuando estas contracciones ocurren de manera coordinada, las aurículas y los ventrículos del corazón bombearán sangre al resto del cuerpo. [12]
Normalmente, el origen del potencial de acción que provoca la contracción de los cardiomiocitos se origina en el nódulo sinoauricular (nódulo SA). Esta colección de tejido de conducción especializado se encuentra en la aurícula derecha, cerca de la entrada de la vena cava superior . [13] El nódulo SA contiene células marcapasos que demuestran "automaticidad" y son capaces de generar impulsos que viajan a través del corazón y crean un latido cardíaco constante. [13]
Al comienzo del ciclo cardíaco, el nódulo SA genera un potencial de acción eléctrica que se propaga por las aurículas derecha e izquierda , provocando la contracción auricular del ciclo cardíaco . [13] Este impulso eléctrico se transmite al nódulo auriculoventricular (nódulo AV), otro grupo especializado de células ubicadas en la base de la aurícula derecha, que es la única conexión eléctrica anatómicamente normal entre las aurículas y los ventrículos. Los impulsos que atraviesan el nódulo AV se ralentizan antes de llegar a los ventrículos, [14] permitiendo el llenado adecuado de los ventrículos antes de la contracción. Los nódulos SA y AV están estrechamente regulados por fibras del sistema nervioso autónomo, lo que permite el ajuste del gasto cardíaco por parte del sistema nervioso central en momentos de mayor demanda metabólica.
Después de una conducción más lenta a través del nódulo auriculoventricular, el potencial de acción producido originalmente en el nódulo SA ahora fluye a través del sistema de His-Purkinje. El haz de His se origina en el nodo AV y rápidamente se divide en una rama izquierda y una derecha, cada una destinada a un ventrículo diferente. Finalmente, estas ramas del haz terminan en las pequeñas fibras de Purkinje que inervan el tejido miocárdico. El sistema His-Purkinje conduce potenciales de acción mucho más rápido de lo que se puede propagar entre las células del miocardio, lo que permite que todo el miocardio ventricular se contraiga en un período de tiempo menor, mejorando la función de la bomba. [13]

La mayoría de las causas patológicas de bradicardia resultan del daño a este sistema de conducción cardíaca normal en varios niveles: el nódulo sinoauricular, el nódulo auriculoventricular o del daño al tejido de conducción entre o después de estos nodos.
La bradicardia causada por las alteraciones de la actividad del nodo sinusal se divide en tres tipos.
Sinus bradycardia is a sinus rhythm of less than 50 BPM.[15] Cardiac action potentials are generated from the SA node, propagated through an otherwise normal conduction system, but occur at a slow rate. It is a common condition found in both healthy individuals and those considered well-conditioned athletes.[1] Studies have found that 50–85% of conditioned athletes have benign sinus bradycardia, as compared to 23% of the general population studied.[16] The heart muscle of athletes has a higher stroke volume, and so requires fewer contractions to circulate the same volume of blood.[17] Asymptomatic sinus bradycardia decreases in prevalence with age.
Sinus arrhythmias are heart rhythm abnormalities characterized by variations in the cardiac cycle length in excess of 120 milliseconds (longest cycle - shortest cycle).[7] These are the most common type of arrhythmia in the general population, and are usually without significant consequence. They typically occur in the young, athletes, or after administration of medications such as morphine. The types of sinus arrhythmia are separated into the respiratory and non-respiratory categories.[7]
Respiratory sinus arrhythmia refers to the physiologically normal variation in heart rate due to breathing. During inspiration, vagus nerve activity decreases, reducing parasympathetic innervation of the sinoatrial node, causing an increase in heart rate. During expiration, heart rates fall due to the converse occurring.[7]
Non-respiratory causes of sinus arrhythmia include sinus pause, sinus arrest, and sinoatrial exit block. Sinus pause and arrest involve slowing or arrest of automatic impulse generation from the sinus node. This can lead to asystole, or cardiac arrest, if ventricular escape rhythms do not engage to create backup sources of cardiac action potentials.[7]
Sinoatrial exit block is a similar non-respiratory phenomenon of temporarily lost sinoatrial impulses. However, in contrast to a sinus pause, the action potential is still generated at the SA node, but is either unable to leave or delayed from leaving the node, preventing or delaying atrial depolariziation and subsequent ventricular systole. Therefore, the length of the pause in heart beats is usually a multiple of the P-P interval as seen on electrocardiography. Like a sinus pause, sinoatrial exit block can be symptomatic, especially with prolonged pause length.[7]
Un síndrome de enfermedad intrínseca del nodo sinusal, denominado síndrome del seno enfermo o disfunción del nodo sinusal , cubre afecciones que incluyen bradicardia sinusal sintomática o incompetencia cronotrópica persistente, bloqueo sinoauricular , paro sinusal y síndrome de taquicardia-bradicardia. [7] Estas afecciones pueden ser causadas por daño al propio nódulo sinusal nativo y con frecuencia van acompañadas de daño en la conducción del nódulo AV y reducción de la actividad del marcapasos de respaldo. [18] La afección también puede ser causada por una disfunción del sistema nervioso autónomo que regula el ganglio y comúnmente se exacerba con medicamentos. [7]
La bradicardia también puede deberse a la inhibición del flujo de potenciales de acción a través del nódulo auriculoventricular (AV). Si bien esto puede ser normal en pacientes jóvenes debido al tono excesivo del nervio vago, la bradicardia sintomática debida a la disfunción del nódulo AV en personas mayores suele deberse a una enfermedad cardíaca estructural, isquemia miocárdica o fibrosis relacionada con la edad. [19]
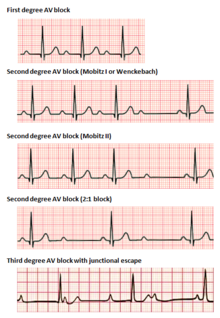
Los bloqueos auriculoventriculares se dividen en 3 categorías, clasificadas según su gravedad. El bloqueo AV se diagnostica mediante ECG de superficie, que suele ser suficiente para localizar la lesión causal del bloqueo, sin necesidad de un estudio electrofisiológico invasivo . [7]
En el bloqueo AV de primer grado , los impulsos eléctricos que se originan en el nódulo SA (u otro foco ectópico encima de los ventrículos) se conducen con un retraso significativo a través del nódulo AV. Esta afección se diagnostica mediante ECG, con intervalos PR superiores a 200 milisegundos. [7] El intervalo PR representa el período de tiempo entre el inicio de la despolarización auricular y el inicio de la despolarización ventricular, lo que representa el flujo de impulsos eléctricos entre los nodos SA y AV. A pesar del término "bloqueo", en esta conducción ningún impulso se pierde por completo, sino que simplemente se retrasa. La ubicación de la lesión causal puede estar en cualquier lugar entre el nodo AV y el sistema His-Purkinje, pero se encuentra más comúnmente en el propio nodo AV. [20] Generalmente, la prolongación aislada del PR en el bloqueo AV de primer grado no se asocia con un aumento de la mortalidad u hospitalización. [21]
El bloqueo AV de segundo grado se caracteriza por una pérdida intermitente de la conducción de impulsos entre el nódulo SA y los ventrículos. Bloqueo de 2º grado, se clasifica en dos tipos. El bloqueo de Mobitz tipo 1, también conocido con el epónimo Wenckebach , demuestra clásicamente patrones agrupados de latidos cardíacos en el ECG. A lo largo del grupo, el intervalo PR se alarga gradualmente, hasta que se produce una caída de la conducción, lo que da como resultado que no se observe complejo QRS en el ECG de superficie después de la última onda P. Después de un retraso, la agrupación se repite, y el intervalo PR se acorta nuevamente hasta el valor inicial. [22] El bloqueo AV de segundo grado tipo 1 debido a una enfermedad en el nódulo AV (a diferencia del sistema de His-Purkinje) rara vez necesita intervención con implantación de marcapasos. [22]
El bloqueo AV de segundo grado, Mobitz tipo 2, es otro fenómeno de caída intermitente de complejos QRS después de agrupaciones características de latidos que se observan en el ECG de superficie. En esta condición, los intervalos PR y RR son consistentes, seguidos de un bloqueo AV repentino y una caída del complejo QRS. [22] Debido a que los bloqueos tipo 2 generalmente se deben a lesiones debajo del nodo AV, la capacidad de los ritmos de escape ventriculares para mantener el gasto cardíaco se ve comprometida. A menudo se requiere la implantación de un marcapasos permanente. [19]
Un ritmo de la unión AV , o bradicardia del nodo auriculoventricular, generalmente es causado por la ausencia del impulso eléctrico del nodo sinusal . Esto suele aparecer en un electrocardiograma con un complejo QRS normal acompañado de una onda P invertida antes, durante o después del complejo QRS. [17]
Un latido de escape de la unión AV es un latido cardíaco retrasado que se origina a partir de un foco ectópico en algún lugar de la unión AV. Ocurre cuando la tasa de despolarización del nodo SA cae por debajo de la tasa del nodo AV . [17] Esta arritmia también puede ocurrir cuando los impulsos eléctricos del nódulo SA no logran llegar al nódulo AV debido a un bloqueo SA o AV. [23] Este es un mecanismo de protección para que el corazón compense un nódulo SA que ya no maneja la actividad del marcapasos y es uno de una serie de sitios de respaldo que pueden asumir la función del marcapasos cuando el nódulo SA no lo hace. Esto se presentaría con un intervalo PR más largo . Un complejo de escape de la unión AV es una respuesta normal que puede resultar de un tono vagal excesivo en el nódulo SA. Las causas patológicas incluyen bradicardia sinusal, paro sinusal, bloqueo de salida sinusal o bloqueo AV. [17]
El ritmo idioventricular , también conocido como bradicardia auriculoventricular o ritmo de escape ventricular, es una frecuencia cardíaca inferior a 50 BPM. Este es un mecanismo de seguridad cuando se produce una falta de impulso eléctrico o estímulos de la aurícula . [17] Los impulsos que se originan dentro o debajo del haz de His en el nodo AV producirán un complejo QRS ancho con frecuencias cardíacas entre 20 y 40 BPM. Los que están por encima del haz de His, también conocido como de unión, normalmente oscilarán entre 40 y 60 BPM con un complejo QRS estrecho. [24] [25] En un bloqueo cardíaco de tercer grado , alrededor del 61 % tiene lugar en la rama del haz de His-sistema de Purkinje, el 21 % en el nódulo AV y el 15 % en el haz de His. [25] El bloqueo AV se puede descartar con un ECG que indique "una relación 1:1 entre las ondas P y los complejos QRS". [24] Las bradicardias ventriculares ocurren con bradicardia sinusal, paro sinusal y bloqueo AV. El tratamiento suele consistir en la administración de atropina y estimulación cardíaca . [17]
Para los bebés, la bradicardia se define como una frecuencia cardíaca inferior a 100 BPM (lo normal es entre 120 y 160 BPM). Los bebés prematuros tienen más probabilidades que los bebés nacidos a término de sufrir episodios de apnea y bradicardia; su causa no se comprende claramente. Los hechizos pueden estar relacionados con centros dentro del cerebro que regulan la respiración y que pueden no estar completamente desarrollados. Tocar al bebé suavemente o balancear ligeramente la incubadora casi siempre hará que el bebé comience a respirar nuevamente, lo que aumentará su frecuencia cardíaca. La práctica estándar de la unidad de cuidados intensivos neonatales es monitorear electrónicamente el corazón y los pulmones. [ cita necesaria ]
La bradicardia arritmia puede tener muchas causas, tanto cardíacas como no cardíacas.
Las causas no cardíacas suelen ser secundarias y pueden implicar uso o abuso de drogas recreativas , problemas metabólicos o endocrinos, especialmente hipotiroidismo , desequilibrio electrolítico , factores neurológicos, reflejos autónomos , factores situacionales, como reposo prolongado en cama y autoinmunidad . [26] En reposo, aunque la taquicardia se observa más comúnmente en los trastornos de oxidación de ácidos grasos , más raramente puede ocurrir bradicardia aguda. [27]
Las causas cardíacas incluyen cardiopatía isquémica aguda o crónica , cardiopatía vascular, valvulopatía o enfermedad eléctrica primaria degenerativa. En definitiva, las causas actúan mediante tres mecanismos: automatismo deprimido del corazón, bloqueo de la conducción o escape de marcapasos y ritmos. [28]
En general, dos tipos de problemas provocan bradicardias: trastornos del nódulo SA y trastornos del nódulo AV. [29]
Con la disfunción del nódulo SA (a veces llamada síndrome del seno enfermo), puede haber un automatismo desordenado o una conducción deficiente del impulso desde el nódulo SA hacia el tejido auricular circundante (un "bloqueo de salida"). Los bloqueos sinoauriculares de segundo grado sólo pueden detectarse mediante el uso de un ECG de 12 derivaciones. [30] Es difícil y a veces imposible asignar un mecanismo a cualquier bradicardia en particular, pero el mecanismo subyacente no es clínicamente relevante para el tratamiento, que es el mismo en ambos casos de síndrome del seno enfermo: un marcapasos permanente . [28]
Las alteraciones de la conducción AV (bloqueo AV; bloqueo AV primario , bloqueo AV secundario tipo I , bloqueo AV secundario tipo II , bloqueo AV terciario ) pueden deberse a una conducción alterada en el nódulo AV o en cualquier lugar debajo de él, como en el haz de His. La relevancia clínica de los bloqueos AV es mayor que la de los bloqueos SA. [30]
Los medicamentos betabloqueantes también pueden disminuir la frecuencia cardíaca y disminuir la fuerza con la que se contrae el corazón. Los betabloqueantes pueden disminuir la frecuencia cardíaca a un nivel peligroso si se recetan con medicamentos del tipo bloqueador de los canales de calcio . [31] La bradicardia también forma parte del reflejo de buceo de los mamíferos . [32]
El diagnóstico de bradicardia en adultos se basa en una frecuencia cardíaca inferior a 60 BPM, [1] aunque algunos estudios utilizan una frecuencia cardíaca inferior a 50 BPM. [33] Esto generalmente se determina mediante palpación o ECG. [1] Si se presentan síntomas, una determinación de electrolitos puede ser útil para determinar la causa subyacente. [31]
El tratamiento de la bradicardia depende de si la persona está estable o inestable. [1] [33]
No se necesita tratamiento de emergencia si la persona es asintomática o mínimamente sintomática. [33]
Si una persona está inestable, el tratamiento inicial recomendado es atropina intravenosa . [33] No se deben utilizar dosis inferiores a 0,5 mg, ya que esto puede disminuir aún más la tasa. [33] Si esto no es eficaz, se debe utilizar una infusión intravenosa de inotrópicos ( dopamina , epinefrina ) o estimulación transcutánea . [33] Es posible que se requiera estimulación transvenosa si la causa de la bradicardia no es rápidamente reversible. [33]
En los niños se recomienda administrar oxígeno, apoyar su respiración y realizar compresiones torácicas . [34] [35]
En la práctica clínica, las personas mayores de 65 años y los atletas jóvenes de ambos sexos pueden tener bradicardia sinusal. [1] Los Centros para el Control y la Prevención de Enfermedades de EE. UU . informaron en 2011 que el 15,2 % de los hombres adultos y el 6,9 % de las mujeres adultas tenían bradicardia clínicamente definida (una frecuencia del pulso en reposo inferior a 60 BPM). [36]