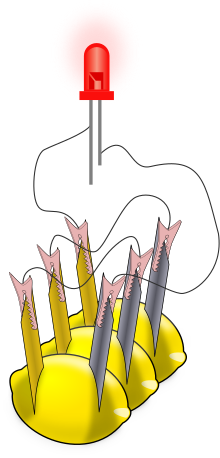
Una batería de limón es una batería simple que a menudo se fabrica con fines educativos. Por lo general, se inserta un trozo de metal de zinc (como un clavo galvanizado ) y un trozo de cobre (como una moneda de un centavo) en un limón y se conectan mediante cables. La energía generada por la reacción de los metales se utiliza para alimentar un pequeño dispositivo como un diodo emisor de luz (LED).
La batería de limón es similar a la primera batería eléctrica inventada en 1800 por Alessandro Volta , que utilizaba salmuera (agua salada) en lugar de jugo de limón. [1] La batería de limón ilustra el tipo de reacción química ( oxidación-reducción ) que ocurre en las baterías. [2] [3] [4] El zinc y el cobre se llaman electrodos , y el jugo del interior del limón se llama electrolito . Existen muchas variaciones de la celda de limón que utilizan diferentes frutas (o líquidos) como electrolitos y metales distintos del zinc y el cobre como electrodos.
Existen numerosos conjuntos de instrucciones para fabricar baterías de limón y para obtener componentes como diodos emisores de luz (LED), medidores eléctricos ( multímetros ) y clavos y tornillos zincados ( galvanizados ). [5] [6] Los kits científicos comerciales de "reloj de papa" incluyen electrodos y un reloj digital de bajo voltaje. Después de ensamblar una celda, se puede usar un multímetro para medir el voltaje o la corriente eléctrica de la celda voltaica; un voltaje típico es de 0,9 V con limones. Las corrientes son más variables, pero varían hasta aproximadamente 1 mA (cuanto mayores son las superficies del electrodo, mayor es la corriente). Para un efecto más visible, las celdas de limón se pueden conectar en serie para alimentar un LED (ver ilustración) u otros dispositivos. La conexión en serie aumenta el voltaje disponible para los dispositivos. Swartling y Morgan han publicado una lista de dispositivos de bajo voltaje junto con la cantidad correspondiente de celdas de limón que se necesitaban para alimentarlos; incluían LED, zumbadores piezoeléctricos y pequeños relojes digitales. Con los electrodos de zinc/cobre, se necesitaban al menos dos celdas de limón para cualquiera de estos dispositivos. [7] La sustitución del electrodo de zinc por un electrodo de magnesio genera una celda con un voltaje mayor (1,5-1,6 V), y una sola celda de magnesio/cobre alimentará algunos dispositivos. [7] Tenga en cuenta que las bombillas incandescentes de las linternas no se utilizan porque la batería de limón no está diseñada para producir suficiente corriente eléctrica para encenderlas. Una batería de este tipo normalmente produce 0,001 A (1 mA) de corriente con una diferencia de potencial de 0,7 V; Estos valores se multiplican para determinar la potencia total de 0,0007 W (0,7 mW).

Se pueden utilizar muchas frutas y líquidos como electrolito ácido. La fruta es conveniente porque proporciona electrolitos y una forma sencilla de sostener los electrodos. El ácido implicado en los cítricos (limones, naranjas, pomelos, etc.) es el ácido cítrico . La acidez, que se indica mediante el pH medido , varía sustancialmente.
Las patatas tienen ácido fosfórico y funcionan bien; son la base de los kits comerciales de "reloj de patatas". [8] [9] Se ha propuesto el uso de baterías de papa con iluminación LED en países pobres o en poblaciones fuera de la red. Una investigación internacional iniciada en 2010 demostró que hervir patatas durante ocho minutos mejora su producción eléctrica, al igual que colocar rodajas de patatas entre múltiples placas de cobre y zinc. Según investigadores de Sri Lanka, la médula (tallo) de plátano hervida y picada también es adecuada. [10]
En lugar de fruta se pueden utilizar líquidos en distintos recipientes. El vinagre doméstico ( ácido acético ) funciona bien. [11] El chucrut ( ácido láctico ) apareció en un episodio del programa de televisión estadounidense Head Rush (una rama del programa MythBusters ). El chucrut había sido enlatado y se convirtió en electrolito, mientras que la lata misma era uno de los electrodos. [12]
Los electrodos de zinc y cobre son razonablemente seguros y fáciles de obtener. También se pueden estudiar otros metales como plomo, hierro, magnesio, etc.; Producen voltajes diferentes a los del par zinc/cobre. En particular, los electrodos de magnesio/cobre pueden generar voltajes de hasta 1,6 V en celdas de limón. Este voltaje es mayor que el que se puede obtener usando celdas de zinc/cobre. Es comparable al de las baterías domésticas estándar (1,5 V), que resulta útil para alimentar dispositivos con una sola celda en lugar de utilizar celdas en serie. [7]
Para los alumnos más pequeños, de entre 5 y 9 años, el objetivo educativo es utilitario: [13] las baterías son dispositivos que pueden alimentar otros dispositivos, siempre que estén conectados mediante un material conductor. Las baterías son componentes de circuitos eléctricos; enganchar un solo cable entre una batería y una bombilla no alimentará la bombilla.
Para los niños de entre 10 y 13 años, las pilas se utilizan para ilustrar la conexión entre la química y la electricidad, así como para profundizar en el concepto de circuito de la electricidad. El hecho de que se utilicen diferentes elementos químicos como el cobre y el zinc puede situarse en el contexto más amplio de que los elementos no desaparecen ni se descomponen cuando sufren reacciones químicas.
Para los alumnos mayores y los estudiantes universitarios, las baterías sirven para ilustrar los principios de las reacciones de oxidación-reducción. [13] [14] Los estudiantes pueden descubrir que dos electrodos idénticos no producen voltaje y que diferentes pares de metales (más allá del cobre y el zinc) producen diferentes voltajes. Se pueden examinar los voltajes y corrientes de combinaciones en serie y en paralelo de las baterías. [15]
La corriente que sale de la batería a través de un medidor dependerá del tamaño de los electrodos, de qué tan lejos se insertan los electrodos en la fruta y qué tan cerca unos de otros están colocados; el voltaje es bastante independiente de estos detalles de los electrodos. [dieciséis]
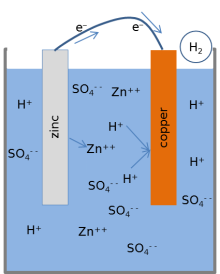
La mayoría de los libros de texto presentan el siguiente modelo para las reacciones químicas de una batería de limón. [1] [3] [17] Cuando la celda proporciona una corriente eléctrica a través de un circuito externo, el zinc metálico en la superficie del electrodo de zinc se disuelve en la solución. Los átomos de zinc se disuelven en el electrolito líquido como iones cargados eléctricamente (Zn 2+ ), dejando 2 electrones cargados negativamente (e − ) en el metal:
Esta reacción se llama oxidación . Mientras el zinc ingresa al electrolito, dos iones de hidrógeno cargados positivamente (H + ) del electrolito se combinan con dos electrones en la superficie del electrodo de cobre y forman una molécula de hidrógeno sin carga (H 2 ):
Esta reacción se llama reducción. Los electrones utilizados en el cobre para formar las moléculas de hidrógeno se transfieren desde el zinc a través de un cable externo que conecta el cobre y el zinc. Las moléculas de hidrógeno formadas en la superficie del cobre por la reacción de reducción finalmente burbujean como gas hidrógeno.
Este modelo de reacciones químicas hace varias predicciones que fueron examinadas en experimentos publicados por Jerry Goodisman en 2001. Goodisman señala que numerosos autores recientes proponen reacciones químicas para la batería de limón que implican la disolución del electrodo de cobre en el electrolito. Goodisman excluye esta reacción por ser inconsistente con los experimentos y señala que la química correcta, que implica la evolución de hidrógeno en el electrodo de cobre pero también puede usar plata en lugar de cobre, se conoce desde hace muchos años. [4] La mayoría de las predicciones detalladas del modelo se aplican al voltaje de la batería que se mide directamente con un medidor en circuito abierto (no hay nada más conectado a la batería). Cuando se modificó el electrolito añadiendo sulfato de zinc (ZnSO 4 ), el voltaje de la celda se redujo como se predijo usando la ecuación de Nernst para el modelo. La ecuación de Nernst esencialmente dice cuánto cae el voltaje a medida que se agrega más sulfato de zinc. La adición de sulfato de cobre (CuSO 4 ) no afectó el voltaje. Este resultado es consistente con el hecho de que los átomos de cobre del electrodo no participan en el modelo de reacción química de la celda.
Cuando la batería está conectada a un circuito externo y fluye una corriente eléctrica significativa, el electrodo de zinc pierde masa, como lo predice la reacción de oxidación del zinc anterior. De manera similar, el gas hidrógeno se desprende en forma de burbujas del electrodo de cobre. Finalmente, el voltaje de la celda dependía de la acidez del electrolito, medida por su pH; La disminución de la acidez (y el aumento del pH) hace que el voltaje caiga. Este efecto también lo predice la ecuación de Nernst; el ácido particular que se utilizó (cítrico, clorhídrico, sulfúrico, etc.) no afecta el voltaje excepto a través del valor del pH.
La predicción de la ecuación de Nernst falló para electrolitos fuertemente ácidos (pH < 3,4), cuando el electrodo de zinc se disuelve en el electrolito incluso cuando la batería no proporciona corriente a un circuito. Las dos reacciones de oxidación-reducción enumeradas anteriormente solo ocurren cuando se puede transportar carga eléctrica a través del circuito externo. La reacción adicional en circuito abierto se puede observar mediante la formación de burbujas en el electrodo de zinc en circuito abierto. Este efecto finalmente limitó el voltaje de las celdas a 1,0 V cerca de la temperatura ambiente en los niveles más altos de acidez.
La energía proviene del cambio químico en el zinc cuando se disuelve en el ácido. La energía no proviene del limón ni de la patata. El zinc se oxida en el interior del limón, intercambiando algunos de sus electrones con el ácido para alcanzar un estado energético más bajo, y la energía liberada proporciona la energía. [4]
En la práctica actual, el zinc se produce mediante electroobtención de sulfato de zinc o reducción pirometalúrgica de zinc con carbono, lo que requiere un aporte de energía. La energía producida en la batería de limón proviene de revertir esta reacción, recuperando parte de la energía aportada durante la producción de zinc.
Desde 1840 hasta finales del siglo XIX, se utilizaron ampliamente en la industria de la impresión grandes celdas voltaicas que utilizaban un electrodo de zinc y un electrolito de ácido sulfúrico . Si bien a veces se usaban electrodos de cobre como los de las baterías de limón, en 1840 Alfred Smee inventó una versión refinada de esta celda que usaba plata con una capa rugosa de platino en lugar de un electrodo de cobre. [18] [19] El gas hidrógeno adherido a la superficie de un electrodo de plata o cobre reduce la corriente eléctrica que se puede extraer de una celda; El fenómeno se llama "polarización". [17] [20] La superficie rugosa y "platinizada" acelera el burbujeo del gas hidrógeno y aumenta la corriente de la celda. A diferencia del electrodo de zinc, los electrodos de cobre o plata platinada no se consumen con el uso de la batería y los detalles de este electrodo no afectan el voltaje de la celda. La celda de Smee era conveniente para la electrotipificación , que producía placas de cobre para la impresión tipográfica de periódicos y libros, así como estatuas y otros objetos metálicos. [19] [21] [22] [23] [24]
La celda de Smee utilizó zinc amalgamado en lugar de zinc puro; la superficie del zinc amalgamado ha sido tratada con mercurio . [23] Aparentemente, el zinc amalgamado era menos propenso a la degradación por una solución ácida que el zinc puro. [25] Los electrodos de zinc amalgamado y de zinc simple dan esencialmente el mismo voltaje cuando el zinc es puro. [26] Con el zinc imperfectamente refinado en los laboratorios del siglo XIX, normalmente daban diferentes voltajes. [25]
Antiguamente, una batería galvánica era una máquina estupenda y costosa que ocupaba un gran espacio y costaba una suma considerable mantenerla en su corta duración de acción.
Ahora se puede fabricar un instrumento mucho más potente en una tabaquera y llevarlo en el bolsillo.
Estas observaciones nos las imponen las asombrosas baterías de platino del Sr. Grove y las baterías químico-mecánicas inventadas por el Sr. Smee...
La primera mejora real con respecto a la simple celda de zinc-cobre en ácido se debió al Dr. Alfred Smee, quien notó que el gas hidrógeno liberado en la placa negativa se desprendía de ella mucho más fácilmente, por lo que la polarización tenía lugar mucho menos rápidamente si la superficie de esta placa estaba rugosa en lugar de ser bastante lisa;
y el medio que encontró más eficiente fue el de recubrir la lámina o láminas de plata con platino finamente dividido...
De la aplicación de esta celda se puede disponer una modificación muy importante, convirtiéndola en una
batería
ÁCIDA , análoga a la plata platinada del Sr. Smee.
Aquellos que están familiarizados con el ingenioso dispositivo de ese caballero, saben que la característica de su disposición es que la placa negativa, donde se libera el hidrógeno, se desprenderá de este hidrógeno muy fácilmente.
En circunstancias normales, el hidrógeno se adhiere mucho a las placas de una batería ácida y, por su presencia en sus superficies, deja fuera de acción una parte considerable de las placas.
Para remediar esto, ha "platinizado", como él mismo dice, las superficies.
En 1840, Smee inventó una batería que hizo posible comercialmente la electrotipificación.
... Quizás uno de los mayores avances en relación con la electrotipificación se dio cuando se inventó la dinamo de revestimiento.
La primera adopción de una dinamo, en lugar de la batería tipo Smee, fue por Leslie, de Nueva York, en 1872.Cartilla para aprendices de la industria gráfica. Buena y breve introducción a la historia de la electrotipificación.
La celda de Smee es la celda más comúnmente empleada debido a su extrema simplicidad de construcción y gestión.Una discusión detallada de la construcción y mantenimiento de las celdas Smee, c. 1874.
Se realizaron algunos encargos importantísimos en electrotipos, como los "bronces" que adornan la Ópera de París y la estatua de 320 cm de altura del Príncipe Alberto y cuatro figuras que lo acompañan, erigida detrás del Albert Hall de Londres como monumento a la Gran Exposición. de 1851.
La singular propiedad que posee el zinc amalgamado de no ser atacado por el ácido sulfúrico diluido en agua se debe a la adhesión del hidrógeno sobre la placa en la solución ácida.