La reacción de ciclización de Nazarov (a menudo denominada simplemente ciclización de Nazarov ) es una reacción química utilizada en química orgánica para la síntesis de ciclopentenonas . La reacción se divide típicamente en variantes clásicas y modernas , dependiendo de los reactivos y sustratos empleados. Fue descubierta originalmente por Ivan Nikolaevich Nazarov (1906-1957) en 1941 mientras estudiaba los reordenamientos de las alilvinilcetonas. [1]

Como se describió originalmente, la ciclización de Nazarov implica la activación de una divinilcetona utilizando un promotor de ácido Lewis estequiométrico o ácido prótico . El paso clave del mecanismo de reacción implica un cierre de anillo electrocíclico 4π- catiónico que forma el producto ciclopentenona (ver Mecanismo a continuación). A medida que se ha desarrollado la reacción, las variantes que involucran sustratos distintos de las divinilcetonas y promotores distintos de los ácidos Lewis se han incluido bajo el nombre de ciclización de Nazarov, siempre que sigan una vía mecanística similar .
El éxito de la ciclización de Nazarov como herramienta en la síntesis orgánica se debe a la utilidad y ubicuidad de las ciclopentenonas como motivos en productos naturales (incluida la jasmona , las aflatoxinas y una subclase de prostaglandinas ) y como intermediarios sintéticos útiles para la síntesis total . La reacción se ha utilizado en varias síntesis totales y se han publicado varias revisiones. [2] [3] [4] [5] [6] [7]
El mecanismo de la reacción clásica de ciclización de Nazarov fue demostrado experimentalmente por primera vez por Charles Shoppee como una electrociclación intramolecular y se describe a continuación. La activación de la cetona por el catalizador ácido genera un catión pentadienilo , que experimenta una electrociclación conrotatoria 4π permitida térmicamente según lo dictan las reglas de Woodward-Hoffman . Esto genera un catión oxialilo que experimenta una reacción de eliminación para perder un β-hidrógeno. La tautomerización posterior del enolato produce el producto ciclopentenona. [8] [9]

Como se señaló anteriormente, se conocen variantes que se desvían de esta plantilla; lo que designa una ciclización de Nazarov en particular es la generación del catión pentadienilo seguida del cierre del anillo electrocíclico a un catión oxialilo. Para lograr esta transformación, la molécula debe estar en la conformación s-trans/s-trans , colocando los grupos vinilo en una orientación apropiada. La propensión del sistema a entrar en esta conformación influye drásticamente en la velocidad de reacción , con sustratos α-sustituidos que tienen una mayor población del confórmero requerido debido a la tensión alílica . La coordinación de un sustituyente α donador de electrones por el catalizador también puede aumentar la velocidad de reacción al imponer esta conformación. [2]
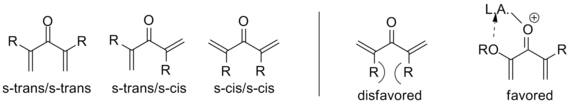
De manera similar, la β-sustitución dirigida hacia adentro restringe la conformación s-trans tan severamente que se ha demostrado que la isomerización EZ ocurre antes de la ciclización en una amplia gama de sustratos, produciendo la ciclopentenona trans independientemente de la configuración inicial. De esta manera, la ciclización de Nazarov es un ejemplo raro de una reacción pericíclica estereoselectiva , mientras que la mayoría de las electrociclaciones son estereoespecíficas . El ejemplo siguiente utiliza trietilsilano para atrapar el catión oxialilo de modo que no se produzca eliminación. [2] (Ver ciclizaciones interrumpidas a continuación)

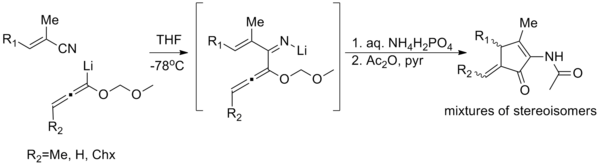
En esta misma línea, las cetonas de vinilo alenílico del tipo estudiado extensamente por Marcus Tius de la Universidad de Hawai muestran una aceleración dramática de la velocidad debido a la eliminación de β-hidrógenos, lo que evita una gran cantidad de tensión estérica en el confórmero s-cis. [6]

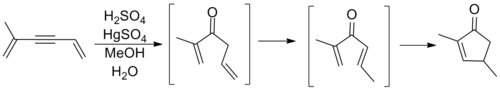
Aunque ya se habían observado ciclizaciones que seguían el patrón general anterior antes de la participación de Nazarov, fue su estudio de los reordenamientos de las cetonas de vinilo alílico lo que marcó el primer examen importante de este proceso. Nazarov razonó correctamente que la olefina alílica se isomerizaba in situ para formar una cetona divinílica antes del cierre del anillo para formar el producto ciclopentenona. La reacción que se muestra a continuación implica una reacción de oximercuración de alquino para generar la cetona requerida. [10]
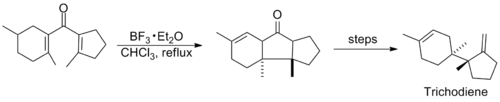
La investigación relacionada con esta reacción fue relativamente tranquila en los años siguientes, hasta que a mediados de la década de 1980 se publicaron varias síntesis que empleaban la ciclización de Nazarov. A continuación se muestran los pasos clave en las síntesis de tricodieno y nor-esterepolida, la última de las cuales se cree que se produce a través de una isomerización inusual de alquino - aleno que genera la divinilcetona. [11] [12]

La versión clásica de la ciclización de Nazarov presenta varios inconvenientes que las variantes modernas intentan evitar. Los dos primeros no son evidentes a partir del mecanismo por sí solo, pero son indicativos de las barreras a la ciclización; los tres últimos se derivan de problemas de selectividad relacionados con la eliminación y protonación del intermediario. [2]

Las deficiencias señaladas anteriormente limitan la utilidad de la reacción de ciclización de Nazarov en su forma canónica. Sin embargo, las modificaciones de la reacción enfocadas en remediar sus problemas siguen siendo un área activa de investigación académica . En particular, la investigación se ha centrado en algunas áreas clave: hacer que la reacción sea catalítica en el promotor, efectuar la reacción con promotores más suaves para mejorar la tolerancia del grupo funcional , dirigir la regioselectividad del paso de eliminación y mejorar la estereoselectividad general . Estas han tenido éxito en diversos grados.
Además, se han realizado modificaciones que se han centrado en alterar el progreso de la reacción, ya sea generando el catión pentadienilo de una manera poco ortodoxa o "interceptando" el catión oxialilo de diversas maneras. Además, se han desarrollado variantes enantioselectivas de diversos tipos. La gran cantidad de literatura sobre el tema impide un examen exhaustivo de este campo; a continuación se ofrecen algunos ejemplos clave.
Los primeros esfuerzos para mejorar la selectividad de la ciclización de Nazarov aprovecharon el efecto del silicio β para dirigir la regioselectividad del paso de eliminación. Esta química fue desarrollada más extensamente por el Profesor Scott Denmark de la Universidad de Illinois, Urbana-Champaign a mediados de la década de 1980 y utiliza cantidades estequiométricas de tricloruro de hierro para promover la reacción. Con productos bicíclicos , el isómero cis fue seleccionado en diversos grados. [13]

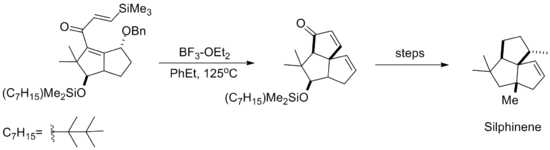
La reacción de ciclización de Nazarov dirigida por silicio se empleó posteriormente en la síntesis del producto natural Silphinene, que se muestra a continuación. La ciclización tiene lugar antes de la eliminación de la fracción de alcohol bencílico , de modo que la estereoquímica resultante del anillo recién formado surge de la aproximación del anti alqueno de sililo al éter. [10]
Basándose en los efectos de los sustituyentes recopilados en varios ensayos de la reacción, la profesora Alison Frontier de la Universidad de Rochester desarrolló un paradigma para las ciclizaciones de Nazarov "polarizadas" en las que se utilizan grupos donantes y aceptores de electrones para mejorar la selectividad general de la reacción. La creación de un nucleófilo vinílico eficaz y un electrófilo vinílico en el sustrato permite la activación catalítica con triflato de cobre y la eliminación regioselectiva. Además, el grupo aceptor de electrones aumenta la acidez del protón α, lo que permite la formación selectiva del epímero trans-α a través del equilibrio. [14]
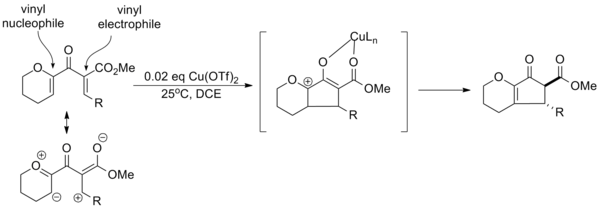
A menudo es posible lograr la activación catalítica utilizando solo un grupo donante o retractor, aunque la eficiencia de la reacción (rendimiento, tiempo de reacción, etc.) suele ser menor.
Por extensión, cualquier catión pentadienilo, independientemente de su origen, es capaz de sufrir una ciclización de Nazarov. Se han publicado numerosos ejemplos en los que se llega al catión requerido mediante una variedad de reordenamientos. [2] Uno de estos ejemplos implica la apertura del anillo catiónico de los ciclopropanos dicloroalílicos catalizada por plata. La sal de plata facilita la pérdida de cloruro a través de la precipitación de cloruro de plata insoluble . [15]
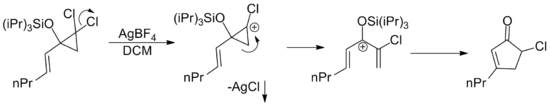
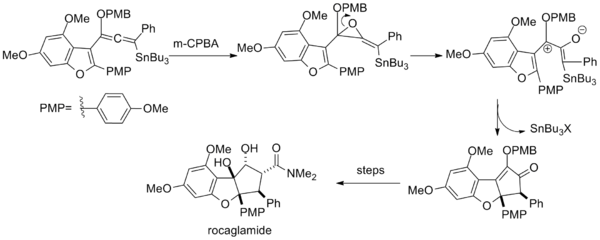
En la síntesis total de rocaglamida, la epoxidación de un estannano de vinil alcoxialenilo también genera un catión pentadienilo a través de la apertura del anillo del epóxido resultante . [16]
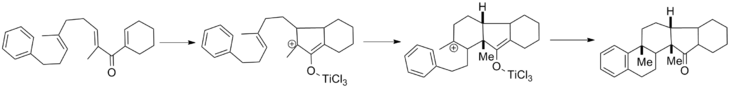
Una vez que se ha producido la ciclización, se forma un catión oxialilo. Como se ha comentado ampliamente anteriormente, el curso típico de este intermedio es la eliminación seguida de la tautomerización del enolato . Sin embargo, estos dos pasos pueden ser interrumpidos por varios nucleófilos y electrófilos , respectivamente. El atrapamiento del catión oxialilo ha sido desarrollado ampliamente por Fredrick G. West de la Universidad de Alberta y su revisión cubre el campo. [17] El catión oxialilo puede ser atrapado con nucleófilos heteroátomos y carbonosos y también puede sufrir cicloadiciones catiónicas con varios socios anclados. A continuación se muestra una reacción en cascada en la que el atrapamiento sucesivo de cationes genera un núcleo pentacíclico en un solo paso con diastereoselectividad completa . [18]
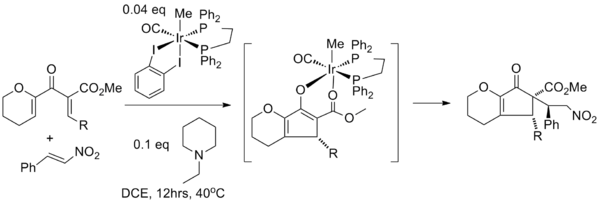
La captura de enolato con varios electrófilos es decididamente menos común. En un estudio, la ciclización de Nazarov se combina con una reacción de Michael que utiliza un catalizador de iridio para iniciar la adición conjugada nucleofílica del enolato al β-nitrostireno . En esta reacción en tándem, el catalizador de iridio es necesario para ambas conversiones: actúa como el ácido de Lewis en la ciclización de Nazarov y en el siguiente paso, el grupo nitro del nitrostireno se coordina primero con el iridio en un intercambio de ligando con el átomo de oxígeno del éster carbonílico antes de que tenga lugar la adición de Michael real a la cara opuesta del grupo R. [19]
El desarrollo de una ciclización de Nazarov enantioselectiva es una adición deseable al repertorio de reacciones de ciclización de Nazarov. Con ese fin, se han desarrollado varias variaciones que utilizan auxiliares quirales y catalizadores quirales . También se conocen ciclizaciones diastereoselectivas , en las que los estereocentros existentes dirigen la ciclización. Casi todos los intentos se basan en la idea de la torquoselectividad ; la selección de una dirección para que los grupos vinilo "roten" a su vez establece la estereoquímica como se muestra a continuación. [2]

Las ciclizaciones de Nazarov dirigidas por silicio pueden exhibir diastereoselectividad inducida de esta manera. En el ejemplo siguiente, el grupo sililo actúa para dirigir la ciclización al evitar que el alqueno distante rote "hacia" él a través de una interacción estérica desfavorable . De esta manera, el silicio actúa como un auxiliar sin trazas . (El material de partida no es enantiopuro, pero la retención del exceso enantiomérico sugiere que el auxiliar dirige la ciclización). [2]

Los sustratos alenílicos de Tius pueden exhibir transferencia de quiralidad axial a tetraédrica si se utilizan alenos enantiopuros. El ejemplo siguiente genera un diosfenpol quiral con un rendimiento del 64 % y un exceso enantiomérico del 95 % . [2]

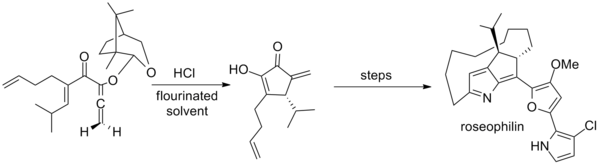
Tius ha desarrollado además un auxiliar basado en alcanfor para alenos aquirales que se empleó en la primera síntesis asimétrica de roseofilina . El paso clave emplea una mezcla inusual de hexafluoro-2-propanol y trifluoroetanol como disolvente. [2] [20]
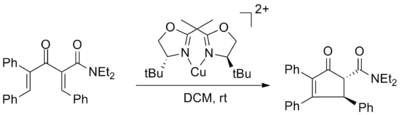
El primer ácido de Lewis quiral que promovió la ciclización asimétrica de Nazarov fue reportado por Varinder Aggarwal y utilizó complejos de ligando de cobre (II) bisoxazolina con hasta un 98% ee. El exceso enantiomérico no se vio afectado por el uso de 50% molar del complejo de cobre, pero el rendimiento disminuyó significativamente. [2]
Las extensiones de la ciclización de Nazarov generalmente también se incluyen bajo el mismo nombre. Por ejemplo, una cetona insaturada α-β, γ-δ puede experimentar una ciclización conrotatoria catiónica similar que normalmente se conoce como reacción de ciclización iso-Nazarov . [21] Otras extensiones similares han recibido nombres similares, incluidas las ciclizaciones homo -Nazarov y las ciclizaciones vinílogas de Nazarov. [22] [23]
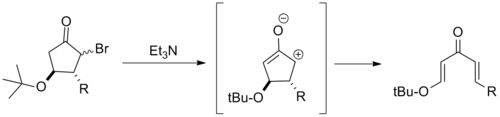
Debido a que sobreestabilizan el catión pentadienilo, los sustituyentes donantes de electrones β a menudo impiden gravemente la ciclización de Nazarov. A partir de esto, se han descrito varias aperturas de anillos electrocíclicos de β-alcoxiciclopentanos. Estas reacciones se conocen normalmente como reacciones de retrociclación de Nazarov . [2]
Los análogos nitrogenados de la reacción de ciclización de Nazarov (conocidas como reacciones de ciclización de imino-Nazarov ) tienen pocos ejemplos; hay un ejemplo de una ciclización de imino-Nazarov generalizada reportada (mostrada a continuación), [24] y varias reacciones de iso-imino-Nazarov en la literatura. [25] [26] Incluso estas tienden a sufrir de una estereoselectividad pobre, bajos rendimientos o alcance limitado. La dificultad surge de la sobreestabilización relativa del catión pentadienilo por donación de electrones, lo que impide la ciclización. [27]
{{citation}}: Falta o está vacío |title=( ayuda )