En la química de los carbohidratos , un par de anómeros (del griego ἄνω 'arriba, encima' y μέρος 'parte') es un par de estereoisómeros o diastereoisómeros casi idénticos que difieren solo en el carbono anomérico , el átomo de carbono que lleva el grupo funcional aldehído o cetona en la forma de cadena abierta del azúcar . Sin embargo, para que existan anómeros, el azúcar debe estar en su forma cíclica , ya que en forma de cadena abierta, el átomo de carbono anomérico es plano y, por lo tanto, aquiral . Dicho de manera más formal, un anómero es un epímero en el átomo de carbono hemiacetal/hemicetal en un sacárido cíclico . [1] La anomerización es el proceso de conversión de un anómero en otro. Como es típico de los compuestos estereoisoméricos, los diferentes anómeros tienen diferentes propiedades físicas, puntos de fusión y rotaciones específicas .
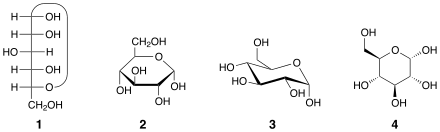
Cada dos anómeros se designan alfa (α) o beta (β), según la relación configuracional entre el centro anomérico y el átomo de referencia anomérico , por lo tanto, son estereodescriptores relativos . [2] El centro anomérico en los hemiacetales es el carbono anomérico C-1; en los hemicetales, es el carbono derivado del carbonilo de la cetona (por ejemplo, C-2 en D -fructosa). En las aldohexosas, el átomo de referencia anomérico es el estereocentro más alejado del carbono anomérico en el anillo (el átomo configuracional, que define el azúcar como D o L ). Por ejemplo, en la α- D -glucopiranosa, el átomo de referencia es C-5.
Si en la proyección cíclica de Fischer [3] el átomo de oxígeno exocíclico en el centro anomérico está en cis (en el mismo lado) con respecto al oxígeno exocíclico unido al átomo de referencia anomérico (en el grupo OH), el anómero es α. Si los dos oxígenos están en trans (en lados diferentes), el anómero es β. [4] Por lo tanto, las configuraciones absolutas del carbono anomérico y del átomo de referencia son las mismas (ambos R o ambos S ) en el anómero α y opuestas (uno R y el otro S ) en el anómero β. [5]
La anomerización es el proceso de conversión de un anómero en otro. En el caso de los azúcares reductores , la anomerización se denomina mutarrotación y se produce fácilmente en solución y está catalizada por un ácido y una base. Este proceso reversible suele dar lugar a una mezcla anomérica en la que, finalmente, se alcanza un equilibrio entre los dos anómeros individuales.
La proporción de los dos anómeros es específica para el azúcar en cuestión. Por ejemplo, independientemente de la configuración de la D -glucosa de partida, una solución se convertirá gradualmente en una mezcla de aproximadamente un 64% de β- D -glucopiranósido y un 36% de α- D -glucopiranósido. A medida que cambia la proporción, cambia la rotación óptica de la mezcla; este fenómeno se denomina mutarrotación .


Aunque las formas cíclicas de los azúcares suelen ser las más favorecidas, los hemiacetales en solución acuosa están en equilibrio con sus formas de cadena abierta . En las aldohexosas, este equilibrio se establece cuando el enlace hemiacetal entre C-1 (el carbono unido a dos oxígenos) y el oxígeno C-5 se escinde (formando el compuesto de cadena abierta) y se reforma (formando el compuesto cíclico). Cuando se reforma el grupo hemiacetal , el grupo OH en C-5 puede atacar a cualquiera de los dos lados estereoquímicamente distintos del grupo aldehído en C-1. El lado al que ataca determina si se forma el anómero α o β.
La anomerización de los glicósidos ocurre típicamente en condiciones ácidas. Normalmente, la anomerización ocurre a través de la protonación del oxígeno del acetal exocíclico, la ionización para formar un ion oxocarbenio con liberación de un alcohol y el ataque nucleofílico por parte de un alcohol en la cara inversa del ion oxocarbenio, seguido de la desprotonación.
Los anómeros tienen estructuras diferentes y, por lo tanto, tienen diferentes efectos estabilizadores y desestabilizadores entre sí. Los principales factores que contribuyen a la estabilidad de un determinado anómero son:
En el caso del D -glucopiranósido, el anómero β es el más estable en agua. En el caso de la D -manopiranosa , el anómero α es el más estable.
Debido a que los anómeros son diastereómeros entre sí, a menudo difieren en sus propiedades físicas y químicas. Una de las propiedades físicas más importantes que se utilizan para estudiar los anómeros es la rotación específica , que se puede controlar mediante polarimetría .