
Un líquido es un fluido casi incompresible que se adapta a la forma del recipiente que lo contiene pero que conserva un volumen casi constante independientemente de la presión. Es uno de los cuatro estados fundamentales de la materia (los otros son el sólido , el gas y el plasma ) y es el único estado con un volumen definido pero sin una forma fija.
La densidad de un líquido suele ser cercana a la de un sólido y mucho mayor que la de un gas. Por lo tanto, tanto a los líquidos como a los sólidos se les denomina materia condensada . Por otro lado, como los líquidos y los gases comparten la capacidad de fluir, a ambos se les denomina fluidos.
Un líquido está formado por diminutas partículas de materia vibrantes, como átomos, unidas por enlaces intermoleculares . Al igual que un gas, un líquido puede fluir y adoptar la forma de un recipiente. A diferencia de un gas, un líquido mantiene una densidad bastante constante y no se dispersa para llenar todo el espacio de un recipiente.
Aunque el agua líquida es abundante en la Tierra, este estado de la materia es en realidad el menos común en el universo conocido, porque los líquidos requieren un rango de temperatura y presión relativamente estrecho para existir. La mayor parte de la materia conocida en el universo es gas (como nubes interestelares ) o plasma (como estrellas ).

El líquido es uno de los cuatro estados primarios de la materia , junto con el sólido, el gas y el plasma . Un líquido es un fluido . A diferencia de un sólido, las moléculas de un líquido tienen mucha más libertad para moverse. Las fuerzas que unen las moléculas en un sólido son solo temporales en un líquido, lo que permite que un líquido fluya mientras que un sólido permanece rígido.
Un líquido, al igual que un gas, muestra las propiedades de un fluido. Un líquido puede fluir, adoptar la forma de un recipiente y, si se coloca en un recipiente sellado, distribuirá la presión aplicada de manera uniforme a todas las superficies del recipiente. Si el líquido se coloca en una bolsa, se puede apretar para que adopte cualquier forma. A diferencia de un gas, un líquido es casi incompresible, lo que significa que ocupa un volumen casi constante en un amplio rango de presiones; generalmente no se expande para llenar el espacio disponible en un recipiente, sino que forma su propia superficie y no siempre puede mezclarse fácilmente con otro líquido. Estas propiedades hacen que un líquido sea adecuado para aplicaciones como la hidráulica .
Las partículas líquidas están unidas firmemente, pero no rígidamente. Pueden moverse libremente unas alrededor de otras, lo que da como resultado un grado limitado de movilidad de partículas. A medida que aumenta la temperatura, las mayores vibraciones de las moléculas hacen que las distancias entre ellas aumenten. Cuando un líquido alcanza su punto de ebullición , las fuerzas de cohesión que unen estrechamente a las moléculas se rompen y el líquido cambia a su estado gaseoso (a menos que se produzca un sobrecalentamiento ). Si se reduce la temperatura, las distancias entre las moléculas se reducen. Cuando el líquido alcanza su punto de congelación , las moléculas generalmente se bloquearán en un orden muy específico, llamado cristalización, y los enlaces entre ellas se vuelven más rígidos, cambiando el líquido a su estado sólido (a menos que se produzca un sobreenfriamiento ).
Solo dos elementos son líquidos en condiciones estándar de temperatura y presión : el mercurio y el bromo . Cuatro elementos más tienen puntos de fusión ligeramente superiores a la temperatura ambiente : el francio , el cesio , el galio y el rubidio . [1] Además, ciertas mezclas de elementos son líquidas a temperatura ambiente, incluso si los elementos individuales son sólidos en las mismas condiciones (véase mezcla eutéctica ). Un ejemplo es la aleación metálica de sodio y potasio NaK . [2] Otras aleaciones metálicas que son líquidas a temperatura ambiente incluyen el galinstan , que es una aleación de galio, indio y estaño que se funde a −19 °C (−2 °F), así como algunas amalgamas (aleaciones que implican mercurio). [3]
Las sustancias puras que son líquidas en condiciones normales incluyen el agua, el etanol y muchos otros disolventes orgánicos. El agua líquida es de vital importancia en química y biología, y es necesaria para todas las formas de vida conocidas. [4] [5]
Los líquidos inorgánicos incluyen agua, magma , disolventes inorgánicos no acuosos y muchos ácidos .
Los líquidos cotidianos importantes incluyen soluciones acuosas como el blanqueador doméstico , otras mezclas de diferentes sustancias como el aceite mineral y la gasolina, emulsiones como la vinagreta o la mayonesa , suspensiones como la sangre y coloides como la pintura y la leche .
Muchos gases pueden licuarse mediante enfriamiento, lo que produce líquidos como el oxígeno líquido , el nitrógeno líquido , el hidrógeno líquido y el helio líquido . Sin embargo, no todos los gases pueden licuarse a presión atmosférica. El dióxido de carbono , por ejemplo, solo puede licuarse a presiones superiores a 5,1 atm . [6]
Algunos materiales no pueden clasificarse dentro de los tres estados clásicos de la materia. Por ejemplo, los cristales líquidos (utilizados en las pantallas de cristal líquido ) poseen propiedades tanto de sólido como de líquido y pertenecen a su propio estado de la materia, distinto del líquido o del sólido. [7]

Los líquidos son útiles como lubricantes debido a su capacidad de formar una capa delgada y que fluye libremente entre materiales sólidos. Los lubricantes como el aceite se eligen por sus características de viscosidad y flujo que son adecuadas en todo el rango de temperatura de funcionamiento del componente. Los aceites se utilizan a menudo en motores, cajas de cambios , metalurgia y sistemas hidráulicos por sus buenas propiedades de lubricación. [8]
Muchos líquidos se utilizan como disolventes para disolver otros líquidos o sólidos. Las soluciones se encuentran en una amplia variedad de aplicaciones, incluidas pinturas , selladores y adhesivos . La nafta y la acetona se utilizan con frecuencia en la industria para limpiar aceite, grasa y alquitrán de piezas y maquinaria. Los fluidos corporales son soluciones a base de agua.
Los surfactantes se encuentran comúnmente en jabones y detergentes . Los solventes como el alcohol se utilizan a menudo como antimicrobianos . Se encuentran en cosméticos, tintas y láseres de colorante líquido . Se utilizan en la industria alimentaria, en procesos como la extracción de aceite vegetal . [9]
Los líquidos tienden a tener una mejor conductividad térmica que los gases, y la capacidad de fluir hace que un líquido sea adecuado para eliminar el exceso de calor de los componentes mecánicos. El calor se puede eliminar canalizando el líquido a través de un intercambiador de calor , como un radiador , o el calor se puede eliminar con el líquido durante la evaporación . [10] Los refrigerantes de agua o glicol se utilizan para evitar que los motores se sobrecalienten. [11] Los refrigerantes utilizados en los reactores nucleares incluyen agua o metales líquidos, como sodio o bismuto . [12] Las películas de propulsor líquido se utilizan para enfriar las cámaras de empuje de los cohetes . [13] En el mecanizado , se utilizan agua y aceites para eliminar el exceso de calor generado, que puede arruinar rápidamente tanto la pieza de trabajo como las herramientas. Durante la transpiración , el sudor elimina el calor del cuerpo humano al evaporarse. En la industria de la calefacción, la ventilación y el aire acondicionado (HVAC), se utilizan líquidos como el agua para transferir calor de un área a otra. [14]
Los líquidos se utilizan a menudo en la cocina debido a sus excelentes capacidades de transferencia de calor. Además de la conducción térmica, los líquidos transmiten energía por convección. En particular, debido a que los fluidos más cálidos se expanden y se elevan mientras que las áreas más frías se contraen y se hunden, los líquidos con baja viscosidad cinemática tienden a transferir calor a través de la convección a una temperatura bastante constante, lo que hace que un líquido sea adecuado para blanquear , hervir o freír . Se pueden lograr tasas de transferencia de calor aún más altas condensando un gas en un líquido. En el punto de ebullición del líquido, toda la energía térmica se utiliza para provocar el cambio de fase de un líquido a un gas, sin un aumento acompañante de la temperatura, y se almacena como energía potencial química . Cuando el gas se condensa nuevamente en un líquido, este exceso de energía térmica se libera a una temperatura constante. Este fenómeno se utiliza en procesos como la cocción al vapor .
Dado que los líquidos suelen tener diferentes puntos de ebullición, las mezclas o soluciones de líquidos o gases se pueden separar normalmente mediante destilación , utilizando calor, frío, vacío , presión u otros medios. La destilación se puede encontrar en todo, desde la producción de bebidas alcohólicas , hasta las refinerías de petróleo , pasando por la destilación criogénica de gases como el argón , el oxígeno , el nitrógeno , el neón o el xenón mediante licuefacción (enfriándolos por debajo de sus puntos de ebullición individuales). [15]
El líquido es el componente principal de los sistemas hidráulicos , que aprovechan la ley de Pascal para proporcionar potencia fluida . Dispositivos como bombas y ruedas hidráulicas se han utilizado para convertir el movimiento del líquido en trabajo mecánico desde la antigüedad. Los aceites se impulsan a través de bombas hidráulicas , que transmiten esta fuerza a cilindros hidráulicos . La hidráulica se puede encontrar en muchas aplicaciones, como frenos y transmisiones de automóviles , equipos pesados y sistemas de control de aviones. Varias prensas hidráulicas se utilizan ampliamente en reparación y fabricación, para levantar, prensar, sujetar y dar forma. [16]
Los metales líquidos tienen varias propiedades que son útiles en la detección y actuación , particularmente su conductividad eléctrica y capacidad para transmitir fuerzas (incompresibilidad). Como sustancias que fluyen libremente, los metales líquidos conservan estas propiedades en masa incluso bajo una deformación extrema. Por esta razón, se han propuesto para su uso en robots blandos y dispositivos sanitarios portátiles , que deben poder funcionar bajo deformación repetida. [17] [18] El metal galio se considera un candidato prometedor para estas aplicaciones, ya que es un líquido cerca de la temperatura ambiente, tiene baja toxicidad y se evapora lentamente. [19]
Los líquidos se utilizan a veces en dispositivos de medición. Un termómetro suele utilizar la expansión térmica de los líquidos, como el mercurio , combinada con su capacidad de fluir para indicar la temperatura. Un manómetro utiliza el peso del líquido para indicar la presión del aire . [20]
La superficie libre de un líquido giratorio forma un paraboloide circular y, por lo tanto, se puede utilizar como telescopio . Estos se conocen como telescopios de espejo líquido . [21] Son significativamente más baratos que los telescopios convencionales, [22] pero solo pueden apuntar directamente hacia arriba ( telescopio cenital ). Una opción común para el líquido es el mercurio.

Las cantidades de líquidos se miden en unidades de volumen . Estas incluyen la unidad SI metro cúbico (m 3 ) y sus divisiones, en particular el decímetro cúbico, más comúnmente llamado litro (1 dm 3 = 1 L = 0,001 m 3 ), y el centímetro cúbico, también llamado mililitro (1 cm 3 = 1 mL = 0,001 L = 10 −6 m 3 ). [23]
El volumen de una cantidad de líquido está determinado por su temperatura y presión . Los líquidos generalmente se expanden cuando se calientan y se contraen cuando se enfrían. El agua entre 0 °C y 4 °C es una notable excepción. [24]
Por otra parte, los líquidos tienen poca compresibilidad . El agua, por ejemplo, se comprime sólo 46,4 partes por millón por cada unidad de aumento de la presión atmosférica (bar). [25] A unos 4000 bar (400 megapascales o 58.000 psi ) de presión a temperatura ambiente, el agua experimenta sólo una disminución del 11% en su volumen. [26] La incompresibilidad hace que los líquidos sean adecuados para transmitir potencia hidráulica , porque un cambio de presión en un punto de un líquido se transmite sin disminución a todas las demás partes del líquido y se pierde muy poca energía en forma de compresión. [27]
Sin embargo, la compresibilidad insignificante da lugar a otros fenómenos. El golpeteo de las tuberías, llamado golpe de ariete , se produce cuando una válvula se cierra de repente, lo que crea un enorme pico de presión en la válvula que viaja hacia atrás a través del sistema a una velocidad justo por debajo de la del sonido. Otro fenómeno causado por la incompresibilidad de los líquidos es la cavitación . Debido a que los líquidos tienen poca elasticidad, pueden literalmente separarse en áreas de alta turbulencia o cambio drástico de dirección, como el borde de salida de la hélice de un barco o una esquina aguda de una tubería. Un líquido en un área de baja presión (vacío) se vaporiza y forma burbujas, que luego colapsan al entrar en áreas de alta presión. Esto hace que el líquido llene las cavidades dejadas por las burbujas con una tremenda fuerza localizada, erosionando cualquier superficie sólida adyacente. [28]
En un campo gravitatorio , los líquidos ejercen presión sobre los lados de un recipiente, así como sobre cualquier cosa que se encuentre dentro del propio líquido. Esta presión se transmite en todas las direcciones y aumenta con la profundidad. Si un líquido está en reposo en un campo gravitatorio uniforme, la presión en la profundidad viene dada por [29]
dónde:
Para un cuerpo de agua abierto al aire, sería la presión atmosférica .
Los líquidos estáticos en campos gravitacionales uniformes también presentan el fenómeno de flotabilidad , donde los objetos sumergidos en el líquido experimentan una fuerza neta debido a la variación de presión con la profundidad. La magnitud de la fuerza es igual al peso del líquido desplazado por el objeto, y la dirección de la fuerza depende de la densidad promedio del objeto sumergido. Si la densidad es menor que la del líquido, la fuerza de flotación apunta hacia arriba y el objeto flota, mientras que si la densidad es mayor , la fuerza de flotación apunta hacia abajo y el objeto se hunde. Esto se conoce como el principio de Arquímedes . [30]

A menos que el volumen de un líquido coincida exactamente con el volumen de su recipiente, se observan una o más superficies. La presencia de una superficie introduce nuevos fenómenos que no están presentes en un líquido a granel. Esto se debe a que una molécula en una superficie posee enlaces con otras moléculas de líquido solo en el lado interno de la superficie, lo que implica una fuerza neta que atrae las moléculas de la superficie hacia adentro. De manera equivalente, esta fuerza se puede describir en términos de energía: hay una cantidad fija de energía asociada con la formación de una superficie de un área determinada. Esta cantidad es una propiedad material llamada tensión superficial , en unidades de energía por unidad de área (unidades SI: J / m 2 ). Los líquidos con fuertes fuerzas intermoleculares tienden a tener grandes tensiones superficiales. [31]
Una implicación práctica de la tensión superficial es que los líquidos tienden a minimizar su área superficial, formando gotas esféricas y burbujas a menos que existan otras restricciones. La tensión superficial también es responsable de una variedad de otros fenómenos, incluidas las ondas superficiales , la acción capilar , la humectación y las ondulaciones . En líquidos confinados a escala nanométrica , los efectos de la superficie pueden desempeñar un papel dominante ya que, en comparación con una muestra macroscópica de líquido, una fracción mucho mayor de moléculas se encuentran cerca de una superficie.
La tensión superficial de un líquido afecta directamente su humectabilidad . La mayoría de los líquidos comunes tienen tensiones que varían en decenas de mJ/m2 , por lo que las gotas de aceite, agua o pegamento pueden fusionarse fácilmente y adherirse a otras superficies, mientras que los metales líquidos como el mercurio pueden tener tensiones que varían en cientos de mJ/m2 , por lo que las gotas no se combinan fácilmente y las superficies solo pueden humedecerse en condiciones específicas.
Las tensiones superficiales de los líquidos comunes ocupan un rango relativamente estrecho de valores cuando se exponen a condiciones cambiantes como la temperatura, lo que contrasta fuertemente con la enorme variación observada en otras propiedades mecánicas, como la viscosidad. [32]
La superficie libre de un líquido se ve perturbada por la gravedad ( planitud ) y las ondas ( rugosidad de la superficie ).

Una propiedad física importante que caracteriza el flujo de líquidos es la viscosidad . Intuitivamente, la viscosidad describe la resistencia de un líquido a fluir.
En términos más técnicos, la viscosidad mide la resistencia de un líquido a la deformación a una velocidad determinada, como cuando se lo corta a una velocidad finita. [33] Un ejemplo específico es un líquido que fluye a través de una tubería: en este caso, el líquido sufre una deformación por corte, ya que fluye más lentamente cerca de las paredes de la tubería que cerca del centro. Como resultado, presenta una resistencia viscosa al flujo. Para mantener el flujo, se debe aplicar una fuerza externa, como una diferencia de presión entre los extremos de la tubería.
La viscosidad de los líquidos disminuye al aumentar la temperatura. [34]
El control preciso de la viscosidad es importante en muchas aplicaciones, en particular en la industria de la lubricación. Una forma de lograr dicho control es mezclando dos o más líquidos de diferentes viscosidades en proporciones precisas. [35] Además, existen varios aditivos que pueden modular la dependencia de la temperatura de la viscosidad de los aceites lubricantes. Esta capacidad es importante ya que la maquinaria a menudo funciona en un rango de temperaturas (ver también índice de viscosidad ). [36]
El comportamiento viscoso de un líquido puede ser newtoniano o no newtoniano . Un líquido newtoniano exhibe una curva de tensión/deformación lineal, lo que significa que su viscosidad es independiente del tiempo, la velocidad de corte o el historial de velocidad de corte. Algunos ejemplos de líquidos newtonianos son el agua, la glicerina , el aceite de motor , la miel o el mercurio. Un líquido no newtoniano es aquel en el que la viscosidad no es independiente de estos factores y se espesa (aumenta la viscosidad) o se adelgaza (disminuye la viscosidad) bajo cizallamiento. Algunos ejemplos de líquidos no newtonianos son el kétchup , las natillas o las soluciones de almidón . [37]
La velocidad del sonido en un líquido se expresa mediante donde es el módulo volumétrico del líquido y la densidad. Por ejemplo, el agua tiene un módulo volumétrico de aproximadamente 2,2 GPa y una densidad de 1000 kg/m 3 , lo que da c = 1,5 km/s. [38]

A una temperatura inferior al punto de ebullición , cualquier materia en forma líquida se evaporará hasta alcanzar el equilibrio con el proceso inverso de condensación de su vapor. En este punto, el vapor se condensará al mismo ritmo que se evapora el líquido. Por lo tanto, un líquido no puede existir de forma permanente si el líquido evaporado se elimina continuamente. [39] Un líquido en o por encima de su punto de ebullición normalmente hervirá, aunque el sobrecalentamiento puede evitarlo en determinadas circunstancias.
A una temperatura por debajo del punto de congelación, un líquido tenderá a cristalizarse , cambiando a su forma sólida. A diferencia de la transición a gas, no hay equilibrio en esta transición bajo presión constante, [ cita requerida ] por lo que, a menos que ocurra un sobreenfriamiento , el líquido eventualmente cristalizará por completo. Sin embargo, esto solo es cierto bajo presión constante, de modo que (por ejemplo) el agua y el hielo en un recipiente cerrado y resistente podrían alcanzar un equilibrio donde ambas fases coexistan. Para la transición opuesta de sólido a líquido, véase fusión .
El diagrama de fases explica por qué los líquidos no existen en el espacio ni en ningún otro vacío. Puesto que la presión es esencialmente cero (excepto en las superficies o en el interior de los planetas y las lunas), el agua y otros líquidos expuestos al espacio hervirán o se congelarán inmediatamente según la temperatura. En las regiones del espacio cercanas a la Tierra, el agua se congelará si el sol no brilla directamente sobre ella y se vaporizará (sublimará) tan pronto como esté expuesta a la luz solar. Si el agua existe en forma de hielo en la Luna, solo puede existir en agujeros sombreados donde el sol nunca brilla y donde la roca circundante no la calienta demasiado. En algún punto cerca de la órbita de Saturno, la luz del Sol es demasiado débil para sublimar el hielo y convertirlo en vapor de agua. Esto es evidente por la longevidad del hielo que compone los anillos de Saturno. [40]
Los líquidos pueden formar soluciones con gases, sólidos y otros líquidos.
Se dice que dos líquidos son miscibles si pueden formar una solución en cualquier proporción; de lo contrario, son inmiscibles. Por ejemplo, el agua y el etanol (alcohol para beber) son miscibles, mientras que el agua y la gasolina son inmiscibles. [41] En algunos casos, una mezcla de líquidos que de otro modo serían inmiscibles se puede estabilizar para formar una emulsión , donde un líquido se dispersa en el otro como gotas microscópicas. Por lo general, esto requiere la presencia de un surfactante para estabilizar las gotas. Un ejemplo conocido de una emulsión es la mayonesa , que consiste en una mezcla de agua y aceite que se estabiliza con lecitina , una sustancia que se encuentra en las yemas de huevo . [42]
La estructura microscópica de los líquidos es compleja e históricamente ha sido objeto de intensa investigación y debate. [43] [44] [45] [46] A continuación se explican algunas de las ideas clave.
Microscópicamente, los líquidos consisten en un denso y desordenado empaquetamiento de moléculas. Esto contrasta con las otras dos fases comunes de la materia, los gases y los sólidos. Aunque los gases están desordenados, las moléculas están bien separadas en el espacio e interactúan principalmente a través de colisiones entre moléculas. Por el contrario, aunque las moléculas en los sólidos están densamente empaquetadas, generalmente caen en una estructura regular, como una red cristalina ( los vidrios son una notable excepción).
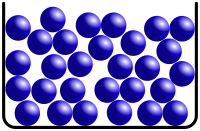
Si bien los líquidos no exhiben un ordenamiento de largo alcance como en una red cristalina, sí poseen un orden de corto alcance , que persiste en unos pocos diámetros moleculares. [47] [48]
En todos los líquidos, las interacciones de volumen excluidas inducen un orden de corto alcance en las posiciones moleculares (coordenadas del centro de masa). Los líquidos monoatómicos clásicos como el argón y el criptón son los ejemplos más simples. Dichos líquidos pueden modelarse como "montones" desordenados de esferas muy compactas, y el orden de corto alcance corresponde al hecho de que los vecinos más cercanos y los próximos más cercanos en un empaquetamiento de esferas tienden a estar separados por múltiplos enteros del diámetro. [49] [50]
En la mayoría de los líquidos, las moléculas no son esferas y las fuerzas intermoleculares poseen una direccionalidad, es decir, dependen de la orientación relativa de las moléculas. Como resultado, existe un orden de orientación de corto alcance además del orden posicional mencionado anteriormente. El orden de orientación es especialmente importante en líquidos con enlaces de hidrógeno como el agua. [51] [52] La fuerza y la naturaleza direccional de los enlaces de hidrógeno impulsan la formación de "redes" o "grupos" locales de moléculas. Debido a la importancia relativa de las fluctuaciones térmicas en los líquidos (en comparación con los sólidos), estas estructuras son altamente dinámicas, deformándose, rompiéndose y reformándose continuamente. [49] [51]
Las características microscópicas de los líquidos derivan de una interacción entre fuerzas intermoleculares atractivas y fuerzas entrópicas . [53]
Las fuerzas de atracción tienden a atraer a las moléculas y, junto con las interacciones repulsivas de corto alcance, son las fuerzas dominantes detrás de la estructura regular de los sólidos. Las fuerzas entrópicas no son "fuerzas" en el sentido mecánico; más bien, describen la tendencia de un sistema a maximizar su entropía a una energía fija (véase el conjunto microcanónico ). En términos generales, las fuerzas entrópicas alejan a las moléculas entre sí, maximizando el volumen que ocupan. Las fuerzas entrópicas dominan en los gases y explican la tendencia de los gases a llenar sus contenedores. En los líquidos, por el contrario, las fuerzas intermoleculares y entrópicas son comparables, por lo que no es posible descuidar una en favor de la otra. Cuantitativamente, la energía de enlace entre moléculas adyacentes es del mismo orden de magnitud que la energía térmica . [54]
La competencia entre energía y entropía hace que los líquidos sean difíciles de modelar a nivel molecular, ya que no existe un "estado de referencia" idealizado que pueda servir como punto de partida para descripciones teóricas manejables. Matemáticamente, no existe un parámetro pequeño a partir del cual se pueda desarrollar una teoría de perturbación sistemática . [44] Esta situación contrasta tanto con los gases como con los sólidos. Para los gases, el estado de referencia es el gas ideal , y la densidad se puede utilizar como un pequeño parámetro para construir una teoría de gases reales (no ideales) (véase expansión virial ). [55] Para los sólidos cristalinos, el estado de referencia es una red cristalina perfecta, y los posibles parámetros pequeños son los movimientos térmicos y los defectos de la red . [51]
Como todas las formas conocidas de materia, los líquidos son fundamentalmente mecánico-cuánticos . Sin embargo, en condiciones estándar (cerca de la temperatura y presión ambiente), gran parte del comportamiento macroscópico de los líquidos se puede entender en términos de mecánica clásica . [54] [56] La "imagen clásica" postula que las moléculas constituyentes son entidades discretas que interactúan a través de fuerzas intermoleculares de acuerdo con las leyes de movimiento de Newton . Como resultado, sus propiedades macroscópicas se pueden describir utilizando la mecánica estadística clásica . Si bien la ley de fuerza intermolecular deriva técnicamente de la mecánica cuántica, generalmente se entiende como una entrada del modelo a la teoría clásica, obtenida ya sea de un ajuste a datos experimentales o del límite clásico de una descripción mecánica cuántica. [57] [47] Un ejemplo ilustrativo, aunque muy simplificado, es una colección de moléculas esféricas que interactúan a través de un potencial de Lennard-Jones . [54]
Para que se aplique el límite clásico, una condición necesaria es que la longitud de onda térmica de De Broglie sea ,
es pequeño en comparación con la escala de longitud en consideración. [54] [58] Aquí, es la constante de Planck y es la masa de la molécula. Los valores típicos de son alrededor de 0,01-0,1 nanómetros (Tabla 1). Por lo tanto, un modelo de alta resolución de la estructura del líquido a escala nanométrica puede requerir consideraciones de mecánica cuántica. Un ejemplo notable es el enlace de hidrógeno en líquidos asociados como el agua, [59] [60] donde, debido a la pequeña masa del protón, los efectos inherentemente cuánticos como el movimiento del punto cero y la tunelización son importantes. [61]
Para que un líquido se comporte de manera clásica a nivel macroscópico, debe ser pequeño en comparación con la distancia promedio entre moléculas. [54] Es decir,
En la Tabla 1 se dan valores representativos de esta relación para algunos líquidos. La conclusión es que los efectos cuánticos son importantes para líquidos a bajas temperaturas y con pequeña masa molecular . [54] [56] Para los procesos dinámicos, existe una restricción de escala de tiempo adicional:
donde es la escala de tiempo del proceso en consideración. Para líquidos a temperatura ambiente, el lado derecho es de aproximadamente 10 −14 segundos, lo que generalmente significa que los procesos dependientes del tiempo que involucran movimiento de traslación se pueden describir de manera clásica. [54]
A temperaturas extremadamente bajas, incluso el comportamiento macroscópico de ciertos líquidos se desvía de la mecánica clásica. Ejemplos notables son el hidrógeno y el helio. Debido a su baja temperatura y masa, estos líquidos tienen una longitud de onda térmica de De Broglie comparable a la distancia promedio entre moléculas. [54]
La expresión para la velocidad del sonido de un líquido,
contiene el módulo volumétrico K . Si K es independiente de la frecuencia, entonces el líquido se comporta como un medio lineal, de modo que el sonido se propaga sin disipación ni acoplamiento de modos . En realidad, todos los líquidos muestran cierta dispersión : al aumentar la frecuencia, K cruza desde el límite de baja frecuencia, similar al líquido, hasta el límite de alta frecuencia, similar al sólido . En líquidos normales, la mayor parte de este cruce tiene lugar en frecuencias entre GHz y THz, a veces llamadas hipersonido .
En frecuencias sub-GHz, un líquido normal no puede soportar ondas de corte : el límite de frecuencia cero del módulo de corte es 0. Esto a veces se considera como la propiedad definitoria de un líquido. [62] [63] Sin embargo, al igual que el módulo volumétrico K , el módulo de corte G también depende de la frecuencia y exhibe un cruce similar en frecuencias de hipersonido.
Según la teoría de respuesta lineal , la transformada de Fourier de K o G describe cómo el sistema vuelve al equilibrio después de una perturbación externa; por esta razón, el paso de dispersión en la región de GHz a THz también se llama relajación . A medida que un líquido se sobreenfría hacia la transición vítrea, el tiempo de relajación estructural aumenta exponencialmente, lo que explica el comportamiento viscoelástico de los líquidos formadores de vidrio.
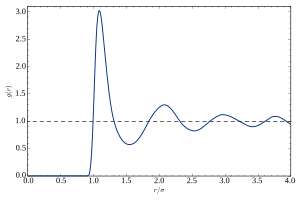
La ausencia de orden de largo alcance en los líquidos se refleja en la ausencia de picos de Bragg en la difracción de rayos X y neutrones . En condiciones normales, el patrón de difracción tiene simetría circular, lo que expresa la isotropía del líquido. Radialmente, la intensidad de difracción oscila suavemente. Esto se puede describir mediante el factor de estructura estática , con el número de onda dado por la longitud de onda de la sonda (fotón o neutrón) y el ángulo de Bragg . Las oscilaciones de expresan el orden de corto alcance del líquido, es decir, las correlaciones entre una molécula y las "capas" de los vecinos más cercanos, los vecinos más próximos, etc.
Una representación equivalente de estas correlaciones es la función de distribución radial , que está relacionada con la transformada de Fourier de . [49] Representa un promedio espacial de una instantánea temporal de correlaciones de pares en el líquido.
Los métodos para predecir las propiedades de los líquidos se pueden organizar por su "escala" de descripción, es decir, las escalas de longitud y de tiempo sobre las que se aplican. [64] [65]
Las correlaciones empíricas son expresiones matemáticas simples destinadas a aproximar las propiedades de un líquido en un rango de condiciones experimentales, como variación de temperatura y presión. [66] Se construyen ajustando formas funcionales simples a datos experimentales. Por ejemplo, la dependencia de la temperatura de la viscosidad del líquido a veces se aproxima mediante la función , donde y son constantes de ajuste. [67] Las correlaciones empíricas permiten estimaciones extremadamente eficientes de propiedades físicas, que pueden ser útiles en simulaciones termofísicas. Sin embargo, requieren datos experimentales de alta calidad para obtener un buen ajuste y no pueden extrapolarse de manera confiable más allá de las condiciones cubiertas por los experimentos.
Los potenciales termodinámicos son funciones que caracterizan el estado de equilibrio de una sustancia. Un ejemplo es la energía libre de Gibbs , que es una función de la presión y la temperatura. Conocer cualquier potencial termodinámico es suficiente para calcular todas las propiedades de equilibrio de una sustancia, a menudo simplemente tomando derivadas de . [55] Por lo tanto, una única correlación para puede reemplazar correlaciones separadas para propiedades individuales. [68] [69] Por el contrario, una variedad de mediciones experimentales (por ejemplo, densidad, capacidad térmica, presión de vapor) se pueden incorporar en el mismo ajuste; en principio, esto permitiría predecir propiedades difíciles de medir como la capacidad térmica en términos de otras mediciones más fácilmente disponibles (por ejemplo, presión de vapor). [70]
Las teorías hidrodinámicas describen los líquidos en términos de campos macroscópicos dependientes del espacio y del tiempo , como la densidad, la velocidad y la temperatura. Estos campos obedecen a ecuaciones diferenciales parciales , que pueden ser lineales o no lineales . [71] Las teorías hidrodinámicas son más generales que las descripciones termodinámicas de equilibrio, que suponen que los líquidos son aproximadamente homogéneos e independientes del tiempo. Las ecuaciones de Navier-Stokes son un ejemplo bien conocido: son ecuaciones diferenciales parciales que dan la evolución temporal de la densidad, la velocidad y la temperatura de un fluido viscoso. Existen numerosos métodos para resolver numéricamente las ecuaciones de Navier-Stokes y sus variantes. [72] [73]
Los métodos mesoscópicos operan en escalas de longitud y tiempo entre los niveles de partículas y de continuo. Por este motivo, combinan elementos de la dinámica basada en partículas y la hidrodinámica del continuo. [64]
Un ejemplo es el método de Boltzmann en red , que modela un fluido como una colección de partículas ficticias que existen en una red. [64] Las partículas evolucionan en el tiempo a través del flujo (movimiento en línea recta) y las colisiones . Conceptualmente, se basa en la ecuación de Boltzmann para gases diluidos, donde la dinámica de una molécula consiste en un movimiento libre interrumpido por colisiones binarias discretas, pero también se aplica a líquidos. A pesar de la analogía con las trayectorias moleculares individuales, es una descripción de grano grueso que normalmente opera en escalas de longitud y tiempo mayores que las de la dinámica molecular verdadera (de ahí la noción de partículas "ficticias").
Otros métodos que combinan elementos de la dinámica continua y a nivel de partículas incluyen la hidrodinámica de partículas suavizadas , [74] [75] la dinámica de partículas disipativas , [76] y la dinámica de colisión de múltiples partículas. [77]
Los métodos de simulación microscópica trabajan directamente con las ecuaciones de movimiento (clásicas o cuánticas) de las moléculas constituyentes.
La dinámica molecular clásica (MD) simula líquidos utilizando la ley de movimiento de Newton; a partir de la segunda ley de Newton ( ), las trayectorias de las moléculas se pueden trazar explícitamente y utilizar para calcular propiedades macroscópicas de líquidos como la densidad o la viscosidad. Sin embargo, la MD clásica requiere expresiones para las fuerzas intermoleculares (" F " en la segunda ley de Newton). Por lo general, estas deben aproximarse utilizando datos experimentales o alguna otra entrada. [47]
Los métodos mecánicos cuánticos ab initio simulan líquidos utilizando únicamente las leyes de la mecánica cuántica y las constantes atómicas fundamentales. [57] A diferencia de la dinámica molecular clásica, los campos de fuerza intermoleculares son un resultado del cálculo, en lugar de una entrada basada en mediciones experimentales u otras consideraciones. En principio, los métodos ab initio pueden simular las propiedades de un líquido dado sin ningún dato experimental previo. Sin embargo, son muy costosos computacionalmente, especialmente para moléculas grandes con estructura interna.
{{cite book}}: CS1 maint: location missing publisher (link){{cite book}}: CS1 maint: location missing publisher (link){{cite book}}: CS1 maint: location missing publisher (link){{cite book}}: CS1 maint: location missing publisher (link){{cite book}}: CS1 maint: location missing publisher (link)