Un ciclo Otto es un ciclo termodinámico idealizado que describe el funcionamiento de un motor de pistón de encendido por chispa típico . Es el ciclo termodinámico que se encuentra con mayor frecuencia en los motores de automóviles. [1]
El ciclo Otto es una descripción de lo que le sucede a un gas cuando se lo somete a cambios de presión, temperatura, volumen, adición y eliminación de calor. El gas que se somete a esos cambios se denomina sistema. El sistema, en este caso, se define como el fluido (gas) dentro del cilindro. Por el contrario, al describir los cambios que tienen lugar dentro del sistema, también se describe el efecto del sistema sobre el medio ambiente. El propósito del ciclo Otto es estudiar la producción de trabajo neto del sistema que puede propulsar un vehículo y sus ocupantes en el medio ambiente.
El ciclo de Otto se construye a partir de:
El proceso isentrópico de compresión o expansión implica que no habrá ineficiencia (pérdida de energía mecánica) y no habrá transferencia de calor hacia dentro o hacia fuera del sistema durante ese proceso. Se supone que el cilindro y el pistón son impermeables al calor durante ese tiempo. Se realiza trabajo en el sistema durante el proceso de compresión isentrópica inferior. El calor fluye hacia el ciclo Otto a través del proceso de presurización izquierdo y parte de él fluye de regreso a través del proceso de despresurización derecho. La suma del trabajo agregado al sistema más el calor agregado menos el calor eliminado da como resultado el trabajo mecánico neto generado por el sistema.
Los procesos se describen mediante: [2]
El ciclo Otto consiste en compresión isentrópica, adición de calor a volumen constante, expansión isentrópica y rechazo de calor a volumen constante. En el caso de un ciclo Otto de cuatro tiempos, técnicamente hay dos procesos adicionales: uno para el escape del calor residual y los productos de la combustión a presión constante (isobárico), y otro para la entrada de aire frío rico en oxígeno también a presión constante; sin embargo, estos procesos se omiten a menudo en un análisis simplificado. Aunque estos dos procesos son críticos para el funcionamiento de un motor real, en el que los detalles de la transferencia de calor y la química de la combustión son relevantes, para el análisis simplificado del ciclo termodinámico, es más conveniente suponer que todo el calor residual se elimina durante un solo cambio de volumen.
El motor de cuatro tiempos fue patentado por primera vez por Alphonse Beau de Rochas en 1861. [3] Antes, alrededor de 1854-57, dos italianos ( Eugenio Barsanti y Felice Matteucci ) inventaron un motor que se rumoreaba que era muy similar, pero la patente se perdió. [ cita requerida ]
La primera persona en construir un motor de cuatro tiempos funcional, un motor estacionario que utiliza una mezcla de aire y gas de carbón como combustible (un motor de gas ), fue el ingeniero alemán Nicolaus Otto . [4] Es por esto que hoy en día el principio de cuatro tiempos se conoce comúnmente como ciclo Otto y los motores de cuatro tiempos que utilizan bujías a menudo se denominan motores Otto.
El ciclo consta de cuatro partes: una masa que contiene una mezcla de combustible y oxígeno es aspirada hacia el cilindro por el pistón que desciende, es comprimida por el pistón que sube, la masa se enciende por una chispa que libera energía en forma de calor, el gas resultante se expande al empujar el pistón hacia abajo y, finalmente, la masa se agota cuando el pistón sube una segunda vez. Como el pistón es capaz de moverse a lo largo del cilindro, el volumen del gas cambia con su posición en el cilindro. Los procesos de compresión y expansión inducidos en el gas por el movimiento del pistón se idealizan como reversibles, es decir, no se pierde trabajo útil por turbulencia o fricción y no se transfiere calor hacia o desde el gas durante esos dos procesos. Una vez que se completa la expansión en el cilindro, se extrae el calor restante y, finalmente, el gas se agota al medio ambiente. Durante el proceso de expansión se produce trabajo mecánico y parte de él se utiliza para comprimir la masa de aire del siguiente ciclo. El trabajo mecánico producido menos el utilizado para el proceso de compresión es el trabajo neto ganado y que se puede utilizar para la propulsión o para impulsar otras máquinas. Alternativamente, el trabajo neto ganado es la diferencia entre el calor producido y el calor eliminado.

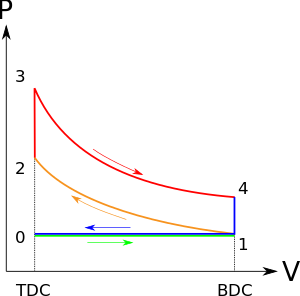
Una masa de aire (fluido de trabajo) se introduce en el cilindro, de 0 a 1, a presión atmosférica (presión constante) a través de la válvula de admisión abierta, mientras que la válvula de escape está cerrada durante este proceso. La válvula de admisión se cierra en el punto 1.
El pistón se mueve desde el extremo del cigüeñal (BDC, punto muerto inferior y volumen máximo) hasta el extremo de la cabeza del cilindro ( TDC , punto muerto superior y volumen mínimo) a medida que el gas de trabajo con estado inicial 1 se comprime isentrópicamente hasta el punto de estado 2, a través de la relación de compresión ( V 1 / V 2 ) . Mecánicamente, esta es la compresión isentrópica de la mezcla de aire/combustible en el cilindro, también conocida como carrera de compresión. Este proceso isentrópico supone que no se pierde energía mecánica debido a la fricción y que no se transfiere calor hacia o desde el gas, por lo tanto, el proceso es reversible. El proceso de compresión requiere que se agregue trabajo mecánico al gas de trabajo. Generalmente, la relación de compresión es de alrededor de 9-10:1 ( V 1 : V 2 ) para un motor típico. [5]
El pistón se encuentra momentáneamente en reposo en el PMS . Durante este instante, que se conoce como fase de ignición, la mezcla de aire y combustible permanece en un pequeño volumen en la parte superior de la carrera de compresión. La combustión del combustible inyectado añade calor al fluido de trabajo, y el volumen se mantiene prácticamente constante. La presión aumenta y la relación se denomina "relación de explosión".
La mayor presión ejerce una fuerza sobre el pistón y lo empuja hacia el punto muerto inferior . La expansión del fluido de trabajo se produce de forma isentrópica y el sistema realiza trabajo sobre el pistón. La relación de volumen se denomina "relación de expansión isentrópica" (en el ciclo Otto es lo mismo que la relación de compresión ). Mecánicamente, esta es la expansión de la mezcla gaseosa caliente en el cilindro, conocida como carrera de expansión (de potencia).
El pistón se encuentra momentáneamente en reposo en el punto más bajo de la cámara de combustión . La presión del gas de trabajo cae instantáneamente del punto 4 al punto 1 durante un proceso de volumen constante a medida que se elimina calor hacia un disipador de calor externo idealizado que se pone en contacto con la culata. En los motores de combustión interna modernos, el disipador de calor puede ser el aire circundante (para motores de baja potencia) o un fluido circulante, como el refrigerante. El gas ha regresado al estado 1.
La válvula de escape se abre en el punto 1. A medida que el pistón se mueve desde "BDC" (punto 1) a "TDC" (punto 0) con la válvula de escape abierta, la mezcla gaseosa se ventila a la atmósfera y el proceso comienza de nuevo.
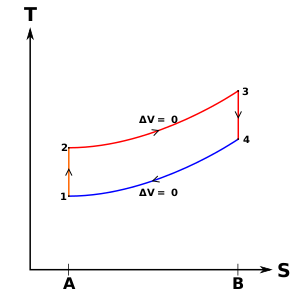
En este proceso 1-2, el pistón realiza trabajo sobre el gas y en el proceso 3-4, el gas realiza trabajo sobre el pistón durante esos procesos de compresión y expansión isentrópica, respectivamente. Los procesos 2-3 y 4-1 son procesos isocóricos; el calor se transfiere al sistema desde 2-3 y se sale del sistema desde 4-1, pero no se realiza trabajo sobre el sistema ni se extrae del sistema durante esos procesos. No se realiza trabajo durante un proceso isocórico (volumen constante) porque la adición o eliminación de trabajo de un sistema requiere el movimiento de los límites del sistema; por lo tanto, como el volumen del cilindro no cambia, no se agrega ni se elimina trabajo del eje del sistema.
Se utilizan cuatro ecuaciones diferentes para describir esos cuatro procesos. Se hace una simplificación suponiendo que los cambios de la energía cinética y potencial que tienen lugar en el sistema (masa del gas) pueden ignorarse y luego se aplica la primera ley de la termodinámica (conservación de la energía) a la masa del gas a medida que cambia de estado, tal como se caracteriza por la temperatura, la presión y el volumen del gas. [2] [ página necesaria ] [6] [ página necesaria ]
Durante un ciclo completo, el gas vuelve a su estado original de temperatura, presión y volumen, por lo que el cambio neto de energía interna del sistema (gas) es cero. Como resultado, la energía (calor o trabajo) agregada al sistema debe compensarse con la energía (calor o trabajo) que sale del sistema. En el análisis de sistemas termodinámicos, la convención es contabilizar la energía que ingresa al sistema como positiva y la energía que sale del sistema como negativa.
Ecuación 1a.
Durante un ciclo completo, el cambio neto de energía del sistema es cero:
Lo anterior establece que el sistema (la masa del gas) vuelve al estado termodinámico original en el que se encontraba al comienzo del ciclo.
¿Dónde se agrega energía al sistema de 1-2-3 y se elimina energía del sistema de 3-4-1? En términos de trabajo y calor agregados al sistema
Ecuación 1b:
Cada término de la ecuación se puede expresar en términos de la energía interna del gas en cada punto del proceso:
El balance energético de la ecuación 1b se convierte en
Para ilustrar el ejemplo elegimos [ dudoso – discutir ] algunos valores para los puntos de la ilustración:
Estos valores se seleccionan de manera arbitraria pero racional [ dudosa – discutir ] . Luego se pueden calcular los términos de trabajo y calor.
La energía agregada al sistema como trabajo durante la compresión de 1 a 2 es
La energía añadida al sistema como calor desde el punto 2 al 3 es
La energía extraída del sistema como trabajo durante la expansión de 3 a 4 es
La energía extraída del sistema en forma de calor desde el punto 4 al 1 es
El balance energético es
Tenga en cuenta que la energía agregada al sistema se cuenta como positiva y la energía que sale del sistema se cuenta como negativa y la suma es cero como se espera para un ciclo completo que devuelve el sistema a su estado original.
Del balance energético el trabajo realizado por el sistema es:
La energía neta que sale del sistema en forma de trabajo es -1, lo que significa que el sistema ha producido una unidad neta de energía que sale del sistema en forma de trabajo.
El calor neto que sale del sistema es:
Como la energía añadida al sistema en forma de calor es positiva, de lo anterior se deduce que el sistema ganó una unidad de calor, lo que coincide con la energía producida por el sistema como trabajo del sistema.
La eficiencia térmica es el cociente entre el trabajo neto del sistema y el calor añadido al sistema. Ecuación 2:
Alternativamente, la eficiencia térmica se puede obtener mediante el calor agregado y el calor rechazado estrictamente.
Suministro de valores ficticios
En el ciclo Otto, no hay transferencia de calor durante los procesos 1-2 y 3-4, ya que son procesos isentrópicos. El calor se suministra solo durante los procesos de volumen constante 2-3 y se rechaza solo durante los procesos de volumen constante 4-1.
Los valores anteriores son valores absolutos que podrían, por ejemplo [ dudoso – discutir ] , tener unidades de julios (suponiendo que se use el sistema de unidades MKS) y serían útiles para un motor particular con dimensiones particulares. En el estudio de los sistemas termodinámicos, las cantidades extensivas como la energía, el volumen o la entropía (en comparación con las cantidades intensivas de temperatura y presión) se colocan sobre una base de masa unitaria, y lo mismo ocurre con los cálculos, lo que los hace más generales y, por lo tanto, de uso más general. Por lo tanto, cada término que involucre una cantidad extensiva podría dividirse por la masa, dando los términos unidades de julios/kg ( energía específica ), metros 3 /kg (volumen específico) o julios/(kelvin·kg) (entropía específica, capacidad calorífica), etc. y se representarían utilizando letras minúsculas, u, v, s, etc.
La ecuación 1 puede relacionarse ahora con la ecuación del calor específico para volumen constante. Los calores específicos son particularmente útiles para los cálculos termodinámicos que involucran el modelo de gas ideal .
Reordenando los rendimientos:
Insertando la ecuación de calor específico en la ecuación de eficiencia térmica (Ecuación 2) se obtiene.
Al reorganizar:
A continuación, si nos fijamos en los diagramas (ver relaciones isentrópicas para un gas ideal ), podemos omitir ambos. La ecuación se reduce entonces a:
Ecuación 2:
Dado que el ciclo Otto utiliza procesos isentrópicos durante la compresión (proceso 1 a 2) y la expansión (proceso 3 a 4), las ecuaciones isentrópicas de los gases ideales y las relaciones presión/volumen constantes se pueden utilizar para obtener las ecuaciones 3 y 4. [7]
Ecuación 3:
Ecuación 4:
Simplificando aún más la ecuación 4, donde es la relación de compresión :
Ecuación 5:
Al invertir la ecuación 4 e insertarla en la ecuación 2, la eficiencia térmica final se puede expresar como: [ página necesaria ] [6] [ página necesaria ]
Ecuación 6:
Del análisis de la ecuación 6 es evidente que la eficiencia del ciclo Otto depende directamente de la relación de compresión . Dado que para el aire es 1,4, un aumento en producirá un aumento en . Sin embargo, para los productos de combustión de la mezcla de combustible/aire a menudo se toma aproximadamente en 1,3. La discusión anterior implica que es más eficiente tener una alta relación de compresión. La relación estándar es aproximadamente 10:1 para automóviles típicos. Por lo general, esto no aumenta mucho debido a la posibilidad de autoignición, o " detonación ", que coloca un límite superior en la relación de compresión. [2] [ página necesaria ] Durante el proceso de compresión 1–2 la temperatura aumenta, por lo tanto, un aumento en la relación de compresión causa un aumento en la temperatura. La autoignición ocurre cuando la temperatura de la mezcla de combustible/aire se vuelve demasiado alta antes de que se encienda por el frente de llama. La carrera de compresión está destinada a comprimir los productos antes de que la llama encienda la mezcla. Si se aumenta la relación de compresión, la mezcla puede autoencenderse antes de que se complete la carrera de compresión, lo que lleva a "detonación del motor". Esto puede dañar los componentes del motor y disminuirá la potencia de freno del motor.
La potencia producida por el ciclo Otto es una energía desarrollada por unidad de tiempo. Los motores Otto se denominan motores de cuatro tiempos. La carrera de admisión y la carrera de compresión requieren una rotación del cigüeñal del motor. La carrera de potencia y la carrera de escape requieren otra rotación. Para dos rotaciones hay una carrera generadora de trabajo.
Del análisis del ciclo anterior, el trabajo neto producido por el sistema:
(de nuevo, usando la convención de signos, el signo menos implica que la energía sale del sistema como trabajo)
Si las unidades utilizadas fueran MKS, el ciclo habría producido un julio de energía en forma de trabajo. Para un motor de una determinada cilindrada, como un litro, la masa de gas del sistema se puede calcular suponiendo que el motor funciona a temperatura (20 °C) y presión (1 atm) estándar. Utilizando la Ley Universal de los Gases, la masa de un litro de gas es a temperatura ambiente y presión a nivel del mar:
A una velocidad del motor de 3000 RPM hay 1500 golpes de trabajo/minuto o 25 golpes de trabajo/segundo.
La potencia es 25 veces mayor, ya que hay 25 golpes de trabajo por segundo.
Si el motor utiliza varios cilindros con la misma cilindrada, el resultado se multiplicaría por el número de cilindros. Estos resultados son el producto de los valores de la energía interna que se supusieron para los cuatro estados del sistema al final de cada uno de los cuatro tiempos (dos rotaciones). Se seleccionaron solo con fines ilustrativos y, obviamente, son de bajo valor. La sustitución de los valores reales de un motor real produciría resultados más cercanos a los del motor. Cuyos resultados serían superiores a los del motor real, ya que se han hecho muchas suposiciones simplificadoras en el análisis que pasan por alto las ineficiencias. Tales resultados sobrestimarían la potencia de salida.
La diferencia entre las presiones y temperaturas de escape y admisión significa que se puede obtener un cierto aumento en la eficiencia mediante el uso de un turbocompresor , eliminando del flujo de escape parte de la energía restante y transfiriéndola al flujo de admisión para aumentar la presión de admisión. Una turbina de gas puede extraer energía de trabajo útil de la corriente de escape y luego puede usarse para presurizar el aire de admisión. La presión y la temperatura de los gases de escape se reducirían a medida que se expanden a través de la turbina de gas y ese trabajo se aplica luego a la corriente de gas de admisión, aumentando su presión y temperatura. La transferencia de energía equivale a una mejora de la eficiencia y también mejora la densidad de potencia resultante del motor. El aire de admisión generalmente se enfría para reducir su volumen, ya que el trabajo producido por carrera es una función directa de la cantidad de masa que se introduce en el cilindro; el aire más denso producirá más trabajo por ciclo. En términos prácticos, la temperatura de la masa del aire de admisión también debe reducirse para evitar la ignición prematura en un motor alimentado con gasolina; por lo tanto, se utiliza un intercooler para eliminar algo de energía en forma de calor y reducir así la temperatura de admisión. Este esquema aumenta tanto la eficiencia como la potencia del motor.
La aplicación de un supercargador impulsado por el cigüeñal aumenta la potencia de salida (densidad de potencia), pero no aumenta la eficiencia, ya que utiliza parte del trabajo neto producido por el motor para presurizar el aire de admisión y no extrae la energía que de otro modo se desperdiciaría asociada con el flujo de escape a alta temperatura y una presión hacia el ambiente.