Las moléculas liberadoras de monóxido de carbono ( CORM ) son compuestos químicos diseñados para liberar cantidades controladas de monóxido de carbono (CO). Los CORM se están desarrollando como posibles agentes terapéuticos para administrar localmente CO a células y tejidos, superando así las limitaciones de los protocolos de inhalación de gas CO.
El CO es mejor conocido por su toxicidad en el envenenamiento por monóxido de carbono en dosis altas. Sin embargo, el CO es un gasotransmisor y dosis bajas suplementarias de CO se han relacionado con beneficios terapéuticos. La investigación preclínica se ha centrado en la actividad antiinflamatoria del CO con importantes aplicaciones en enfermedades cardiovasculares, oncología, cirugía de trasplantes y neuroprotección. [1]
La fuente más simple de CO proviene de una reacción de combustión mediante la quema de fuentes como combustibles fósiles o leña . Las fuentes que liberan CO durante la descomposición térmica o la combustión generalmente no se consideran CORM.
El interés terapéutico por el CO se remonta al estudio de los aires facticios ( hidrocarbonato ) en la década de 1790 por Thomas Beddoes , James Watt , James Lind , Humphry Davy , Tiberius Cavallo y muchos otros. [2]
El tetracarbonilo de níquel fue el primer complejo carbonilo utilizado para lograr la administración local de CO y fue la primera molécula de administración de CO que se sugirió que tenía potencial terapéutico en 1891. [2] El acrónimo CORM se acuñó en 2002, lo que marca la primera iniciativa biomédica y farmacéutica moderna. [3] La reacción enzimática de la hemo oxigenasa inspiró el desarrollo de CORM sintéticos.
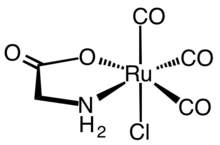
Los primeros CORM sintéticos eran típicamente complejos de carbonilo metálico . Un CORM representativo que se ha caracterizado ampliamente desde un punto de vista bioquímico y farmacológico es el complejo de rutenio (II) Ru ( glicinato ) Cl (CO) 3 , comúnmente conocido como CORM-3. Se están reevaluando los datos terapéuticos relacionados con los CORM metálicos para dilucidar si los efectos observados se deben en realidad al CO o si la reactividad del metal media los efectos fisiológicos a través del agotamiento de tioles, lo que facilita la reducción, el bloqueo de los canales iónicos o la catálisis redox. [4] [5] A pesar de las preguntas relacionadas con los metales de transición, el gas CO puro y los profármacos y dispositivos de administración de fármacos de CO no metálicos alternativos han confirmado el potencial terapéutico del CO.
La mayoría de los CORM terapéuticamente relevantes son complejos de metales de transición basados principalmente en hierro , molibdeno , rutenio , manganeso , cobalto , renio y otros. [6]
La liberación de CO de los agentes portadores puede inducirse fotoquímicamente. Estos portadores se denominan fotoCORM e incluyen tanto complejos metálicos como compuestos ( orgánicos ) libres de metales de diversos motivos estructurales que podrían considerarse como un tipo especial de grupo protector fotolábil . [7]
Se han desarrollado CORM activados por enzimas (ET-CORM) para mejorar la administración local selectiva de CO. Algunos profármacos de ET-CORM son activados por enzimas esterasas para la liberación de CO en un sitio específico. [8]
Se están desarrollando CORM orgánicos para superar la reactividad y ciertas limitaciones de toxicidad de los CORM inorgánicos.
El cloruro de metileno fue el primer CORM orgánico administrado por vía oral según informes anteriores sobre la formación de carboxihemoglobina a través del metabolismo. El segundo CORM orgánico, CORM-A1 (boranocarbonato de sodio), se desarrolló basándose en un informe de la década de 1960 sobre la liberación de CO a partir del boranocarbonato de potasio. [2]
En 2003, se sugirieron los oxocarbonos cíclicos como fuente de CO terapéutico, incluidos el ácido deltico , el ácido escuárico , el ácido crocónico y el ácido rodizónico y sus sales. [9]
En los últimos años se ha observado un creciente interés en los profármacos orgánicos de CO debido a la necesidad de considerar cuestiones de desarrollo de fármacos al desarrollar terapias basadas en CO. [10] Estos profármacos de CO tienen una tasa de liberación ajustable, liberación activada y la capacidad de liberar más de una carga útil de un solo profármaco. [11]
Basado en la sinergia del sistema hemo oxigenasa y el suministro de CO, surgió una nueva clase de híbrido molecular-CORM (HYCO) que consiste en un inductor HO-1 conjunto y especies CORM. Uno de esos HYCO incluye un resto dimetilfumarato que activa NRF2 para inducir HO-1, mientras que el resto CORM también libera CO. [12]
Los materiales liberadores de monóxido de carbono (CORMA) son esencialmente formulaciones y plataformas de administración de fármacos novedosas que han surgido para superar las limitaciones farmacéuticas de la mayoría de las especies de CORM. [13] Un CORMA ejemplar desarrollado por Hubbell consiste en una formulación de micelas preparadas a partir de copolímeros tribloque con una entidad CORM, cuya liberación se activa mediante la adición de cisteína . Otros armazones de liberación de CO incluyen polímeros , péptidos , nanopartículas de sílice , nanodiamantes , nanopartículas magnéticas , gel de nanofibras , metalodendrímeros y conjugados de proteína CORM (macromolécula). [14] [15]
Se han desarrollado otros dispositivos avanzados de administración de fármacos, como CORM encapsulados y tecnologías inspiradas en membranas extracorpóreas . [5]
Se puede infundir carboxihemoglobina para administrar CO. Los enfoques más comunes se basan en carboxihemoglobina bovina PEGilada con polietilenglicol y carboxihemoglobina humana conjugada con PEG de maleimida . [dieciséis]
Se han desplegado estructuras de porfirina como hemo , hemina y análogos de protoporfirina IX metálica (PPIX) (como el cobalto PPIX) para inducir la hemo oxigenasa y posteriormente someterse a biotransformación para liberar CO, el ion inorgánico y biliverdina / bilirrubina . [17] Algunos análogos de PPIX, como PPIX de estaño , mesoporfirina de estaño y PPIX de zinc , son inhibidores de la hemo oxigenasa .
Se considera que el HMOX es la principal fuente de producción endógena de CO, aunque en los últimos años se han identificado otros contribuyentes menores. [18] El CO se forma a una velocidad de 16,4 μmol/hora en el cuerpo humano, aproximadamente el 86% se origina a partir del grupo hemo a través de la hemooxigenasa y ~14% a partir de fuentes no hemo que incluyen: fotooxidación, peroxidación lipídica y xenobióticos. [19] El nivel promedio de carboxihemoglobina (CO-Hb) en un no fumador es inferior al 3% de CO-Hb (mientras que un fumador puede alcanzar niveles cercanos al 10% de CO-Hb), [20] aunque la ubicación geográfica, la ocupación, la salud y El comportamiento son variables contribuyentes.
A finales de la década de 1960, Rudi Schmid caracterizó la enzima que facilita la reacción para el catabolismo del hemo, identificando así la enzima hemo oxigenasa (HMOX).
HMOX es un miembro que contiene hemo de la familia de proteínas de choque térmico (HSP) identificada como HSP32 . Hasta la fecha se han identificado tres isoformas de HMOX, incluida la HMOX-1 inducida por estrés y la HMOX-2 constitutiva. HMOX-1 se considera una proteína de rescate celular que se induce en respuesta al estrés oxidativo y a numerosas enfermedades. Además, HMOX-1 es inducido por innumerables moléculas, incluidas estatinas , hemina y productos naturales . [21] [22]
HMOX cataliza la degradación del hemo a biliverdina / bilirrubina , ion ferroso y CO. Aunque está presente en todo el cuerpo, el HO tiene una actividad significativa en el bazo en la degradación de la hemoglobina durante el reciclaje de eritrocitos (0,8% del conjunto de eritrocitos por día), lo que representa ~80% de la producción endógena de CO derivada del hemo. La mayor parte del 20% restante de la producción de CO derivada del hemo se atribuye al catabolismo hepático de las hemoproteínas ( mioglobina , citocromos , catalasa , peroxidasas , guanilato ciclasa soluble , óxido nítrico sintasa ) y a la eritropoyesis ineficaz en la médula ósea . [23]
La velocidad enzimática y la actividad catalítica de HMOX pueden mejorarse mediante una gran cantidad de sustancias dietéticas y xenobióticos para aumentar la producción de CO.
La formación de CO a partir de la peroxidación lipídica se informó por primera vez a finales de la década de 1960 y se considera un contribuyente menor a la producción endógena de CO. [24] [25] Otras fuentes que contribuyen incluyen: el microbioma, la citocromo P450 reductasa , la acireductona dioxigenasa humana , la tirosinasa , la peroxidación lipídica , los alfa-cetoácidos y otros mecanismos oxidativos y redox. [18]
El monóxido de carbono es una de las tres moléculas de señalización gaseosas junto con el óxido nítrico y el sulfuro de hidrógeno . Estos gases se denominan colectivamente gasotransmisores . El CO es un ejemplo clásico de hormesis en el que una dosis baja es esencial y beneficiosa, mientras que la ausencia o exposición excesiva al CO puede ser tóxica.
La primera evidencia de CO como molécula de señalización se produjo tras la observación de que el CO estimula la guanilato ciclasa soluble y la posterior producción de monofosfato de guanosina cíclico (cGMP) para actuar como vasodilatador en las células del músculo liso vascular . Los efectos antiinflamatorios del CO se atribuyen a la activación de la vía de la proteína quinasa activada por mitógenos (MAPK) p38. Si bien el CO comúnmente interactúa con el átomo de hierro ferroso del hemo en una hemoproteína , [26] se ha demostrado que el CO activa los canales de potasio dependientes de calcio al establecer enlaces de hidrógeno con residuos de histidina de la superficie. [18] [27]
El CO puede tener un efecto inhibidor sobre numerosas proteínas, incluidas el citocromo P450 y la citocromo c oxidasa . [28]
El CO tiene aproximadamente 210 veces mayor afinidad por la hemoglobina que el oxígeno . La constante de disociación de equilibrio para la reacción Hb-CO ⇌ Hb + CO favorece fuertemente al complejo de CO, por lo que la liberación de CO para la excreción pulmonar generalmente lleva algún tiempo.
Basado en esta afinidad de unión, la sangre es esencialmente un sumidero irreversible de CO y presenta un desafío terapéutico para el suministro de O2 a las células y tejidos.
El CO se considera no reactivo en el cuerpo y se excreta principalmente por vía pulmonar . [29]