La tripanosomiasis africana es una infección parasitaria transmitida por insectos que afecta a humanos y otros animales. [3]
La tripanosomiasis africana humana (HAT), también conocida como enfermedad del sueño africana o simplemente enfermedad del sueño , es causada por la especie Trypanosoma brucei . [3] Los humanos están infectados por dos tipos, Trypanosoma brucei gambiense (TbG) y Trypanosoma brucei rhodesiense (TbR). [3] La TbG causa más del 92% de los casos notificados. [1] Ambos generalmente se transmiten por la picadura de una mosca tsetsé infectada y son más comunes en las zonas rurales. [3]
Inicialmente, la primera etapa de la enfermedad se caracteriza por fiebre, dolores de cabeza, picazón y dolores en las articulaciones, y comienza de una a tres semanas después de la picadura. [1] [2] Semanas o meses después, la segunda etapa comienza con confusión, mala coordinación, entumecimiento y problemas para dormir. [2] El diagnóstico se realiza encontrando el parásito en un frotis de sangre o en el líquido de un ganglio linfático. [2] A menudo se necesita una punción lumbar para diferenciar entre la primera y la segunda etapa de la enfermedad. [2] Si la enfermedad no se trata rápidamente, puede provocar la muerte.
La prevención de enfermedades graves implica realizar pruebas de detección de TbG en la población en riesgo. [3] El tratamiento es más fácil cuando la enfermedad se detecta tempranamente y antes de que se presenten síntomas neurológicos. [3] El tratamiento de la primera etapa ha sido con los medicamentos pentamidina o suramina . [3] El tratamiento de la segunda etapa ha involucrado eflornitina o una combinación de nifurtimox y eflornitina para la TbG. [2] [3] El fexinidazol es un tratamiento más reciente que se puede tomar por vía oral, para cualquier etapa de la TbG. [3] Si bien el melarsoprol funciona para ambos tipos, generalmente solo se usa para la TbR, debido a sus efectos secundarios graves. [3] Sin tratamiento, la enfermedad del sueño generalmente resulta en la muerte. [3]
La enfermedad se presenta regularmente en algunas regiones del África subsahariana y la población en riesgo asciende a unos 70 millones en 36 países. [5] Se estima que actualmente hay 11.000 personas infectadas y 2.800 nuevas infecciones en 2015. [6] [1] En 2018 hubo 977 nuevos casos. [3] En 2015 causó alrededor de 3.500 muertes, frente a 34.000 en 1990. [4] [7] Más del 80% de estos casos se producen en la República Democrática del Congo . [1] En la historia reciente se han producido tres brotes importantes: uno entre 1896 y 1906, principalmente en Uganda y la cuenca del Congo , y dos en 1920 y 1970, en varios países africanos. [1] Está clasificada como una enfermedad tropical desatendida . [8] Otros animales, como las vacas, pueden ser portadores de la enfermedad y infectarse, en cuyo caso se la conoce como Nagana o tripanosomiasis animal . [1]
Los síntomas de la tripanosomiasis africana se presentan en dos etapas: la etapa hemolinfática y la etapa neurológica (esta última se caracteriza por la invasión parasitaria del sistema nervioso central). [9] [10] Los síntomas neurológicos ocurren además de las características iniciales, y las dos etapas pueden ser difíciles de distinguir basándose únicamente en las características clínicas. [10]
Se ha informado que la enfermedad se presenta con síntomas atípicos en personas infectadas que provienen de áreas no endémicas (por ejemplo, viajeros). Las razones de esto no están claras y pueden ser genéticas. El bajo número de estos casos también puede haber sesgado los resultados. En estas personas, se dice que la infección se presenta principalmente como fiebre con síntomas gastrointestinales (por ejemplo, diarrea e ictericia) y que sólo en raras ocasiones se desarrolla linfadenopatía . [11]
La enfermedad sistémica a veces es presagiada por una úlcera tripanosómica que se desarrolla en el sitio de la picadura de la mosca infecciosa dentro de los dos días posteriores a la infección. La úlcera se observa con mayor frecuencia en T. b. rhodesiense , y sólo raramente en T. b. gambiense (sin embargo, en la infección por T. b. gambiense , las úlceras son más comunes en personas de áreas no endémicas). [10]
El período de incubación es de 1 a 3 semanas para T. b. rhodesiense, y más largo (pero caracterizado con menos precisión) en T. b. infección gambiense . La primera etapa/inicial, conocida como fase hemolinfática, se caracteriza por síntomas generalizados e inespecíficos [10] como: fiebre (intermitente) , dolores de cabeza (severos), [12] dolores en las articulaciones , picazón , [9] [10] debilidad, malestar general, fatiga, pérdida de peso, linfadenopatía y hepatoesplenomegalia . [10]
El diagnóstico puede retrasarse debido a la vaguedad de los síntomas iniciales. La enfermedad también puede confundirse con la malaria (que, de hecho, puede ocurrir como una coinfección). [11]
La fiebre es intermitente, con ataques que duran de un día a una semana, separados por intervalos de unos pocos días a un mes o más. [9] [10] Los episodios de fiebre se vuelven menos frecuentes a medida que avanza la enfermedad. [10]
La invasión de los sistemas circulatorio y linfático por parte del parásito se asocia con una inflamación grave de los ganglios linfáticos , a menudo de tamaños enormes. [9] Los ganglios linfáticos cervicales posteriores son los más comúnmente afectados; sin embargo, también puede ocurrir afectación de los ganglios linfáticos axilares, inguinales y epitrocleares. [10] Puede aparecer el signo de Winterbottom , los reveladores ganglios linfáticos inflamados a lo largo de la parte posterior del cuello. [9] El signo de Winterbottom es común en T. b. infección gambiense . [10]
Los afectados pueden presentar además: erupción cutánea, [12] anemia hemolítica, hepatomegalia y función hepática anormal, esplenomegalia, alteraciones endocrinas, afectación cardíaca (por ejemplo, pericarditis e insuficiencia cardíaca congestiva) y afectación oftálmica. [11]
La segunda fase de la enfermedad, la fase neurológica (también llamada etapa meningoencefálica [10] ), comienza cuando el parásito invade el sistema nervioso central atravesando la barrera hematoencefálica . [9] La progresión a la fase neurológica se produce después de aproximadamente 21 a 60 días en el caso de T. b. rhodesiens e, y de 300 a 500 días en el caso de T. b. infección gambiense . [10]
En realidad, las dos fases se superponen y son difíciles de distinguir basándose únicamente en las características clínicas; La determinación del estadio real de la enfermedad se logra examinando el líquido cefalorraquídeo para detectar la presencia del parásito. [10]
Los trastornos del sueño y la vigilia son una característica principal de la etapa neurológica [9] [15] y dan a la enfermedad su nombre común de "enfermedad del sueño". [9] [10] [15] Las personas infectadas experimentan un ciclo de sueño-vigilia desorganizado y fragmentado. [9] Los afectados experimentan una inversión del sueño que resulta en sueño diurno [9] y somnolencia, [10] y períodos nocturnos de vigilia [9] e insomnio. [10] Además, los afectados también experimentan episodios de somnolencia repentina. [10]
Los síntomas neurológicos incluyen: temblor , debilidad muscular general, hemiparesia , parálisis de una extremidad, [16] tono muscular anormal, alteración de la marcha, ataxia, alteraciones del habla, parestesia, hiperestesia, anestesia, alteración visual, reflejos anormales, convulsiones y coma. [10] Los movimientos similares al Parkinson pueden surgir debido a trastornos del movimiento no específicos y trastornos del habla. [16]
Los individuos pueden exhibir síntomas psiquiátricos que a veces pueden dominar el diagnóstico clínico y pueden incluir agresividad, apatía , [10] [16] irritabilidad, reacciones psicóticas [16] y alucinaciones , ansiedad , labilidad emocional , confusión , manía , déficit de atención y delirio . [10]
Sin tratamiento, la enfermedad es invariablemente mortal, con un deterioro mental progresivo que conduce al coma, insuficiencia orgánica sistémica y la muerte. Una infección no tratada por T. b. rhodesiense causará la muerte en unos meses [17], mientras que una infección no tratada por T. b. gambiense le provocará la muerte al cabo de varios años. [18] El daño causado en la fase neurológica es irreversible. [19]
El Trypanosoma brucei gambiense representa la mayoría de los casos de tripanosomiasis africana, siendo los humanos el principal reservorio necesario para la transmisión, mientras que el Trypanosoma brucei rhodesiense es principalmente zoonótico, con infecciones humanas accidentales. [20] La epidemiología de la tripanosomiasis africana depende de las interacciones entre el parásito (tripanosoma), el vector ( mosca tsetsé ) y el huésped. [20]
Hay dos subespecies del parásito que son responsables de iniciar la enfermedad en humanos. Trypanosoma brucei gambiense causa enfermedades en África occidental y central , mientras que Trypanosoma brucei rhodesiense tiene un rango geográfico limitado y es responsable de causar la enfermedad en África oriental y meridional. Además, una tercera subespecie del parásito conocida como Trypanosoma brucei brucei es la encargada de afectar a los animales pero no a los humanos. [16]
Los seres humanos son el principal reservorio de T. b. gambiense pero esta especie también se puede encontrar en cerdos y otros animales. Los animales de caza silvestre y el ganado son los principales reservorios de T. b. rodesiense . Estos parásitos infectan principalmente a personas del África subsahariana porque es allí donde se encuentra el vector (la mosca tsetsé). Las dos formas humanas de la enfermedad también varían mucho en intensidad. T. b. gambiense causa una condición crónica que puede permanecer en una fase pasiva durante meses o años antes de que surjan los síntomas y la infección puede durar unos tres años antes de que ocurra la muerte. [16]
T. b. rhodesiense es la forma aguda de la enfermedad y la muerte puede ocurrir en unos meses, ya que los síntomas aparecen en unas semanas y es más virulenta y de desarrollo más rápido que T. b. gambiense . Además, los tripanosomas están rodeados por una capa compuesta de glicoproteínas de superficie variantes (VSG). Estas proteínas actúan para proteger al parásito de cualquier factor lítico presente en el plasma humano. El sistema inmunológico del huésped reconoce las glicoproteínas presentes en la cubierta del parásito y produce diferentes anticuerpos (IgM e IgG). [16]
Estos anticuerpos actuarán entonces para destruir los parásitos que circulan por la sangre. Sin embargo, de los diversos parásitos presentes en el plasma, un pequeño número de ellos experimentará cambios en sus capas superficiales, lo que dará como resultado la formación de nuevos VSG. Por lo tanto, los anticuerpos producidos por el sistema inmunológico ya no reconocerán el parásito que conduce a la proliferación hasta que se creen nuevos anticuerpos para combatir los nuevos VSG. Con el tiempo, el sistema inmunológico ya no podrá combatir el parásito debido a los cambios constantes en los VSG y surgirá una infección. [16]

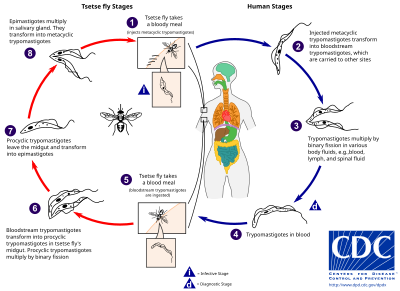
La mosca tsetsé (género Glossina ) es una mosca grande, marrón y picadora que sirve como huésped y vector de los parásitos tripanosomas . Mientras extrae sangre de un huésped mamífero, una mosca tsetsé infectada inyecta tripomastigotes metacíclicos en el tejido de la piel. Desde la picadura, los parásitos ingresan primero al sistema linfático y luego pasan al torrente sanguíneo. Dentro del huésped mamífero, se transforman en tripomastigotes del torrente sanguíneo y son transportados a otros sitios del cuerpo, alcanzan otros fluidos corporales (p. ej., linfa, líquido cefalorraquídeo) y continúan replicándose mediante fisión binaria . [21] [22]
Todo el ciclo de vida de los tripanosomas africanos está representado por etapas extracelulares. Una mosca tsetsé se infecta con tripomastigotes del torrente sanguíneo cuando ingiere sangre de un huésped mamífero infectado. En el intestino medio de la mosca, los parásitos se transforman en tripomastigotes procíclicos, se multiplican por fisión binaria, abandonan el intestino medio y se transforman en epimastigotes. Los epimastigotes llegan a las glándulas salivales de la mosca y continúan su multiplicación por fisión binaria. [23]
El ciclo de vida completo de la mosca dura unas tres semanas. Además de por la picadura de la mosca tsetsé , la enfermedad puede transmitirse por:
Los tábanos ( Tabanidae ) y las moscas de los establos ( Muscidae ) posiblemente desempeñen un papel en la transmisión de nagana (la forma animal de la enfermedad del sueño) y la forma de enfermedad humana. [26]
El triptofol es un compuesto químico producido por el parásito tripanosómico en la enfermedad del sueño que induce el sueño en los humanos. [27]

El estándar de oro para el diagnóstico es la identificación de tripanosomas en una muestra mediante examen microscópico. Las muestras que se pueden utilizar para el diagnóstico incluyen líquido de úlcera , aspirados de ganglios linfáticos, sangre, médula ósea y, durante la etapa neurológica, líquido cefalorraquídeo . La detección de anticuerpos específicos de tripanosoma se puede utilizar para el diagnóstico, pero la sensibilidad y especificidad de estos métodos son demasiado variables para usarse solos para el diagnóstico clínico. Además, la seroconversión se produce después de la aparición de los síntomas clínicos durante una infección por T. b. infección rhodesiense , por lo que tiene un uso diagnóstico limitado. [ cita necesaria ]
Los tripanosomas se pueden detectar a partir de muestras utilizando dos preparaciones diferentes. Se puede utilizar una preparación húmeda para buscar tripanosomas móviles. Alternativamente, se puede teñir un frotis fijo (secado) usando la técnica de Giemsa o Field y examinarlo bajo un microscopio. A menudo, el parásito se encuentra en una abundancia relativamente baja en la muestra, por lo que se pueden utilizar técnicas para concentrar los parásitos antes del examen microscópico. Para las muestras de sangre, estas incluyen la centrifugación seguida del examen de la capa leucocitaria ; miniintercambio aniónico/centrifugación; y la técnica cuantitativa de capa leucocitaria (QBC). Para otras muestras, como el líquido cefalorraquídeo, las técnicas de concentración incluyen la centrifugación seguida del examen del sedimento. [ cita necesaria ]
También están disponibles tres pruebas serológicas para la detección del parásito: la micro-CATT (prueba de aglutinación en tarjeta para la tripanosomiasis), wb-CATT y wb-LATEX. El primero utiliza sangre seca, mientras que los otros dos utilizan muestras de sangre completa. Un estudio de 2002 encontró que el wb-CATT es el más eficaz para el diagnóstico, mientras que el wb-LATEX es un mejor examen para situaciones en las que se requiere mayor sensibilidad. [28]

Actualmente existen pocas opciones de prevención médicamente relacionadas para la tripanosomiasis africana (es decir, no existe ninguna vacuna para la inmunidad). Aunque el riesgo de infección por la picadura de la mosca tsetsé es menor (se estima en menos del 0,1%), el uso de repelentes de insectos, el uso de ropa de manga larga, evitar las zonas con mucha densidad de mosca tsetsé, la implementación de métodos de limpieza de arbustos y el sacrificio de animales de caza silvestre son los mejores. opciones para evitar la infección disponibles para los residentes locales de las áreas afectadas. [16]
En julio de 2000, se aprobó una resolución para formar la Campaña Panafricana de Erradicación de la Mosca Tsetsé y la Tripanosomiasis (PATTEC). La campaña tiene como objetivo erradicar los niveles de población del vector tsetsé y, posteriormente, la enfermedad de los protozoos, mediante el uso de objetivos impregnados con insecticidas, trampas para moscas, ganado tratado con insecticidas, fumigación aérea/terrestre (SAT) con dosis ultrabajas de los lugares de descanso de la mosca tsetsé y zonas estériles. técnica de insectos (SIT). [30] El uso de la TIE en Zanzíbar demostró ser eficaz para eliminar toda la población de moscas tsetsé, pero era costoso y relativamente poco práctico de usar en muchos de los países endémicos afectados por la tripanosomiasis africana. [31]
Un programa piloto en Senegal ha reducido la población de mosca tsetsé hasta en un 99% mediante la introducción de moscas macho que han sido esterilizadas por exposición a rayos gamma . [32] [33]
La vigilancia activa periódica, que implica la detección y el tratamiento rápido de nuevas infecciones, y el control de la mosca tsetsé son la columna vertebral de la estrategia utilizada para controlar la enfermedad del sueño. La detección sistemática de las comunidades en riesgo es el mejor enfoque, porque la detección caso por caso no es práctica en regiones endémicas. La detección sistemática puede adoptar la forma de clínicas móviles o centros de detección fijos donde los equipos viajan diariamente a áreas con altas tasas de infección. Estos esfuerzos de detección son importantes porque los primeros síntomas no son evidentes ni lo suficientemente graves como para justificar que las personas con enfermedad gambiense busquen atención médica, especialmente en áreas muy remotas. Además, el diagnóstico de la enfermedad es difícil y es posible que los trabajadores de la salud no asocien estos síntomas generales con la tripanosomiasis. La detección sistemática permite detectar y tratar la enfermedad en etapa temprana antes de que progrese y elimina el posible reservorio humano. [34] Se ha informado de un solo caso de transmisión sexual de la enfermedad del sueño en África occidental. [25]
El tratamiento depende de si la enfermedad se descubre en la primera o segunda etapa de la enfermedad. Un requisito para el tratamiento de la segunda etapa es que el fármaco atraviese la barrera hematoencefálica .
El tratamiento para la enfermedad en primera etapa es fexinidazol por vía oral o pentamidina inyectable para T. b. gambiense . [3] La suramina inyectable se utiliza para la T. b. rodesiense . [3]
Se puede utilizar fexinidazol para la segunda etapa de la TbG, si la enfermedad no es grave. [35] [3] De lo contrario, un régimen que incluya la combinación de nifurtimox y eflornitina , el tratamiento combinado de nifurtimox y eflornitina (NECT) o eflornitina sola parece ser más efectivo y producir menos efectos secundarios. [36] Estos tratamientos pueden reemplazar al melarsoprol cuando esté disponible. [36] [2] NECT tiene la ventaja de requerir menos inyecciones de eflornitina. [36]
El melarsoprol intravenoso era anteriormente el tratamiento estándar para la enfermedad en segunda etapa (fase neurológica) y es eficaz para ambos tipos. [2] Melarsoprol es el único tratamiento para la T. b. rodesiense ; sin embargo, provoca la muerte en el 5% de las personas que lo toman. [2] Puede producirse resistencia al melarsoprol. [2]
Proyectos de desarrollo de fármacos . Un desafío importante ha sido encontrar fármacos que atraviesen fácilmente la barrera hematoencefálica. El último fármaco que se ha utilizado clínicamente es el fexinidazol, pero también se han obtenido resultados prometedores con el fármaco benzoxaborol acoziborol (SCYX-7158). Actualmente este fármaco se encuentra en evaluación como tratamiento oral en monodosis, lo que supone una gran ventaja frente a los fármacos utilizados actualmente. Otro campo de investigación que se ha estudiado ampliamente en Trypanosoma brucei es apuntar a su metabolismo de nucleótidos. [37] Los estudios sobre el metabolismo de los nucleótidos han conducido al desarrollo de análogos de adenosina que parecen prometedores en estudios con animales, y al hallazgo de que la regulación negativa del transportador de adenosina P2 es una forma común de adquirir resistencia parcial a los fármacos contra las familias de fármacos melaminofenilarsénico y diamidina. (que contienen melarsoprol y pentamidina, respectivamente). [37] La absorción y degradación de los medicamentos son dos cuestiones importantes a considerar para evitar el desarrollo de resistencia a los medicamentos. En el caso de los análogos de nucleósidos, deben ser captados por el transportador de nucleósidos P1 (en lugar de P2) y también deben ser resistentes a la escisión en el parásito. [38] [39]
Si no se trata, T. b. gambiense casi siempre resulta en la muerte, y en un seguimiento a largo plazo de 15 años, solo unos pocos individuos demostraron haber sobrevivido después de rechazar el tratamiento. T. b. rhodesiense , al ser una forma más aguda y grave de la enfermedad, es siempre mortal si no se trata. [2]
La progresión de la enfermedad varía mucho según la forma de la enfermedad. Para personas infectadas por T. b. gambiense , que representa el 92% de todos los casos reportados, una persona puede estar infectada durante meses o incluso años sin signos ni síntomas hasta la etapa avanzada de la enfermedad, donde ya es demasiado tarde para ser tratada con éxito. Para personas afectadas por T. b. rhodesiense , que representa el 2% de todos los casos notificados, los síntomas aparecen a las pocas semanas o meses de la infección. La progresión de la enfermedad es rápida e invade el sistema nervioso central, provocando la muerte en poco tiempo. [40]

En 2010, causó alrededor de 9.000 muertes, frente a 34.000 en 1990. [7] En 2000, los años de vida ajustados por discapacidad (9 a 10 años) perdidos debido a la enfermedad del sueño ascendieron a 2,0 millones. [42] Entre 2010 y 2014, se estimaba que 55 millones de personas estaban en riesgo de contraer tripanosomiasis africana gambiense y más de 6 millones de personas en riesgo de contraer tripanosomiasis africana rhodesiense . [43] En 2014, la Organización Mundial de la Salud informó 3.797 casos de tripanosomiasis africana humana cuando el número previsto de casos era de 5.000. El número total de casos notificados en 2014 supone una reducción del 86 % con respecto al número total de casos notificados en 2000. [43]
Se ha registrado que la enfermedad ocurre en 37 países, todos en el África subsahariana. Ocurre regularmente en el sureste de Uganda y el oeste de Kenia, y mató a más de 48.000 africanos en 2008. [19] La República Democrática del Congo es el país más afectado del mundo y representa el 75% de los casos de Trypanosoma brucei gambiense . [20] La población en riesgo es de aproximadamente 69 millones, de los cuales un tercio se encuentra en un riesgo "muy alto" a "moderado" y los dos tercios restantes en un riesgo "bajo" a "muy bajo". [5] El número de personas afectadas por la enfermedad ha disminuido. A este ritmo, la eliminación de la enfermedad del sueño es una posibilidad. La Organización Mundial de la Salud planea erradicar la enfermedad del sueño para 2030. [43] [44]

Esta condición ha estado presente en África desde hace miles de años. [47] Debido a la falta de viajes entre los pueblos indígenas, la enfermedad del sueño en los humanos se había limitado a focos aislados. Esto cambió después de que los traficantes de esclavos árabes entraron en África central desde el este, siguiendo el río Congo , trayendo consigo parásitos. La enfermedad del sueño de Gambia viajó por el río Congo y luego más al este. [48]
Un escritor árabe del siglo XIV dejó la siguiente descripción del caso de un sultán del Reino de Mali: "Su fin fue ser sobrepasado por la enfermedad del sueño ( illat an-nawm ), que es una enfermedad que frecuentemente afecta a los habitantes de estos países, especialmente a sus jefes, el sueño se apodera de uno de ellos de tal manera que es casi imposible despertarlo". [48]
El cirujano naval británico John Atkins describió la enfermedad a su regreso de África occidental en 1734: [48]
El Moquillo Soñoliento (común entre los Negros) no da más aviso previo que la falta de Apetito 2 ó 3 días antes; sus sueños son profundos y sus sentidos y sensaciones son muy escasos; porque tirar, golpear o azotar difícilmente despertará el Sentido y el Poder suficientes para moverse; y en el momento en que dejas de golpear, el dolor se olvida y vuelve a caer en un estado de insensibilidad, goteando constantemente de la boca como si estuviera salivando profundamente; Respire lentamente, pero no de manera desigual, ni resople. Los jóvenes están más sujetos a ello que los mayores; y el juicio generalmente pronunciado es la muerte, y el Prognostik rara vez falla. Si de vez en cuando uno de ellos se recupera, ciertamente pierde la poca Razón que tenía y se vuelve Ideota...
La cirujana naval francesa Marie-Théophile Griffon du Bellay trató y describió casos mientras estaba estacionada a bordo del barco hospital Caravane en Gabón a finales de la década de 1860. [49]
En 1901, estalló una epidemia devastadora en Uganda , que mató a más de 250.000 personas, [50] incluidas aproximadamente dos tercios de la población de las zonas afectadas a orillas del lago. Según The Cambridge History of Africa , "Se ha estimado que hasta la mitad de la gente murió de enfermedad del sueño y viruela en las tierras a ambas orillas del bajo río Congo ". [51]
El agente causal y el vector fueron identificados en 1903 por David Bruce , y las subespecies de los protozoos se diferenciaron en 1910. Bruce había demostrado anteriormente que T. brucei era la causa de una enfermedad similar en caballos y ganado que era transmitida por la mosca tsetsé. ( Glosina morsitans ). [48]
El primer tratamiento eficaz, atoxyl , un fármaco a base de arsénico desarrollado por Paul Ehrlich y Kiyoshi Shiga , se introdujo en 1910, pero la ceguera fue un efecto secundario grave.
La suramina fue sintetizada por primera vez por Oskar Dressel y Richard Kothe en 1916 para Bayer . Fue introducido en 1920 para tratar la primera etapa de la enfermedad. En 1922, la suramina se combinaba generalmente con triparsamida (otro fármaco organoarsénico pentavalente), el primer fármaco que entró en el sistema nervioso y fue útil en el tratamiento de la segunda etapa de la forma gambiense. La triparsamida fue anunciada en el Journal of Experimental Medicine en 1919 y probada en el Congo belga por Louise Pearce del Instituto Rockefeller en 1920. Se utilizó durante la gran epidemia en África occidental y central en millones de personas y fue la base de la terapia hasta la década de 1960. [52] El médico misionero estadounidense Arthur Lewis Piper participó activamente en el uso de triparsamida para tratar la enfermedad del sueño en el Congo belga en 1925. [53]
La pentamidina , un fármaco muy eficaz para la primera etapa de la enfermedad, se utiliza desde 1937. [54] Durante la década de 1950, se utilizó ampliamente como agente profiláctico en África occidental, lo que provocó una fuerte disminución de las tasas de infección. En aquel momento se pensaba que la erradicación de la enfermedad estaba al alcance de la mano. [ cita necesaria ] [55]
El melarsoprol organoarsenical (Arsobal) desarrollado en la década de 1940 es eficaz para las personas con enfermedad del sueño en la segunda etapa. Sin embargo, entre el 3 y el 10% de los inyectados padecen encefalopatía reactiva (convulsiones, coma progresivo o reacciones psicóticas) y entre el 10 y el 70% de esos casos provocan la muerte; puede causar daño cerebral en quienes sobreviven a la encefalopatía. Sin embargo, debido a su eficacia, el melarsoprol todavía se utiliza en la actualidad. La resistencia al melarsoprol está aumentando y actualmente se está investigando la terapia combinada con nifurtimox. [ cita necesaria ]
La eflornitina (difluorometilornitina o DFMO), el tratamiento más moderno, fue desarrollada en los años 1970 por Albert Sjoerdsma y fue sometida a ensayos clínicos en los años 1980. El medicamento fue aprobado por la Administración de Alimentos y Medicamentos de los Estados Unidos en 1990. [56] Aventis , la empresa responsable de su fabricación, detuvo la producción en 1999. En 2001, Aventis, en asociación con Médicos Sin Fronteras y la Organización Mundial de la Salud , firmó un acuerdo a largo plazo para fabricar y donar el medicamento. [ cita necesaria ]
Además de la enfermedad del sueño, los nombres anteriores incluían letargo negro, maladie du sommeil (francés), Schlafkrankheit (alemán), letargo africano [57] y tripanosomiasis del Congo. [57] [58]
Se ha secuenciado el genoma del parásito y se han identificado varias proteínas como objetivos potenciales para el tratamiento farmacológico. El análisis del genoma también reveló la razón por la que ha sido tan difícil generar una vacuna para esta enfermedad. T. brucei tiene más de 800 genes que producen proteínas que el parásito "mezcla y combina" para evadir la detección del sistema inmunológico. [59]
Se está estudiando el uso de una forma genéticamente modificada de una bacteria que se encuentra naturalmente en el intestino de los vectores como método para controlar la enfermedad. [60]
Hallazgos recientes indican que el parásito no puede sobrevivir en el torrente sanguíneo sin su flagelo . Esta idea ofrece a los investigadores un nuevo ángulo con el que atacar al parásito. [61]
Se están investigando vacunas contra la tripanosomiasis .
Además, la Iniciativa de Medicamentos para Enfermedades Desatendidas ha contribuido a la investigación africana sobre la enfermedad del sueño mediante el desarrollo de un compuesto llamado fexinidazol . Este proyecto se inició originalmente en abril de 2007 e inscribió a 749 personas en la República Democrática del Congo y la República Centroafricana . Los resultados mostraron eficacia y seguridad en ambas etapas de la enfermedad, tanto en adultos como en niños ≥ 6 años y con peso ≥ 20 kg. [62] La Agencia Europea de Medicamentos lo aprobó para la enfermedad en primera y segunda etapa fuera de Europa en noviembre de 2018. [63] El tratamiento fue aprobado en la República Democrática del Congo en diciembre de 2018. [64]
Para las estadísticas de financiación actuales, la tripanosomiasis africana humana se agrupa con las infecciones por cinetoplástidos. Los cinetoplastidos se refieren a un grupo de protozoos flagelados. [65] Las infecciones por cinetoplastidios incluyen la enfermedad del sueño africana, la enfermedad de Chagas y la leishmaniasis. En conjunto, estas tres enfermedades representaron 4,4 millones de años de vida ajustados por discapacidad (AVAD) y 70.075 muertes adicionales registradas cada año. [65] Para las infecciones por cinetoplastidios, la financiación global total para investigación y desarrollo fue de aproximadamente 136,3 millones de dólares en 2012. Cada una de las tres enfermedades, la enfermedad del sueño africana, la enfermedad de Chagas y la leishmaniasis, recibieron cada una aproximadamente un tercio de la financiación, que fue de aproximadamente 36,8 dólares. millones de dólares estadounidenses, 38,7 millones de dólares estadounidenses y 31,7 millones de dólares estadounidenses, respectivamente. [65]
Para la enfermedad del sueño, la financiación se dividió en investigación básica, descubrimiento de fármacos, vacunas y diagnóstico. La mayor parte de la financiación se destinó a la investigación básica de la enfermedad; Se destinaron aproximadamente 21,6 millones de dólares estadounidenses a ese esfuerzo. En cuanto al desarrollo terapéutico, se invirtieron aproximadamente $10,9 millones. [65]
Los principales financiadores de la investigación y el desarrollo de la infección por cinetoplastos son fuentes públicas. Alrededor del 62% de la financiación proviene de países de ingresos altos, mientras que el 9% proviene de países de ingresos bajos y medianos. La financiación pública de los países de altos ingresos es el mayor contribuyente al esfuerzo de investigación de enfermedades desatendidas. Sin embargo, en los últimos años, la financiación procedente de los países de altos ingresos ha ido disminuyendo constantemente; en 2007, los países de altos ingresos proporcionaron el 67,5% del financiamiento total, mientras que, en 2012, los fondos públicos de los países de altos ingresos solo proporcionaron el 60% del financiamiento total para las infecciones por cinetoplastos. Esta tendencia a la baja deja un vacío que deben llenar otros financiadores, como fundaciones filantrópicas y compañías farmacéuticas privadas. [65]
Gran parte del progreso que se ha logrado en la investigación africana sobre la enfermedad del sueño y las enfermedades desatendidas en su conjunto es el resultado de otros financiadores no públicos. Una de estas principales fuentes de financiación proviene de fundaciones, que cada vez están más comprometidas con el descubrimiento de fármacos para enfermedades desatendidas en el siglo XXI. En 2012, las fuentes filantrópicas proporcionaron el 15,9% de la financiación total. [65] La Fundación Bill y Melinda Gates ha sido líder en la provisión de fondos para el desarrollo de medicamentos para enfermedades desatendidas . Han aportado 444,1 millones de dólares estadounidenses para la investigación de enfermedades desatendidas en 2012. Hasta la fecha, han donado más de 1.020 millones de dólares estadounidenses para los esfuerzos de descubrimiento de enfermedades desatendidas. [66]
Para las infecciones por cinetoplastidios específicamente, han donado un promedio de 28,15 millones de dólares estadounidenses al año entre los años 2007 y 2011. [65] Han etiquetado a la tripanosomiasis africana humana como un objetivo de alta oportunidad, lo que significa que es una enfermedad que presenta la mayor oportunidad de control. eliminación y erradicación, mediante el desarrollo de nuevos medicamentos, vacunas, programas de salud pública y diagnósticos. Son la segunda fuente de financiación más importante para enfermedades desatendidas, inmediatamente detrás de los Institutos Nacionales de Salud de Estados Unidos. [65] En un momento en el que la financiación pública está disminuyendo y las subvenciones gubernamentales para la investigación científica son más difíciles de obtener, el mundo filantrópico ha intervenido para impulsar la investigación. [ cita necesaria ]
Otro componente importante del aumento del interés y la financiación procede de la industria. En 2012, contribuyeron con el 13,1% del total al esfuerzo de investigación y desarrollo de cinetoplástidos y, además, desempeñaron un papel importante al contribuir a asociaciones público-privadas (PPP), así como a asociaciones de desarrollo de productos (PDP). [65] Una asociación público-privada es un acuerdo entre una o más entidades públicas y una o más entidades privadas que existe para lograr un resultado de salud específico o producir un producto sanitario. La asociación puede existir de numerosas maneras; podrán compartir e intercambiar fondos, propiedades, equipos, recursos humanos y propiedad intelectual. Estas asociaciones público-privadas y asociaciones para el desarrollo de productos se han establecido para abordar los desafíos de la industria farmacéutica, especialmente los relacionados con la investigación de enfermedades desatendidas. Estas asociaciones pueden ayudar a aumentar la escala del esfuerzo hacia el desarrollo terapéutico mediante el uso de diferentes conocimientos, habilidades y experiencia de diferentes fuentes. Se ha demostrado que este tipo de asociaciones son más efectivas que la industria o los grupos públicos que trabajan de forma independiente. [67]
El tripanosoma tanto del tipo rhodesiense como gambiense puede afectar a otros animales como el ganado vacuno y los animales salvajes. [1] La tripanosomiasis africana generalmente se ha considerado una enfermedad antroponótica y, por lo tanto, su programa de control se centró principalmente en detener la transmisión mediante el tratamiento de casos humanos y la eliminación del vector. Sin embargo, se informó que los reservorios animales posiblemente desempeñaran un papel importante en la naturaleza endémica de la tripanosomiasis africana y en su resurgimiento en los focos históricos de África occidental y central. [68] [69]
Véanse las págs. 154-5