
En fisiología cardíaca , el gasto cardíaco ( CO ), también conocido como gasto cardíaco y a menudo denotado por los símbolos , o , [2] es el caudal volumétrico del rendimiento de bombeo del corazón : es decir, el volumen de sangre que se bombea. por un solo ventrículo del corazón, por unidad de tiempo (generalmente medido por minuto). El gasto cardíaco (CO) es el producto de la frecuencia cardíaca (FC), es decir, el número de latidos por minuto (lpm), y el volumen sistólico (SV), que es el volumen de sangre bombeada desde el ventrículo izquierdo por latido; dando así la fórmula:
Los valores del gasto cardíaco generalmente se expresan en L/min. Para un individuo sano que pesa 70 kg, el gasto cardíaco en reposo promedia unos 5 L/min; suponiendo una frecuencia cardíaca de 70 latidos/min, el volumen sistólico sería de aproximadamente 70 ml.
Debido a que el gasto cardíaco está relacionado con la cantidad de sangre que llega a diversas partes del cuerpo, es un componente importante de la eficacia con la que el corazón puede satisfacer las demandas del cuerpo para mantener una perfusión tisular adecuada . Los tejidos corporales requieren un suministro continuo de oxígeno, lo que requiere el transporte sostenido de oxígeno a los tejidos mediante la circulación sistémica de sangre oxigenada a una presión adecuada desde el ventrículo izquierdo del corazón a través de la aorta y las arterias. El suministro de oxígeno (DO 2 ml/min) es el resultado del flujo sanguíneo (gasto cardíaco CO) multiplicado por el contenido de oxígeno en sangre (CaO 2 ). Matemáticamente esto se calcula de la siguiente manera: aporte de oxígeno = gasto cardíaco × contenido de oxígeno arterial, dando la fórmula:
Con un gasto cardíaco en reposo de 5 L/min, un suministro de oxígeno "normal" es de alrededor de 1 L/min. La cantidad/porcentaje de oxígeno circulado consumido (VO 2 ) por minuto a través del metabolismo varía según el nivel de actividad, pero en reposo es aproximadamente el 25 % del DO 2 . El ejercicio físico requiere un nivel de consumo de oxígeno superior al del reposo para favorecer una mayor actividad muscular. En el caso de insuficiencia cardíaca , el CO real puede ser insuficiente para soportar incluso las actividades más sencillas de la vida diaria; ni puede aumentar lo suficiente para satisfacer las mayores demandas metabólicas derivadas incluso del ejercicio moderado.
El gasto cardíaco es un parámetro del flujo sanguíneo global de interés en hemodinámica , el estudio del flujo sanguíneo. Los factores que afectan el volumen sistólico y la frecuencia cardíaca también afectan el gasto cardíaco. La figura del margen derecho ilustra esta dependencia y enumera algunos de estos factores. En la figura siguiente se proporciona una ilustración jerárquica detallada.
Existen muchos métodos para medir el CO, tanto de forma invasiva como no invasiva; cada uno tiene ventajas e inconvenientes, como se describe a continuación.
La función del corazón es impulsar la sangre a través del sistema circulatorio en un ciclo que entrega oxígeno, nutrientes y sustancias químicas a las células del cuerpo y elimina los desechos celulares. Debido a que bombea toda la sangre que regresa desde el sistema venoso , la cantidad de sangre que regresa al corazón determina efectivamente la cantidad de sangre que el corazón bombea: su gasto cardíaco , Q. El gasto cardíaco se define clásicamente junto con el volumen sistólico (SV) y la frecuencia cardíaca (FC) como: [ cita necesaria ]
Al estandarizar qué valores de CO se consideran dentro del rango normal independientemente del tamaño del cuerpo del sujeto, la convención aceptada es indexar aún más la ecuación ( 1 ) utilizando el área de superficie corporal (BSA), dando lugar al índice cardíaco (IC). Esto se detalla en la ecuación ( 2 ) a continuación.
Existen varios métodos clínicos para medir el gasto cardíaco, que van desde el cateterismo intracardíaco directo hasta la medición no invasiva del pulso arterial. Cada método tiene ventajas y desventajas. La comparación relativa está limitada por la ausencia de una medida "estándar de oro" ampliamente aceptada. El gasto cardíaco también puede verse afectado significativamente por la fase de la respiración: los cambios de presión intratorácica influyen en el llenado diastólico y, por tanto, en el gasto cardíaco. Esto es especialmente importante durante la ventilación mecánica, en la que el gasto cardíaco puede variar hasta un 50% en un solo ciclo respiratorio. [ cita necesaria ] Por lo tanto, el gasto cardíaco debe medirse en puntos espaciados uniformemente durante un solo ciclo o promediarse durante varios ciclos. [ cita necesaria ]
Los métodos invasivos son bien aceptados, pero cada vez hay más pruebas de que no son precisos ni eficaces para guiar la terapia. En consecuencia, está creciendo el interés en el desarrollo de métodos no invasivos. [5] [6] [7]
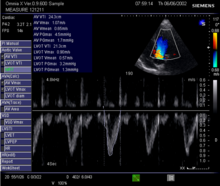
Este método utiliza ultrasonido y el efecto Doppler para medir el gasto cardíaco. La velocidad de la sangre a través del corazón provoca un cambio Doppler en la frecuencia de las ondas de ultrasonido que regresan. Este cambio luego se puede utilizar para calcular la velocidad y el volumen del flujo, y efectivamente el gasto cardíaco, utilizando las siguientes ecuaciones: [ cita necesaria ]
dónde:
Al ser no invasiva, precisa y económica, la ecografía Doppler es una parte rutinaria de la ecografía clínica; tiene altos niveles de confiabilidad y reproducibilidad y ha estado en uso clínico desde la década de 1960. [ cita necesaria ]
La ecocardiografía es un método no invasivo para cuantificar el gasto cardíaco mediante ultrasonido. La ecografía bidimensional (2D) y las mediciones Doppler se utilizan juntas para calcular el gasto cardíaco. La medición 2D del diámetro (d) del anillo aórtico permite calcular el área de la sección transversal del flujo (CSA), que luego se multiplica por el VTI del perfil de flujo Doppler a través de la válvula aórtica para determinar el volumen de flujo por latido ( carrera) . volumen , SV). Luego, el resultado se multiplica por la frecuencia cardíaca (FC) para obtener el gasto cardíaco. Aunque se utiliza en medicina clínica, tiene una amplia variabilidad entre pruebas y pruebas. [8] Se dice que requiere una amplia formación y habilidad, pero nunca se han revelado los pasos exactos necesarios para lograr una precisión clínicamente adecuada. La medición 2D del diámetro de la válvula aórtica es una fuente de ruido; otros son variaciones latido a latido en el volumen sistólico y diferencias sutiles en la posición de la sonda. Una alternativa que no es necesariamente más reproducible es la medición de la válvula pulmonar para calcular el CO del lado derecho. Aunque es de uso generalizado, la técnica requiere mucho tiempo y está limitada por la reproducibilidad de los elementos que la componen. En la forma utilizada en la práctica clínica, la precisión de SV y CO es del orden de ±20%. [ cita necesaria ]
El monitor ultrasónico de gasto cardíaco (USCOM) utiliza Doppler de onda continua para medir el perfil de flujo Doppler VTI. Utiliza la antropometría para calcular los diámetros de las válvulas aórtica y pulmonar y los CSA, lo que permite realizar mediciones de Q en el lado derecho e izquierdo . En comparación con el método ecocardiográfico, USCOM mejora significativamente la reproducibilidad y aumenta la sensibilidad de la detección de cambios en el flujo. El seguimiento automático en tiempo real del perfil de flujo Doppler permite mediciones Q latido a latido del lado derecho e izquierdo , simplificando la operación y reduciendo el tiempo de adquisición en comparación con la ecocardiografía convencional. USCOM ha sido validado desde 0,12 L/min hasta 18,7 L/min [9] en recién nacidos, [10] niños [11] y adultos. [12] El método se puede aplicar con igual precisión a pacientes de todas las edades para el desarrollo de protocolos hemodinámicos fisiológicamente racionales. USCOM es el único método de medición del gasto cardíaco que ha logrado una precisión equivalente a la de la sonda de flujo implantable. [13] Esta precisión ha garantizado altos niveles de uso clínico en afecciones que incluyen sepsis, insuficiencia cardíaca e hipertensión. [14] [15] [16]

El Doppler transesofágico incluye dos tecnologías principales; ecocardiograma transesofágico , que se utiliza principalmente con fines de diagnóstico, y monitorización Doppler esofágica , que se utiliza principalmente para la monitorización clínica del gasto cardíaco. Este último utiliza Doppler de onda continua para medir la velocidad de la sangre en la aorta torácica descendente . Se inserta una sonda de ultrasonido por vía oral o nasal en el esófago hasta el nivel torácico medio, punto en el que el esófago se encuentra junto a la aorta torácica descendente . Debido a que el transductor está cerca del flujo sanguíneo, la señal es clara. Es posible que sea necesario volver a enfocar la sonda para garantizar una señal óptima. Este método tiene buena validación, se usa ampliamente para el manejo de líquidos durante la cirugía y hay evidencia de mejores resultados para los pacientes, [17] [18] [19] [20] [21] [22] [23] [24] y ha sido recomendado por Instituto Nacional para la Salud y la Excelencia Clínica ( NICE ) del Reino Unido. [25] La monitorización Doppler esofágica mide la velocidad de la sangre y no el Q verdadero , por lo tanto se basa en un nomograma [26] basado en la edad, la altura y el peso del paciente para convertir la velocidad medida en volumen sistólico y gasto cardíaco. Este método generalmente requiere sedación del paciente y está aceptado para su uso tanto en adultos como en niños. [ cita necesaria ]
Los métodos de presión de pulso (PP) miden la presión en una arteria a lo largo del tiempo para derivar una forma de onda y utilizar esta información para calcular el rendimiento cardíaco. Sin embargo, cualquier medida de la arteria incluye cambios en la presión asociados con cambios en la función arterial, por ejemplo distensibilidad e impedancia. Se supone que los cambios fisiológicos o terapéuticos en el diámetro del vaso reflejan cambios en Q. Los métodos PP miden el rendimiento combinado del corazón y los vasos sanguíneos, lo que limita su aplicación para la medición de Q. Esto se puede compensar parcialmente mediante la calibración intermitente de la forma de onda con otro método de medición Q y luego monitoreando la forma de onda PP. Idealmente, la forma de onda PP debería calibrarse latido a latido. Existen métodos invasivos y no invasivos para medir la PP. [ cita necesaria ]
En 1967, el fisiólogo checo Jan Peňáz inventó y patentó el método de pinza de volumen para medir la presión arterial continua. El principio del método de pinzamiento de volumen es proporcionar dinámicamente presiones iguales a ambos lados de la pared arterial. Al sujetar la arteria a un volumen determinado, la presión interior (presión intraarterial) equilibra la presión exterior (presión del manguito del dedo). Peñáz decidió que el dedo era el sitio óptimo para aplicar este método de pinza de volumen. El uso de manguitos para los dedos excluye la aplicación del dispositivo en pacientes sin vasoconstricción, como en pacientes con sepsis o en pacientes que toman vasopresores. [ cita necesaria ]
En 1978, los científicos de BMI-TNO, la unidad de investigación de la Organización Holandesa para la Investigación Científica Aplicada de la Universidad de Amsterdam , inventaron y patentaron una serie de elementos clave adicionales que hacen que la pinza de volumen funcione en la práctica clínica. Estos métodos incluyen el uso de luz infrarroja modulada en el sistema óptico dentro del sensor, el brazalete liviano y fácil de envolver con fijación de velcro , un nuevo principio de válvula de control proporcional neumática y una estrategia de punto de ajuste para determinar y rastrear el Volumen correcto al que sujetar las arterias de los dedos: el sistema físico. Acrónimo de calibración fisiológica de las arterias de los dedos, se descubrió que este rastreador Physiocal es preciso, robusto y confiable. [ cita necesaria ]
La metodología Finapres se desarrolló para utilizar esta información para calcular la presión arterial a partir de los datos de presión del manguito para el dedo. Se desarrolló un algoritmo generalizado para corregir la diferencia del nivel de presión entre el dedo y el brazo en los pacientes. Esta corrección funcionó en todas las circunstancias en las que se probó, incluso cuando no fue diseñada para ello, porque aplicaba principios fisiológicos generales. Este innovador método de reconstrucción de la forma de onda de presión braquial se implementó por primera vez en el Finometer, el sucesor de Finapres que BMI-TNO introdujo en el mercado en 2000. [ cita necesaria ]
La disponibilidad de una forma de onda de presión arterial calibrada, continua y de alta fidelidad abrió la perspectiva del cálculo latido a latido de la hemodinámica integrada, basado en dos nociones: la presión y el flujo están interrelacionados en cada sitio del sistema arterial por su la llamada impedancia característica. En el sitio aórtico proximal, el modelo Windkessel de 3 elementos de esta impedancia se puede modelar con suficiente precisión en un paciente individual con edad, sexo, altura y peso conocidos. Según comparaciones de monitores vasculares periféricos no invasivos, la utilidad clínica modesta está restringida a pacientes con circulación normal e invariable. [27]
La monitorización invasiva de PP implica insertar un sensor de presión manómetro en una arteria (generalmente la arteria radial o femoral ) y medir continuamente la forma de onda de PP. Esto generalmente se hace conectando el catéter a un dispositivo de procesamiento de señales con una pantalla. Luego se puede analizar la forma de onda PP para proporcionar mediciones del rendimiento cardiovascular. Los cambios en la función vascular, la posición de la punta del catéter o la amortiguación de la señal de la forma de onda de presión afectarán la precisión de las lecturas. Las mediciones invasivas de PP se pueden calibrar o descalibrar. [ cita necesaria ]
PiCCO (PULSION Medical Systems AG, Munich, Alemania) y PulseCO (LiDCO Ltd, Londres, Inglaterra) generan Q continuo analizando la forma de onda PP arterial. En ambos casos, se requiere una técnica independiente para proporcionar la calibración del análisis Q continuo porque el análisis de PP arterial no puede tener en cuenta variables no medidas, como la distensibilidad cambiante del lecho vascular. Se recomienda la recalibración después de cambios en la posición, terapia o condición del paciente. [ cita necesaria ]
En PiCCO, la termodilución transpulmonar, que utiliza el principio de Stewart-Hamilton pero mide los cambios de temperatura desde la línea venosa central a una línea arterial central, es decir, la línea arterial femoral o axilar, se utiliza como técnica de calibración. El valor Q derivado de la termodilución salina fría se utiliza para calibrar el contorno de PP arterial, que luego puede proporcionar una monitorización Q continua . El algoritmo PiCCO depende de la morfología de la forma de onda de la presión arterial (análisis matemático de la forma de onda PP) y calcula el Q continuo como lo describen Wesseling y sus colegas. [28] La termodilución transpulmonar abarca el corazón derecho, la circulación pulmonar y el corazón izquierdo, lo que permite un análisis matemático adicional de la curva de termodilución y proporciona mediciones de los volúmenes de llenado cardíaco ( GEDV ), el volumen de sangre intratorácica y el agua pulmonar extravascular. La termodilución transpulmonar permite una calibración Q menos invasiva , pero es menos precisa que la termodilución PA y requiere una vía venosa y arterial central con los riesgos de infección que la acompañan. [ cita necesaria ]
En LiDCO, la técnica de calibración independiente es la dilución con cloruro de litio utilizando el principio de Stewart-Hamilton. La dilución con cloruro de litio utiliza una vena periférica y una vía arterial periférica. Al igual que PiCCO, se recomienda una calibración frecuente cuando hay un cambio en Q. [29] Los eventos de calibración tienen una frecuencia limitada porque implican la inyección de cloruro de litio y pueden estar sujetos a errores en presencia de ciertos relajantes musculares. El algoritmo PulseCO utilizado por LiDCO se basa en la derivación de potencia del pulso y no depende de la morfología de la forma de onda. [ cita necesaria ]

FloTrac/Vigileo ( Edwards Lifesciences ) es un monitor hemodinámico no calibrado basado en el análisis del contorno del pulso. Estima el gasto cardíaco ( Q ) utilizando un catéter arterial estándar con un manómetro ubicado en la arteria femoral o radial. El dispositivo consta de un transductor de presión de alta fidelidad que, cuando se utiliza con un monitor de soporte (monitor Vigileo o EV1000), deriva el gasto cardíaco izquierdo ( Q ) a partir de una muestra de pulsaciones arteriales. El dispositivo utiliza un algoritmo basado en la ley del corazón de Frank-Starling , que establece que la presión del pulso (PP) es proporcional al volumen sistólico (SV). El algoritmo calcula el producto de la desviación estándar de la onda de presión arterial (AP) durante un período de muestreo de 20 segundos y un factor de tono vascular (Khi o χ) para generar el volumen sistólico. La ecuación en forma simplificada es: , o, . Khi está diseñado para reflejar la resistencia arterial; la distensibilidad es una ecuación polinómica multivariada que cuantifica continuamente la distensibilidad arterial y la resistencia vascular. Khi hace esto analizando los cambios morfológicos de las formas de onda de la presión arterial poco a poco, basándose en el principio de que los cambios en la distensibilidad o la resistencia afectan la forma de la forma de onda de la presión arterial. Analizando la forma de dichas ondas se evalúa el efecto del tono vascular, permitiendo el cálculo del SV. Luego, Q se deriva usando la ecuación ( 1 ). En la FC sólo se cuentan los latidos perfundidos que generan una forma de onda arterial. [ cita necesaria ]
Este sistema estima Q utilizando un catéter arterial existente con precisión variable. Estos monitores arteriales no requieren cateterismo intracardíaco desde un catéter de arteria pulmonar. Requieren una vía arterial y, por tanto, son invasivos. Al igual que con otros sistemas de forma de onda arterial, los cortos tiempos de configuración y adquisición de datos son beneficios de esta tecnología. Las desventajas incluyen su incapacidad para proporcionar datos sobre las presiones cardíacas del lado derecho o la saturación de oxígeno venoso mixto. [30] [31] La medición de la variación del volumen sistólico (SVV), que predice la capacidad de respuesta del volumen, es intrínseca a todas las tecnologías de formas de onda arterial. Se utiliza para gestionar la optimización de líquidos en pacientes quirúrgicos o críticamente enfermos de alto riesgo. Se ha publicado un programa de optimización fisiológica basado en principios hemodinámicos que incorpora los pares de datos SV y SVV. [32]
Los sistemas de monitorización arterial no pueden predecir cambios en el tono vascular; estiman cambios en la distensibilidad vascular. La medición de la presión en la arteria para calcular el flujo en el corazón es fisiológicamente irracional y de precisión cuestionable [33] y de beneficio no demostrado. [34] La monitorización de la presión arterial está limitada en pacientes sin ventilación, en fibrilación auricular, en pacientes que toman vasopresores y en aquellos con un sistema autónomo dinámico, como aquellos con sepsis. [29]
El Método Analítico de Registro de Presión (PRAM), estima Q a partir del análisis del perfil de onda de presión obtenido de un catéter arterial, acceso radial o femoral. Esta forma de onda PP se puede utilizar para determinar Q. A medida que la forma de onda se muestrea a 1000 Hz, la curva de presión detectada se puede medir para calcular el volumen sistólico real latido a latido. A diferencia de FloTrac, no se necesitan valores constantes de impedancia de calibración externa ni datos preestimados in vivo o in vitro .
PRAM ha sido validado frente a los métodos considerados estándar de oro en condiciones estables [35] y en diversos estados hemodinámicos. [36] Puede usarse para monitorear pacientes pediátricos y con soporte mecánico. [37] [38]
PRAM proporciona valores hemodinámicos generalmente monitoreados, parámetros de respuesta a los fluidos y una referencia exclusiva: Eficiencia del ciclo cardíaco (CCE). Se expresa mediante un número puro que oscila entre 1 (mejor) y -1 (peor) e indica el acoplamiento general de la respuesta corazón-vascular. La relación entre el rendimiento cardíaco y la energía consumida, representada como "índice de estrés" CCE, puede ser de suma importancia para comprender la evolución presente y futura del paciente. [39]
La cardiografía de impedancia (a menudo abreviada como ICG o bioimpedancia eléctrica torácica (TEB)) mide los cambios en la impedancia eléctrica en la región torácica durante el ciclo cardíaco. Una impedancia más baja indica un mayor volumen de líquido intratorácico y flujo sanguíneo. Al sincronizar los cambios en el volumen de líquido con los latidos del corazón, el cambio en la impedancia se puede utilizar para calcular el volumen sistólico, el gasto cardíaco y la resistencia vascular sistémica. [40]
Se utilizan enfoques tanto invasivos como no invasivos. [41] La confiabilidad y validez del enfoque no invasivo ha ganado cierta aceptación, [42] [43] [44] [45] aunque no hay un acuerdo completo sobre este punto. [46] El uso clínico de este enfoque en el diagnóstico, pronóstico y tratamiento de una variedad de enfermedades continúa. [47]
El equipo ICG no invasivo incluye los productos Bio-Z Dx, [48] Niccomo, [49] y TEBCO de BoMed. [50] [51]
La dilución por ultrasonido (UD) utiliza solución salina normal (NS) a temperatura corporal como indicador introducido en un circuito extracorpóreo para crear una circulación auriculoventricular (AV) con un sensor de ultrasonido, que se utiliza para medir la dilución y luego calcular el gasto cardíaco utilizando un sistema patentado. algoritmo. Con este método se pueden calcular otras variables hemodinámicas, como el volumen total al final de la diástole (TEDV), el volumen sanguíneo central (CBV) y el volumen de circulación activa (ACVI). [ cita necesaria ]
El método UD se introdujo por primera vez en 1995. [52] Se utilizó ampliamente para medir flujo y volúmenes con condiciones de circuito extracorpóreo, como ECMO [53] [54] y hemodiálisis , [55] [56] liderando más de 150 estudios revisados por pares. publicaciones. UD ahora se ha adaptado a las unidades de cuidados intensivos (UCI) como dispositivo COstatus. [57]
El método UD se basa en la dilución del indicador ultrasónico. [58] La velocidad del ultrasonido sanguíneo (1560–1585 m/s) es una función de la concentración total de proteínas en la sangre (sumas de proteínas en el plasma y en los glóbulos rojos) y la temperatura. La inyección de solución salina normal a temperatura corporal (la velocidad del ultrasonido de la solución salina es de 1533 m/s) en un circuito AV único disminuye la velocidad del ultrasonido en la sangre y produce curvas de dilución. [ cita necesaria ]
La UD requiere el establecimiento de una circulación extracorpórea a través de su circuito AV único con dos líneas arteriales y venosas centrales preexistentes en pacientes de la UCI. Cuando se inyecta el indicador de solución salina en el bucle AV, el sensor de pinza venosa del bucle lo detecta antes de que entre en la aurícula derecha del corazón del paciente. Después de que el indicador atraviesa el corazón y los pulmones, la curva de concentración en la línea arterial se registra y se muestra en el monitor COstatus HCM101. El gasto cardíaco se calcula a partir del área de la curva de concentración mediante la ecuación de Stewart-Hamilton. La UD es un procedimiento no invasivo que solo requiere una conexión al bucle AV y dos líneas de un paciente. La UD se ha especializado para su aplicación en pacientes pediátricos de la UCI y se ha demostrado que es relativamente segura aunque invasiva y reproducible. [ cita necesaria ]

La cardiometría eléctrica es un método no invasivo similar a la cardiografía por impedancia; Ambos métodos miden la bioimpedancia eléctrica torácica (TEB). El modelo subyacente difiere entre los dos métodos; La cardiometría eléctrica atribuye el fuerte aumento de TEB latido a latido al cambio en la orientación de los glóbulos rojos. Se necesitan cuatro electrodos de ECG estándar para medir el gasto cardíaco. La cardiometría eléctrica es un método registrado por Cardiotronic, Inc. y muestra resultados prometedores en una amplia gama de pacientes. Actualmente está aprobado en EE. UU. para su uso en adultos, niños y bebés. Los monitores de cardiometría eléctrica se han mostrado prometedores en pacientes quirúrgicos cardíacos posoperatorios, tanto en casos hemodinámicamente estables como inestables. [59]
Contraste de fase codificado por velocidad La resonancia magnética (MRI) [60] es la técnica más precisa para medir el flujo en grandes vasos en mamíferos. Se ha demostrado que las mediciones de flujo por resonancia magnética son muy precisas en comparación con las mediciones realizadas con un vaso de precipitados y un temporizador, [61] y menos variables que el principio de Fick [62] y la termodilución. [63]
La resonancia magnética codificada por velocidad se basa en la detección de cambios en la fase de precesión de protones . Estos cambios son proporcionales a la velocidad del movimiento de los protones a través de un campo magnético con un gradiente conocido. Cuando se utiliza resonancia magnética codificada por velocidad, el resultado son dos conjuntos de imágenes, uno para cada punto temporal del ciclo cardíaco. Una es una imagen anatómica y la otra es una imagen en la que la intensidad de la señal en cada píxel es directamente proporcional a la velocidad a través del plano. La velocidad promedio en un vaso, es decir, la aorta o la arteria pulmonar , se cuantifica midiendo la intensidad de señal promedio de los píxeles en la sección transversal del vaso y luego multiplicándola por una constante conocida. El flujo se calcula multiplicando la velocidad media por el área de la sección transversal del recipiente. Estos datos de flujo se pueden utilizar en un gráfico de flujo versus tiempo. El área bajo la curva de flujo versus tiempo para un ciclo cardíaco es el volumen sistólico. La duración del ciclo cardíaco se conoce y determina la frecuencia cardíaca; Q se puede calcular usando la ecuación ( 1 ). La resonancia magnética se utiliza normalmente para cuantificar el flujo durante un ciclo cardíaco como el promedio de varios latidos del corazón. También es posible cuantificar el volumen sistólico en tiempo real latido a latido. [64]
Si bien la resonancia magnética es una herramienta de investigación importante para medir Q con precisión , actualmente no se utiliza clínicamente para la monitorización hemodinámica en entornos de emergencia o cuidados intensivos. A partir de 2015 [actualizar], la medición del gasto cardíaco mediante resonancia magnética se utiliza de forma rutinaria en los exámenes clínicos de resonancia magnética cardíaca. [sesenta y cinco]
El método de dilución del tinte se realiza inyectando rápidamente un tinte, verde de indocianina , en la aurícula derecha del corazón. El tinte fluye con la sangre hacia la aorta. Se inserta una sonda en la aorta para medir la concentración del tinte que sale del corazón en intervalos de tiempo iguales [0, T ] hasta que el tinte se haya aclarado. Sea c ( t) la concentración del tinte en el tiempo t . Al dividir los intervalos de tiempo de [0, T ] en subintervalos Δ t , la cantidad de tinte que fluye más allá del punto de medición durante el subintervalo de a es:
¿Dónde está el caudal que se está calculando? La cantidad total de tinte es:
y dejando , la cantidad de tinte es:
Así, el gasto cardíaco viene dado por:
donde se conoce la cantidad de tinte inyectado y la integral se puede determinar utilizando las lecturas de concentración. [66]
El método de dilución del tinte es uno de los métodos más precisos para determinar el gasto cardíaco durante el ejercicio. El error de un único cálculo de los valores del gasto cardíaco en reposo y durante el ejercicio es inferior al 5%. Este método no permite la medición de cambios 'latido a latido' y requiere un gasto cardíaco que sea estable durante aproximadamente 10 s durante el ejercicio y 30 s en reposo. [ cita necesaria ]

El gasto cardíaco está controlado principalmente por las necesidades de oxígeno de los tejidos del cuerpo. A diferencia de otros sistemas de bombeo , el corazón es una bomba de demanda que no regula su propio gasto. [67] Cuando el cuerpo tiene una alta demanda metabólica de oxígeno, el flujo metabólicamente controlado a través de los tejidos aumenta, lo que lleva a un mayor flujo de sangre de regreso al corazón, lo que genera un mayor gasto cardíaco.
La capacitancia, también conocida como distensibilidad, de los canales arteriovasculares que transportan la sangre también controla el gasto cardíaco. A medida que los vasos sanguíneos del cuerpo se expanden y contraen activamente, la resistencia al flujo sanguíneo disminuye y aumenta respectivamente. Las venas de paredes delgadas tienen aproximadamente dieciocho veces la capacitancia de las arterias de paredes gruesas porque pueden transportar más sangre al ser más distensibles. [68]
A partir de esta fórmula, queda claro que los factores que afectan el volumen sistólico y la frecuencia cardíaca también afectan el gasto cardíaco. La figura de la derecha ilustra esta dependencia y enumera algunos de estos factores. En la figura siguiente se proporciona una ilustración jerárquica más detallada.
La ecuación ( 1 ) revela que la FC y el SV son los principales determinantes del gasto cardíaco Q. En la figura de la derecha se ilustra una representación detallada de estos factores. Los principales factores que influyen en la FC son la inervación autónoma más el control endocrino . No se muestran los factores ambientales, como electrolitos, productos metabólicos y temperatura. Los determinantes del VS durante el ciclo cardíaco son la contractilidad del músculo cardíaco, el grado de precarga de distensión miocárdica antes del acortamiento y la poscarga durante la eyección. [69] Otros factores, como los electrolitos, pueden clasificarse como agentes inotrópicos positivos o negativos. [70]
Cuando Q aumenta en un individuo sano pero no entrenado, la mayor parte del aumento puede atribuirse a un aumento de la frecuencia cardíaca (FC). El cambio de postura, el aumento de la actividad del sistema nervioso simpático y la disminución de la actividad del sistema nervioso parasimpático también pueden aumentar el gasto cardíaco. La FC puede variar en un factor de aproximadamente 3 (entre 60 y 180 latidos por minuto), mientras que el volumen sistólico (SV) puede variar entre 70 y 120 ml (2,5 y 4,2 imp fl oz; 2,4 y 4,1 US fl oz), un factor de sólo 1,7. [71] [72] [73]
Las enfermedades del sistema cardiovascular suelen estar asociadas con cambios en el Q , en particular las enfermedades pandémicas, la hipertensión y la insuficiencia cardíaca . El aumento de Q puede estar asociado con enfermedades cardiovasculares que pueden ocurrir durante una infección y sepsis. La disminución de Q puede estar asociada con miocardiopatía e insuficiencia cardíaca. [69] A veces, en presencia de enfermedad ventricular asociada con dilatación , la VFD puede variar. Un aumento en el EDV podría contrarrestar la dilatación del VI y la contracción alterada. A partir de la ecuación ( 3 ), el gasto cardíaco resultante Q puede permanecer constante. La capacidad de medir Q con precisión es importante en la medicina clínica porque proporciona un mejor diagnóstico de anomalías y puede usarse para guiar el tratamiento adecuado. [74]
La fracción de eyección (EF) es un parámetro relacionado con la SV. La FE es la fracción de sangre eyectada por el ventrículo izquierdo (VI) durante la fase de contracción o eyección del ciclo cardíaco o sístole . Antes del inicio de la sístole, durante la fase de llenado ( diástole ), el VI se llena de sangre hasta la capacidad conocida como volumen diastólico final (VED). Durante la sístole, el VI se contrae y expulsa sangre hasta alcanzar su capacidad mínima conocida como volumen sistólico final (ESV). No se vacía del todo. Las siguientes ecuaciones ayudan a traducir el efecto de EF y EDV sobre el gasto cardíaco Q, a través de SV.
El gasto cardíaco (IC) es la operación inversa del gasto cardíaco. Como el gasto cardíaco implica la expresión volumétrica de la fracción de eyección, el gasto cardíaco implica la fracción volumétrica de inyección (IF).
IF = volumen telediastólico (EDV) / volumen final sistólico (ESV)
El gasto cardíaco es un modelo matemático de diástole que se puede visualizar fácilmente. [ se necesita aclaración ]
En todos los mamíferos en reposo de masa normal, el valor de CO es una función lineal de la masa corporal con una pendiente de 0,1 L/(kg min). [79] [80] La grasa tiene aproximadamente el 65% de la demanda de oxígeno por masa en comparación con otros tejidos corporales magros. Como resultado, el cálculo del valor normal de CO en un sujeto obeso es más complejo; No puede existir un valor "normal" único y común de SV y CO para adultos. Todos los parámetros del flujo sanguíneo deben estar indexados. Se acepta por convención indexarlos por el área de superficie corporal, BSA [m 2 ], mediante la fórmula de DuBois & DuBois, en función de la altura y el peso:
Los parámetros indexados resultantes son el índice de accidente cerebrovascular (SI) y el índice cardíaco (CI). El índice sistólico, medido en ml/latido/m 2 , se define como
El índice cardíaco, medido en L/(min m 2 ), se define como
La ecuación de CO ( 1 ) para parámetros indexados cambia a lo siguiente.
El rango normal para estos parámetros de flujo sanguíneo indexados está entre 35 y 65 ml/latido/m 2 para SI y entre 2,5 y 4 L/(min m 2 ) para CI. [81]
El gasto cardíaco combinado es la suma de los gastos de los lados derecho e izquierdo del corazón. Es una medición útil en la circulación fetal , donde el gasto cardíaco de ambos lados del corazón funciona parcialmente en paralelo a través del agujero oval y el conducto arterioso , que irrigan directamente la circulación sistémica . [82]
El principio de Fick, descrito por primera vez por Adolf Eugen Fick en 1870, supone que la tasa de consumo de oxígeno es función de la tasa de flujo sanguíneo y la tasa de oxígeno captado por los glóbulos rojos. La aplicación del principio de Fick implica calcular el oxígeno consumido a lo largo del tiempo midiendo la concentración de oxígeno en la sangre venosa y arterial. Q se calcula a partir de estas mediciones de la siguiente manera:
De estos valores sabemos que:
dónde
Esto nos permite decir
y por lo tanto calcular Q . ( C A – C V ) también se conoce como diferencia arteriovenosa de oxígeno . [ cita necesaria ]
Si bien se considera el método más preciso para medir Q , el método de Fick es invasivo y requiere tiempo para el análisis de la muestra, y es difícil adquirir muestras precisas del consumo de oxígeno. Ha habido modificaciones al método de Fick donde el contenido de oxígeno respiratorio se mide como parte de un sistema cerrado y el oxígeno consumido se calcula utilizando un índice de consumo de oxígeno supuesto, que luego se usa para calcular Q. Otras variaciones utilizan gases inertes como trazadores y miden el cambio en las concentraciones de gas inspirado y espirado para calcular Q (Innocor, Innovision A/S, Dinamarca).
El cálculo del contenido de oxígeno arterial y venoso de la sangre es un proceso sencillo. Casi todo el oxígeno de la sangre está unido a las moléculas de hemoglobina de los glóbulos rojos. Medir el contenido de hemoglobina en la sangre y el porcentaje de saturación de hemoglobina (la saturación de oxígeno de la sangre) es un proceso simple y está fácilmente disponible para los médicos. Cada gramo de hemoglobina puede transportar 1,34 ml de O 2 ; El contenido de oxígeno de la sangre, ya sea arterial o venosa, se puede estimar mediante la siguiente fórmula:

El método indicador se desarrolló aún más reemplazando el tinte indicador con fluido calentado o enfriado. Los cambios de temperatura, en lugar de la concentración de tinte, se miden en los sitios de la circulación; este método se conoce como termodilución. El catéter de arteria pulmonar (PAC) introducido en la práctica clínica en 1970, también conocido como catéter de Swan-Ganz , proporciona acceso directo al corazón derecho para mediciones de termodilución. La monitorización cardíaca continua e invasiva en las unidades de cuidados intensivos se ha eliminado en su mayor parte. El PAC sigue siendo útil en el estudio del corazón derecho realizado en laboratorios de cateterismo cardíaco. [ cita necesaria ]
El PAC tiene un globo en la punta y se infla, lo que ayuda a "navegar" el globo del catéter a través del ventrículo derecho para ocluir una pequeña rama del sistema de la arteria pulmonar. Luego se desinfla el globo. El método de termodilución PAC implica la inyección de una pequeña cantidad (10 ml) de glucosa fría a una temperatura conocida en la arteria pulmonar y la medición de la temperatura a una distancia conocida de 6 a 10 cm (2,4 a 3,9 pulgadas) utilizando el mismo catéter con medidor de temperatura. sensores separados a una distancia conocida. [ cita necesaria ]
El catéter multilumen de Swan-Ganz, de importancia histórica, permite el cálculo reproducible del gasto cardíaco a partir de una curva de tiempo-temperatura medida, también conocida como curva de termodilución. La tecnología de termistor permitió observar que el CO bajo registra cambios de temperatura lentamente y el CO alto registra cambios de temperatura rápidamente. El grado de cambio de temperatura es directamente proporcional al gasto cardíaco. En este método único, generalmente se promedian tres o cuatro mediciones o pases repetidos para mejorar la precisión. [83] [84] Los catéteres modernos están equipados con filamentos calefactores que se calientan de forma intermitente y miden la curva de termodilución, proporcionando mediciones Q en serie . Estos instrumentos promedian las mediciones durante 2 a 9 minutos dependiendo de la estabilidad de la circulación y, por lo tanto, no proporcionan un monitoreo continuo.
El uso de PAC puede complicarse con arritmias, infecciones, rotura de la arteria pulmonar y daño a la válvula cardíaca derecha. Estudios recientes en pacientes con enfermedades críticas, sepsis, insuficiencia respiratoria aguda e insuficiencia cardíaca sugieren que el uso del PAC no mejora los resultados de los pacientes. [5] [6] [7] Esta ineficacia clínica puede estar relacionada con su escasa precisión y sensibilidad, que se han demostrado en comparación con sondas de flujo en un rango seis veces mayor de valores Q. [13] El uso de PAC está en declive a medida que los médicos avanzan hacia tecnologías menos invasivas y más precisas para monitorear la hemodinámica. [85]
{{cite web}}: Falta o está vacía |url=( ayuda ) en "OP 564–605". Medicina de Cuidados Intensivos . 31 (Suplemento 1): S148–58. 2005. doi :10.1007/s00134-005-2781-3. S2CID 30752685.