
La humectación es la capacidad de un líquido de mantener contacto con una superficie sólida , resultante de interacciones intermoleculares cuando ambas se juntan. [1] Esto sucede en presencia de una fase gaseosa u otra fase líquida no miscible con la primera. El grado de humectación (humectabilidad) está determinado por un equilibrio de fuerzas entre las fuerzas adhesivas y cohesivas . Hay dos tipos de humectación: humectación no reactiva y humectación reactiva. [2] [3]
La humectación es importante en la unión o adherencia de dos materiales. [4] La humectación y las fuerzas superficiales que controlan la humectación también son responsables de otros efectos relacionados, incluidos los efectos capilares . Se pueden utilizar tensioactivos para aumentar el poder humectante de un líquido como el agua.
La humectación es un foco de atención en los estudios de nanotecnología y nanociencia debido a la aparición de muchos nanomateriales en las últimas dos décadas (por ejemplo, grafeno , [5] nanotubos de carbono , nanomallas de nitruro de boro [6] ).
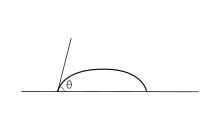
Las fuerzas adhesivas entre un líquido y un sólido hacen que una gota de líquido se extienda por la superficie. Las fuerzas cohesivas dentro del líquido hacen que la gota se forme una bola y evite el contacto con la superficie.

El ángulo de contacto (θ), como se ve en la Figura 1, es el ángulo en el que la interfaz líquido-vapor se encuentra con la interfaz sólido-líquido. El ángulo de contacto está determinado por el equilibrio entre las fuerzas adhesivas y cohesivas. A medida que aumenta la tendencia de una gota a extenderse sobre una superficie plana y sólida, el ángulo de contacto disminuye. Por tanto, el ángulo de contacto proporciona una medida inversa de la humectabilidad. [7]
Un ángulo de contacto inferior a 90° (ángulo de contacto bajo) generalmente indica que la humectación de la superficie es muy favorable y el fluido se esparcirá sobre una gran área de la superficie. Los ángulos de contacto superiores a 90° (ángulo de contacto alto) generalmente significan que la humectación de la superficie es desfavorable, por lo que el fluido minimizará el contacto con la superficie y formará una gota de líquido compacta.
Para el agua, una superficie humectable también puede denominarse hidrófila y una superficie no humectable, hidrófoba . Las superficies superhidrófobas tienen ángulos de contacto superiores a 150°, lo que casi no muestra contacto entre la gota de líquido y la superficie. A esto a veces se le llama " efecto loto ". La tabla describe los diferentes ángulos de contacto y sus correspondientes interacciones sólido/líquido y líquido/líquido. [8] Para líquidos no acuosos, el término liofílico se usa para condiciones de ángulo de contacto bajo y liófobo se usa cuando se obtienen ángulos de contacto más altos. De manera similar, los términos omnifóbico y omnifílico se aplican tanto a líquidos polares como apolares.
Los líquidos pueden interactuar con dos tipos principales de superficies sólidas. Tradicionalmente, las superficies sólidas se han dividido en sólidos de alta y baja energía . La energía relativa de un sólido tiene que ver con la naturaleza masiva del propio sólido. Los sólidos como metales, vidrios y cerámicas se conocen como "sólidos duros" porque los enlaces químicos que los mantienen unidos (p. ej., covalentes , iónicos o metálicos ) son muy fuertes. Por lo tanto, se necesita una gran cantidad de energía para romper estos sólidos (alternativamente, se requiere una gran cantidad de energía para cortar la masa y formar dos superficies separadas), por lo que se denominan "de alta energía". La mayoría de los líquidos moleculares logran una humectación completa con superficies de alta energía.
El otro tipo de sólido son los cristales moleculares débiles (p. ej., fluorocarbonos , hidrocarburos , etc.) donde las moléculas se mantienen unidas esencialmente mediante fuerzas físicas (p. ej., fuerzas de van der Waals y enlaces de hidrógeno ). Dado que estos sólidos se mantienen unidos por fuerzas débiles, se requiere una cantidad muy pequeña de energía para romperlos, por lo que se denominan "de baja energía". Dependiendo del tipo de líquido elegido, las superficies de baja energía pueden permitir una humectación total o parcial. [9] [10]
Se ha informado que las superficies dinámicas sufren cambios en la energía superficial tras la aplicación de un estímulo apropiado. Por ejemplo, se demostró que una superficie que presenta motores moleculares impulsados por fotones sufre cambios en el ángulo de contacto con el agua cuando se cambia entre conformaciones biestables de diferentes energías superficiales. [11]
Las superficies de baja energía interactúan principalmente con líquidos a través de fuerzas dispersivas ( van der Waals ). William Zisman produjo varios hallazgos clave: [12]
Zisman observó que cos θ aumenta linealmente a medida que disminuye la tensión superficial (γ LV ) del líquido. Así, pudo establecer una función lineal entre cos θ y la tensión superficial (γ LV ) para varios líquidos orgánicos .
Una superficie es más humectable cuando γ LV y θ son bajos. Zisman denominó la intersección de estas líneas cuando cos θ = 1 como la tensión superficial crítica (γ c ) de esa superficie. Esta tensión superficial crítica es un parámetro importante porque es una característica únicamente del sólido.
Conociendo la tensión superficial crítica de un sólido, es posible predecir la humectabilidad de la superficie. [7] La humectabilidad de una superficie está determinada por los grupos químicos más externos del sólido. Las diferencias en la humectabilidad entre superficies que son similares en estructura se deben a diferencias en el empaquetamiento de los átomos. Por ejemplo, si una superficie tiene cadenas ramificadas, tendrá un empaquetamiento peor que una superficie con cadenas rectas. Una tensión superficial crítica más baja significa una superficie del material menos humectable.
Una superficie ideal es plana, rígida, perfectamente lisa, químicamente homogénea y tiene histéresis de ángulo de contacto cero . La histéresis cero implica que los ángulos de contacto de avance y retroceso son iguales. En otras palabras, sólo existe un ángulo de contacto termodinámicamente estable. Cuando se coloca una gota de líquido sobre dicha superficie, se forma el ángulo de contacto característico como se muestra en la Figura 1. Además, en una superficie ideal, la gota volverá a su forma original si se la molesta. [8] [12] Las siguientes derivaciones se aplican sólo a superficies sólidas ideales; sólo son válidos para el estado en el que las interfaces no se mueven y la línea límite de fase existe en equilibrio.

La Figura 3 muestra la línea de contacto donde se encuentran tres fases. En equilibrio , la fuerza neta por unidad de longitud que actúa a lo largo de la línea límite entre las tres fases debe ser cero. Las componentes de la fuerza neta en la dirección a lo largo de cada una de las interfaces vienen dadas por:
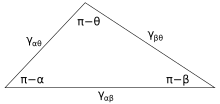
donde α, β y θ son los ángulos mostrados y γ ij es la energía superficial entre las dos fases indicadas. Estas relaciones también se pueden expresar mediante un análogo de un triángulo conocido como triángulo de Neumann, que se muestra en la Figura 4. El triángulo de Neumann es consistente con la restricción geométrica de que , y al aplicarle la ley de los senos y la ley de los cosenos se producen relaciones que describen cómo Los ángulos interfaciales dependen de las proporciones de energías superficiales. [13]
Debido a que estas tres energías superficiales forman los lados de un triángulo , están limitadas por las desigualdades del triángulo, γ ij < γ jk + γ ik , lo que significa que ninguna de las tensiones superficiales puede exceder la suma de las otras dos. Si se ponen en contacto tres fluidos con energías superficiales que no siguen estas desigualdades, no existirá ninguna configuración de equilibrio consistente con la Figura 3.

Si la fase β se reemplaza por una superficie plana y rígida, como se muestra en la Figura 5, entonces β = π, y la segunda ecuación de fuerza neta se simplifica a la ecuación de Young, [14]
que relaciona las tensiones superficiales entre las tres fases: sólida , líquida y gaseosa . Posteriormente, esto predice el ángulo de contacto de una gota de líquido sobre una superficie sólida a partir del conocimiento de las tres energías superficiales involucradas. Esta ecuación también se aplica si la fase "gas" es otra líquida, inmiscible con la gota de la primera fase "líquida".
Considere la interfaz como una curva donde hay un parámetro libre. La energía libre a minimizar es
con las restricciones que podemos escribir como volumen fijo .
El lagrangiano modificado, teniendo en cuenta las restricciones, es por lo tanto
¿ Dónde están los multiplicadores de Lagrange? Por definición, el impulso y el hamiltoniano se calcula como:
Ahora recordemos que la frontera es libre en la dirección y es un parámetro libre. Por tanto, debemos tener:
En la frontera y , por tanto recuperamos la ecuación de Young.
La ecuación de Young supone una superficie perfectamente plana y rígida a menudo denominada superficie ideal . En muchos casos, las superficies están lejos de esta situación ideal, y aquí se consideran dos: el caso de superficies rugosas y el caso de superficies lisas que aún son reales (finitamente rígidas). Incluso en una superficie perfectamente lisa, una gota adoptará un amplio espectro de ángulos de contacto que van desde el llamado ángulo de contacto de avance, hasta el llamado ángulo de contacto de retroceso, . El ángulo de contacto de equilibrio ( ) se puede calcular a partir de y como lo mostró Tadmor [16] como,
dónde
La ecuación de Young-Dupré ( Thomas Young 1805; Anthanase Dupré y Paul Dupré 1869) dicta que ni γ SG ni γ SL pueden ser mayores que la suma de las otras dos energías superficiales. [17] [18] La consecuencia de esta restricción es la predicción de humectación completa cuando γ SG > γ SL + γ LG y humectación cero cuando γ SL > γ SG + γ LG . La falta de una solución a la ecuación de Young-Dupré es un indicador de que no existe una configuración de equilibrio con un ángulo de contacto entre 0 y 180° para esas situaciones. [19]
Un parámetro útil para medir la humectación es el parámetro de dispersión S ,
Cuando S > 0, el líquido moja completamente la superficie (mojado completo). Cuando S < 0, se produce una humectación parcial.
Combinando la definición del parámetro de dispersión con la relación de Young se obtiene la ecuación de Young-Dupré:
que solo tiene soluciones físicas para θ cuando S < 0.
Con mejoras en técnicas de medición como AFM, microscopía confocal y SEM, los investigadores pudieron producir y obtener imágenes de gotas a escalas cada vez más pequeñas. Con la reducción del tamaño de las gotas surgieron nuevas observaciones experimentales sobre la humectación. Estas observaciones confirman que la ecuación de Young modificada [20] no se cumple en las escalas micronano. Además el signo de la tensión de la línea no se mantiene mediante la ecuación de Young modificada. [21]
Para una gota sésil, la energía libre del sistema trifásico se puede expresar como: [22] [23]
A volumen constante en equilibrio termodinámico, esto se reduce a: [24]
Por lo general, el término VdP se ha descuidado para gotas grandes; sin embargo, el trabajo de VdP se vuelve significativo a escalas pequeñas. La variación de presión a volumen constante en el límite libre líquido-vapor se debe a la presión de Laplace , que es proporcional a la curvatura media de la gota y no es cero. Al resolver la ecuación anterior para superficies convexas y cóncavas se obtiene: [25]
Donde los parámetros constantes A, B y C se definen como:

Esta ecuación relaciona el ángulo de contacto , una propiedad geométrica de una gota sésil con la termodinámica global, la energía en el límite de contacto de tres fases y la curvatura de la superficie α. Para el caso especial de una gota sésil sobre una superficie plana (α=0),
Los dos primeros términos son la ecuación de Young modificada, [20] mientras que el tercer término se debe a la presión de Laplace. Esta ecuación no lineal predice correctamente el signo y la magnitud de κ, el aplanamiento del ángulo de contacto a escalas muy pequeñas y la histéresis del ángulo de contacto. [25] [21]
Para muchas configuraciones de superficie/adsorbato, los datos de energía superficial y las observaciones experimentales no están disponibles. Como las interacciones de humectación son de gran importancia en diversas aplicaciones, a menudo se desea predecir y comparar el comportamiento de humectación de varias superficies de materiales con orientaciones cristalográficas particulares, en relación con el agua u otros adsorbatos. Esto se puede hacer desde una perspectiva atomística con herramientas que incluyen la dinámica molecular y la teoría funcional de la densidad . [26] [27] En la predicción teórica de la humectación mediante enfoques ab initio como la DFT, el agua suele sustituirse por hielo. Esto se debe a que los cálculos de DFT generalmente se realizan asumiendo condiciones de movimiento térmico cero de los átomos, lo que esencialmente significa que la simulación se realiza en el cero absoluto . Sin embargo, esta simplificación produce resultados que son relevantes para la adsorción de agua en condiciones realistas y el uso de hielo para la simulación teórica de la humectación es común. [28]
.jpg/440px-Cahysteresis(crop).jpg)
A diferencia de las superficies ideales, las superficies reales no tienen perfecta suavidad, rigidez u homogeneidad química. Tales desviaciones de la idealidad dan como resultado un fenómeno llamado histéresis del ángulo de contacto , que se define como la diferencia entre los ángulos de contacto de avance (θ a ) y de retroceso (θ r ) [29]
Cuando el ángulo de contacto está entre los casos de avance y retroceso, se considera que la línea de contacto está fijada y se puede observar un comportamiento histerético, es decir, histéresis del ángulo de contacto . Cuando se superan estos valores, el desplazamiento de la línea de contacto, como el de la Figura 3, se producirá ya sea por expansión o retracción de la gota. [30] La Figura 6 muestra los ángulos de contacto de avance y retroceso. El ángulo de contacto de avance es el ángulo estable máximo, mientras que el ángulo de contacto de retroceso es el ángulo estable mínimo. La histéresis del ángulo de contacto ocurre porque en un sólido no ideal se encuentran muchos ángulos de contacto termodinámicamente estables diferentes. Estos ángulos de contacto termodinámicamente estables variables se conocen como estados metaestables. [12]
Este movimiento de un límite de fase, que implica ángulos de contacto de avance y retroceso, se conoce como humectación dinámica. La diferencia entre los ángulos de mojado dinámicos y estáticos es proporcional al número de capilares . Cuando una línea de contacto avanza, cubriendo más superficie con líquido, el ángulo de contacto aumenta y generalmente está relacionado con la velocidad de la línea de contacto. [30] [31] Si la velocidad de una línea de contacto aumenta sin límite, el ángulo de contacto aumenta y, a medida que se acerca a 180 °, la fase gaseosa quedará arrastrada en una capa delgada entre el líquido y el sólido. Este es un efecto cinético de desequilibrio que resulta de que la línea de contacto se mueve a una velocidad tan alta que no puede ocurrir una humectación completa.
Una desviación bien conocida de las condiciones ideales es cuando la superficie de interés tiene una textura rugosa. La textura rugosa de una superficie puede clasificarse en una de dos categorías: homogénea o heterogénea. Un régimen de humectación homogéneo es aquel en el que el líquido llena los surcos de una superficie rugosa. Sin embargo, un régimen de humectación heterogéneo es aquel en el que la superficie está compuesta de dos tipos de parches. Un ejemplo importante de una superficie compuesta de este tipo es aquella compuesta de parches tanto de aire como de sólido. Estas superficies tienen efectos variados sobre los ángulos de contacto de los líquidos humectantes. Cassie-Baxter y Wenzel son los dos modelos principales que intentan describir la humectación de superficies texturizadas. Sin embargo, estas ecuaciones sólo se aplican cuando el tamaño de la gota es suficientemente grande en comparación con la escala de rugosidad de la superficie. [32] Cuando el tamaño de la gota es comparable al de los pilares subyacentes, se debe considerar el efecto de la tensión de la línea. [33]

El modelo de Wenzel (Robert N. Wenzel, 1936) describe el régimen de humectación homogéneo, como se ve en la Figura 7, y se define mediante la siguiente ecuación para el ángulo de contacto sobre una superficie rugosa: [32]
donde es el ángulo de contacto aparente que corresponde al estado de equilibrio estable (es decir, el estado mínimo de energía libre para el sistema). La relación de rugosidad, r, es una medida de cómo la rugosidad de la superficie afecta a una superficie homogénea. La relación de rugosidad se define como la relación entre el área real de la superficie sólida y el área aparente.
θ es el ángulo de contacto de Young definido para una superficie ideal. Aunque la ecuación de Wenzel demuestra que el ángulo de contacto de una superficie rugosa es diferente del ángulo de contacto intrínseco , no describe la histéresis del ángulo de contacto . [34]

Cuando se trata de una superficie heterogénea, el modelo de Wenzel no es suficiente. Se necesita un modelo más complejo para medir cómo cambia el ángulo de contacto aparente cuando intervienen varios materiales. Esta superficie heterogénea, como la que se ve en la Figura 8, se explica mediante la ecuación de Cassie-Baxter ( ley de Cassie ): [32]
Aquí, r f es la relación de rugosidad del área de la superficie húmeda y f es la fracción del área de la superficie sólida mojada por el líquido. Es importante darse cuenta de que cuando f = 1 y r f = r , las ecuaciones de Cassie-Baxter se convierten en la ecuación de Wenzel. Por otro lado, cuando hay muchas fracciones diferentes de rugosidad superficial, cada fracción del área superficial total se denota por .
La suma de todos es igual a 1 o la superficie total. Cassie-Baxter también se puede reformular en la siguiente ecuación: [35]
Aquí está la tensión superficial de Cassie-Baxter entre líquido y vapor, es la tensión superficial del vapor sólido de cada componente y es la tensión superficial del líquido sólido de cada componente. Un caso que vale la pena mencionar es cuando la gota de líquido se coloca sobre el sustrato y crea pequeñas bolsas de aire debajo de él. Este caso para un sistema de dos componentes se denota por: [35]
Aquí la diferencia clave a notar es que no hay tensión superficial entre el sólido y el vapor para el segundo componente de tensión superficial. Esto se debe a la suposición de que la superficie del aire expuesta está debajo de la gota y es el único otro sustrato en el sistema. Posteriormente, la ecuación se expresa como (1 – f ). Por lo tanto, la ecuación de Cassie se puede derivar fácilmente de la ecuación de Cassie-Baxter. Los resultados experimentales sobre las propiedades de la superficie de los sistemas Wenzel versus Cassie-Baxter mostraron el efecto de la fijación para un ángulo de Young de 180 a 90 °, una región clasificada bajo el modelo Cassie-Baxter. Este sistema compuesto líquido/aire es en gran medida hidrófobo. Después de ese punto, se encontró una transición brusca al régimen de Wenzel donde la gota moja la superficie, pero no más allá de los bordes de la gota. En realidad, las ecuaciones de Young, Wenzel y Cassie-Baxter representan las condiciones de transversalidad del problema variacional de la humectación. [36] [37]
Con la llegada de las imágenes de alta resolución, los investigadores han comenzado a obtener datos experimentales que les han llevado a cuestionar los supuestos de la ecuación de Cassie-Baxter al calcular el ángulo de contacto aparente. Estos grupos [ ¿quién? ] creen que el ángulo de contacto aparente depende en gran medida de la línea triple. La línea triple, que está en contacto con la superficie heterogénea, no puede descansar sobre la superficie heterogénea como el resto de la gota. En teoría, debería seguir la imperfección de la superficie. Esta curvatura de la línea triple es desfavorable y no se ve en situaciones del mundo real. Una teoría que preserva la ecuación de Cassie-Baxter y al mismo tiempo explica la presencia del estado energético minimizado de la línea triple depende de la idea de una película precursora. Esta película de espesor submicrométrico avanza por delante del movimiento de la gota y se encuentra alrededor de la línea triple. Además, esta película precursora permite que la triple línea se doble y tome diferentes conformaciones que originalmente se consideraban desfavorables. Este fluido precursor se ha observado mediante microscopía electrónica de barrido ambiental (ESEM) en superficies con poros formados en masa. Con la introducción del concepto de película precursora, la línea triple puede seguir conformaciones energéticamente viables, explicando así correctamente el modelo de Cassie-Baxter. [38]

La hidrofobicidad intrínseca de una superficie se puede mejorar al texturizarla con diferentes escalas de rugosidad . La rosa roja aprovecha esto utilizando una jerarquía de micro y nanoestructuras en cada pétalo para proporcionar suficiente rugosidad para la superhidrofobicidad. Más concretamente, cada pétalo de rosa tiene una colección de micropapilas en la superficie y cada papila, a su vez, tiene muchos nanopliegues. El término " efecto pétalo " describe el hecho de que una gota de agua sobre la superficie de un pétalo de rosa tiene forma esférica, pero no puede caer incluso si el pétalo está boca abajo. Las gotas de agua mantienen su forma esférica debido a la superhidrofobicidad del pétalo (ángulo de contacto de aproximadamente 152,4°), pero no se deslizan porque la superficie del pétalo tiene una alta fuerza adhesiva con el agua. [39]
Al comparar el " efecto pétalo " con el " efecto loto ", es importante observar algunas diferencias sorprendentes. La estructura superficial de la hoja de loto y del pétalo de rosa, como se ve en la Figura 9, puede usarse para explicar los dos efectos diferentes.
La hoja de loto tiene una superficie aleatoriamente rugosa y una histéresis de ángulo de contacto bajo , lo que significa que la gota de agua no puede mojar los espacios de la microestructura entre las púas. Esto permite que el aire permanezca dentro de la textura, provocando una superficie heterogénea compuesta tanto de aire como de sólido. Como resultado, la fuerza adhesiva entre el agua y la superficie sólida es extremadamente baja, permitiendo que el agua se escurra fácilmente (es decir, fenómeno de " autolimpieza ").
Las micro y nanoestructuras del pétalo de rosa son de mayor escala que las de la hoja de loto, lo que permite que la película líquida impregne la textura. Sin embargo, como se ve en la Figura 9, el líquido puede entrar en las ranuras de mayor escala, pero no puede entrar en las ranuras más pequeñas. Esto se conoce como régimen humectante de impregnación Cassie. Dado que el líquido puede mojar las ranuras de mayor tamaño, la fuerza adhesiva entre el agua y el sólido es muy alta. Esto explica por qué la gota de agua no se caerá incluso si el pétalo está inclinado en ángulo o al revés. Este efecto fallará si la gota tiene un volumen superior a 10 µl porque se supera el equilibrio entre peso y tensión superficial. [40]

En el modelo de Cassie-Baxter , la gota se asienta sobre la superficie texturizada con aire atrapado debajo. Durante la transición de humectación del estado de Cassie al estado de Wenzel, las bolsas de aire ya no son termodinámicamente estables y el líquido comienza a nuclearse desde el centro de la gota, creando un "estado de hongo", como se ve en la Figura 10. [41] La penetración condición viene dada por:
dónde

El frente de penetración se propaga para minimizar la energía superficial hasta llegar a los bordes de la gota, llegando así al estado de Wenzel. Dado que el sólido puede considerarse un material absorbente debido a la rugosidad de su superficie, este fenómeno de dispersión e imbibición se denomina hemiwicking. Los ángulos de contacto en los que se produce la dispersión/imbibición están entre 0 y π/2. [42]
El modelo de Wenzel es válido entre θ C y π/2. Si el ángulo de contacto es menor que Θ C , el frente de penetración se extiende más allá de la gota y se forma una película líquida sobre la superficie. La Figura 11 representa la transición del estado de Wenzel al estado de película superficial. La película suaviza las rugosidades de la superficie y ya no se aplica el modelo de Wenzel. En este estado, la condición de equilibrio y la relación de Young producen:
Al ajustar la rugosidad de la superficie, es posible lograr una transición entre regiones superhidrófobas y superhidrófilas. Generalmente, cuanto más rugosa es la superficie, más hidrofóbica es.
Si se coloca una gota sobre una superficie horizontal lisa, generalmente no se encuentra en estado de equilibrio. Por lo tanto, se propaga hasta alcanzar un radio de contacto de equilibrio (mojado parcial). Si bien se tienen en cuenta las contribuciones capilares, gravitacionales y viscosas, el radio de caída en función del tiempo se puede expresar como [43]
Para la situación de humectación completa, el radio de caída en cualquier momento durante el proceso de dispersión viene dado por
dónde
Muchos procesos tecnológicos requieren el control de la dispersión del líquido sobre superficies sólidas. Cuando se coloca una gota sobre una superficie, puede mojar completamente, mojar parcialmente o no mojar la superficie. Al reducir la tensión superficial con tensioactivos , se puede hacer que un material no humectante se humedezca parcial o completamente. El exceso de energía libre (σ) de una gota sobre una superficie sólida es: [44]
Según esta ecuación, el exceso de energía libre se minimiza cuando γ disminuye, γ SL disminuye o γ SV aumenta. Los surfactantes se absorben en las interfaces líquido-vapor, sólido-líquido y sólido-vapor, lo que modifica el comportamiento de humectación de los materiales hidrofóbicos para reducir la energía libre. Cuando los tensioactivos se absorben en una superficie hidrofóbica, los grupos de cabezas polares miran hacia la solución con la cola apuntando hacia afuera. En superficies más hidrófobas, los tensioactivos pueden formar una bicapa sobre el sólido, lo que hace que se vuelva más hidrófilo. El radio de caída dinámico se puede caracterizar cuando la caída comienza a extenderse. Por lo tanto, el ángulo de contacto cambia según la siguiente ecuación: [44]
A medida que se absorben los tensioactivos, la tensión superficial sólido-vapor aumenta y los bordes de la gota se vuelven hidrófilos. Como resultado, la caída se extiende.

El ferroceno es un compuesto organometálico activo redox [46] que puede incorporarse a varios monómeros y utilizarse para fabricar polímeros que pueden fijarse a una superficie. [45] El vinilferroceno (ferroceneyleteno) se puede preparar mediante una reacción de Wittig [47] y luego polimerizarse para formar polivinilferroceno (PVFc), un análogo del poliestireno . Otro polímero que se puede formar es poli( ferrocenocarboxilato de 2-(metacriloiloxi)etilo ), PFcMA. Tanto el PVFc como el PFcMA se han unido a obleas de sílice y se ha medido la humectabilidad cuando las cadenas de polímero no están cargadas y cuando los restos de ferroceno se oxidan para producir grupos cargados positivamente, como se ilustra a la derecha. [45] El ángulo de contacto con el agua en las obleas recubiertas de PFcMA fue 70° menor después de la oxidación, mientras que en el caso de PVFc la disminución fue de 30°, y se ha demostrado que el cambio de humectabilidad es reversible. En el caso de PFcMA, se investigó el efecto de cadenas más largas con más grupos ferroceno (y también mayor masa molar ), y se encontró que las cadenas más largas producen reducciones de ángulo de contacto significativamente mayores. [45] [48]
Los óxidos de tierras raras exhiben hidrofobicidad intrínseca y, por lo tanto, pueden usarse en intercambiadores de calor térmicamente estables y otras aplicaciones que involucran hidrofobicidad a alta temperatura. [49] La presencia de vacantes de oxígeno en las superficies de ceria u otros óxidos de tierras raras es fundamental para regular la humectabilidad de la superficie. La adsorción de agua en superficies de óxido puede ocurrir como adsorción molecular, en la que las moléculas de H2O permanecen intactas en la superficie terminada, o como adsorción disociativa, en la que OH y H se adsorben por separado [50] en superficies sólidas. Generalmente se encuentra que la presencia de vacantes de oxígeno mejora la hidrofobicidad al tiempo que promueve la adsorción disociativa. [51]