La regla de Kasha es un principio de la fotoquímica de moléculas excitadas electrónicamente . La regla establece que la emisión de fotones ( fluorescencia o fosforescencia ) se produce con un rendimiento apreciable solo a partir del estado excitado más bajo de una multiplicidad dada . Recibe su nombre del espectroscopista estadounidense Michael Kasha , quien la propuso en 1950. [1] [2]
La regla es relevante para entender el espectro de emisión de una molécula excitada. Al absorber un fotón, una molécula en su estado electrónico fundamental (denotado S 0 , suponiendo un estado singlete ) puede –dependiendo de la longitud de onda del fotón– ser excitada a cualquiera de un conjunto de estados electrónicos superiores (denotado S n donde n >0). Sin embargo, según la regla de Kasha, se espera la emisión de fotones (denominada fluorescencia en el caso de un estado S ) con un rendimiento apreciable solo desde el estado excitado más bajo, S 1 . Dado que solo se espera que un estado produzca emisión, una declaración equivalente de la regla es que la longitud de onda de emisión es independiente de la longitud de onda de excitación. [3]
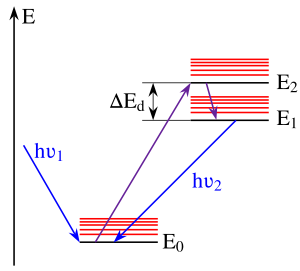
La regla puede explicarse mediante los factores de Franck-Condon para las transiciones vibrónicas . Para un par dado de niveles de energía que difieren tanto en números cuánticos vibracionales como electrónicos , el factor de Franck-Condon expresa el grado de superposición entre sus funciones de onda vibracionales . Cuanto mayor sea la superposición, más rápidamente puede la molécula experimentar una transición del nivel superior al inferior. La superposición entre pares es mayor cuando los dos niveles vibracionales están cerca en energía; este tiende a ser el caso cuando los niveles sin vibración de los estados electrónicos acoplados por la transición (donde el número cuántico vibracional v es cero) están cerca. En la mayoría de las moléculas, los niveles sin vibración de los estados excitados se encuentran todos juntos, por lo que las moléculas en los estados superiores alcanzan rápidamente el estado excitado más bajo, S 1 , antes de que tengan tiempo de fluorescer. Sin embargo, la brecha de energía entre S 1 y S 0 es mayor, por lo que aquí se produce la fluorescencia, ya que ahora es cinéticamente competitiva con la conversión interna (CI). [4] [5]
Las excepciones a la regla de Kasha surgen cuando hay grandes brechas de energía entre los estados excitados. Un ejemplo es el azuleno : la explicación clásica es que los estados S 1 y S 2 se encuentran lo suficientemente separados como para que la fluorescencia se observe principalmente desde S 2 . [4] [5] En 2023, se propuso una explicación que señalaba que el estado excitado S 1 tiene un carácter antiaromático mientras que el estado excitado S 2 es aromático . [6]
Un corolario de la regla de Kasha es la regla de Vavilov , que establece que el rendimiento cuántico de la luminiscencia es generalmente independiente de la longitud de onda de excitación. [4] [7] Esto puede entenderse como una consecuencia de la tendencia –implícita en la regla de Kasha– de las moléculas en estados superiores a relajarse al estado excitado más bajo de manera no radiactiva. Nuevamente hay excepciones: por ejemplo, el vapor de benceno . [4]