Clase de receptores acoplados a proteína G implicados en la quimiotaxis
Los receptores de formilpéptidos ( FPR ) pertenecen a una clase de receptores acoplados a proteína G implicados en la quimiotaxis . [1] [2] En los seres humanos, existen tres isoformas del receptor del péptido formilo, cada una codificada por un gen independiente que se denomina FPR1 , FPR2 y FPR3 . [1] Estos receptores se identificaron originalmente por su capacidad para unirse a N-formil péptidos como la N -formilmetionina producida por la degradación de células bacterianas o huésped. [3] [4] Por lo tanto, los receptores de péptidos formilo participan en la mediación de la respuesta de las células inmunitarias a la infección. Estos receptores también pueden actuar para suprimir el sistema inmunológico bajo ciertas condiciones. [5] La estrecha relación filogenética entre la señalización en la quimiotaxis y el olfato se demostró recientemente mediante la detección de proteínas similares al receptor de péptido formilo como una familia distinta de quimiosensores de órganos vomeronasales en ratones. [6] [7]
Actualmente, la FPR está debidamente aceptada como FPR1 por la Unión Internacional de Farmacología Básica y Clínica. [2]
Descubrimiento
Estudios realizados en la década de 1970 encontraron que una serie de oligopéptidos que contienen N-formilmetionina , incluido el miembro más potente y mejor conocido de esta serie, la N-formilmetionina-leucil-fenilalanina (fMLF o fMet-Leu-Phe), estimulaban la estimulación en conejos y humanos. "Los neutrófilos mediante un aparente mecanismo dependiente del receptor migran en un patrón direccional en ensayos de quimiotaxis de laboratorio clásicos ". Dado que estos oligopéptidos fueron producidos por bacterias o análogos sintéticos de dichos productos, se sugirió que los N-formiloligopéptidos son factores quimiotácticos importantes y sus receptores son importantes receptores de factores quimiotácticos que actúan respectivamente como elementos de señalización y reconocimiento de señales para iniciar respuestas de inflamación en para defenderse de la invasión bacteriana. Otros estudios definieron un receptor para los oligopéptidos N-formilo, el receptor de péptido formil (FPR), llamado así debido a su capacidad para unirse y activarse por los oligopéptidos. Posteriormente se descubrieron dos receptores y se denominaron FPR1 y FPR2 basándose en la similitud de la secuencia de aminoácidos predicha de sus genes con la de FPR en lugar de en cualquier capacidad para unirse o ser activados por los oligopéptidos formil. Estos tres receptores han sido rebautizados como FPR1, FPR2 y FPR3 y se ha descubierto que tienen especificidades muy diferentes para los oligopéptidos formil y funciones muy diferentes que incluyen el inicio de respuestas inflamatorias a los péptidos N-formilo liberados no solo por bacterias sino también por una multiplicidad de elementos liberados. por los tejidos del huésped; amortiguar y resolver las respuestas inflamatorias; y quizás contribuyendo al desarrollo de ciertos cánceres neurológicos y una variedad de enfermedades neurológicas basadas en amiloide . [2]
Estructura y función
El receptor de formilpéptido (FPR) pertenece a la clase de receptores que poseen siete dominios transmembrana hidrófobos. La conformación del FPR se estabiliza mediante varias interacciones. Estos incluyen la posible formación de puentes salinos entre Arg84-Arg205, Lys85-Arg205 y Lys85-Asp284 que ayudan a determinar la estructura tridimensional de los dominios transmembrana, así como residuos cargados positivamente (Arg, Lys) que interactúan con fosfatos cargados negativamente. Además, el residuo Arg163 puede interactuar con el bolsillo de unión al ligando del segundo bucle extracelular del FPR.
Con respecto a la unión del péptido formilo Met-Leu-Phe, existen interacciones potenciales adicionales que incluyen interacciones de enlace de hidrógeno entre Arg84 y Lys85 del primer bucle extracelular y el grupo N-formilo del ligando, así como la columna vertebral peptídica del formilo. Met-Leu-Phe que puede formar interacciones similares. Se demostró que el resto formil-Met del ligando forma puentes disulfuro con residuos de Cys y también se demostró una interacción con Arg163. (Es importante mencionar que algunas interacciones que estabilizan la conformación del receptor también pueden influir en la unión del ligando). También se describieron algunos oligopéptidos como constituyentes característicos unidos a Asn-s de la parte N terminal extracelular y al bolsillo de unión al ligando de el segundo bucle extracelular. Estos componentes también pueden determinar o hacer más específica la interacción ligando-receptor. [7] [8]
Vías de señalización
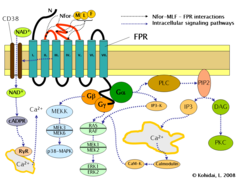
La inducción de FPR desencadena múltiples cambios en las células eucariotas , incluido el reordenamiento del citoesqueleto , que a su vez facilita la migración celular y la síntesis de quimiocinas . Las vías importantes reguladas por FPR incluyen:
- Activación dependiente de la proteína G de la fosfolipasa C (PLC), que da como resultado la descomposición del fosfolípido constituyente de la membrana, fosfatidilinositol (4,5)-bisfosfato (PIP2) en inositol (1,4,5)-trifosfato (IP3) y diacilglicerol ( TROZO DE CUERO). IP3 es uno de los inductores más eficaces del aumento de Ca 2+ desde los depósitos citoplasmáticos y desde el exterior de la célula a través de la apertura de canales de Ca 2+ . DAG a su vez es un inductor de la proteína quinasa C (PKC).
- Activación de la pequeña GTPasa reguladora, RAS . El RAS activo puede a su vez activar RAF , una quinasa Ser/Thr. En el siguiente paso se activan las proteínas quinasas activadas por mitógenos (MAP quinasas). (También conocidas como quinasas reguladas por señales extracelulares: ERK o MAP/ERK quinasa (MEK)). Como resultado del último paso, se activan ERK1 y ERK2 . Las formas fosforiladas de ERK pueden continuar la cascada desencadenando la activación de más quinasas que interactúan, lo que da como resultado una actividad transcripcional alterada en el núcleo.
- La unión del ligando a FPR también puede inducir la activación de CD38 , una ectoenzima de la membrana superficial. Como resultado de la activación, las moléculas de NAD + ingresarán al citoplasma. El NAD + se convierte en ADP ribosa cíclico (cADPR), un segundo mensajero que interactúa con los receptores de rianodina (RyR) en la superficie del retículo endoplásmico rugoso . El resultado general del proceso es un aumento de los niveles de Ca 2+ citoplasmático a través de la vía directa descrita anteriormente y también a través de vías indirectas como la apertura de canales de Ca 2+ en la membrana celular. El aumento sostenido de Ca 2+ es necesario para la migración dirigida de las células. [9]
Ver también
Referencias
- ^ ab Migeotte I, Communi D, Parmentier M (diciembre de 2006). "Receptores de péptidos formilo: una subfamilia promiscua de receptores acoplados a proteína G que controlan las respuestas inmunes". Reseñas de citocinas y factores de crecimiento . 17 (6): 501–19. doi :10.1016/j.cytogfr.2006.09.009. PMID 17084101.
- ^ abc Ye RD, Boulay F, Wang JM, Dahlgren C, Gerard C, Parmentier M, Serhan CN, Murphy PM (junio de 2009). "Unión Internacional de Farmacología Básica y Clínica. LXXIII. Nomenclatura de la familia del receptor de péptido formilo (FPR)". Revisiones farmacológicas . 61 (2): 119–61. doi :10.1124/pr.109.001578. PMC 2745437 . PMID 19498085.
- ^ Le Y, Murphy PM, Wang JM (noviembre de 2002). "Revisión de los receptores de formilopéptido". Tendencias en Inmunología . 23 (11): 541–8. doi :10.1016/S1471-4906(02)02316-5. PMID 12401407.
- ^ Panaro MA, Acquafredda A, Sisto M, Lisi S, Maffione AB, Mitolo V (2006). "Papel biológico de los receptores del péptido N-formilo". Inmunofarmacología e Inmunotoxicología . 28 (1): 103–27. doi :10.1080/08923970600625975. hdl :11586/115781. PMID 16684671. S2CID 23082578.
- ^ Braun MC, Wang JM, Lahey E, Rabin RL, Kelsall BL (junio de 2001). "La activación del receptor del péptido formilo por el péptido T-20 derivado del VIH suprime la producción de interleucina-12 p70 por parte de los monocitos humanos". Sangre . 97 (11): 3531–6. doi :10.1182/sangre.V97.11.3531. PMID 11369647.
- ^ Rivière S, Challet L, Fluegge D, Spehr M, Rodríguez I (mayo de 2009). "Las proteínas similares al receptor del péptido formilo son una nueva familia de quimiosensores vomeronasales". Naturaleza . 459 (7246): 574–7. Código Bib :2009Natur.459..574R. doi : 10.1038/naturaleza08029. PMID 19387439. S2CID 4302009.
- ^ ab Yuan S, Ghoshdastider U, Trzaskowski B, Latek D, Debinski A, Pulawski W, Wu R, Gerke V, Filipek S (2012). "El papel del agua en el mecanismo de activación del receptor 1 del péptido N-formilo humano (FPR1) basado en simulaciones de dinámica molecular". MÁS UNO . 7 (11): e47114. Código Bib : 2012PLoSO...747114Y. doi : 10.1371/journal.pone.0047114 . PMC 3506623 . PMID 23189124.
- ^ Lala A, Gwinn M, De Nardin E (septiembre de 1999). "Función del receptor de péptido formilo humano de los residuos cargados conservados y no conservados". Revista europea de bioquímica . 264 (2): 495–9. doi : 10.1046/j.1432-1327.1999.00647.x . PMID 10491096.
- ^ Partida-Sánchez S, Cockayne DA, Monard S, Jacobson EL, Oppenheimer N, Garvy B, Kusser K, Goodrich S, Howard M, Harmsen A, Randall TD, Lund FE (noviembre de 2001). "La producción cíclica de ADP-ribosa por CD38 regula la liberación de calcio intracelular, el influjo de calcio extracelular y la quimiotaxis en los neutrófilos y es necesaria para la eliminación de bacterias in vivo". Medicina de la Naturaleza . 7 (11): 1209–16. doi :10.1038/nm1101-1209. PMID 11689885. S2CID 13239085.
enlaces externos
- "Receptores de formilpéptido". Base de datos IUPHAR de receptores y canales iónicos . Unión Internacional de Farmacología Básica y Clínica. Archivado desde el original el 19 de junio de 2015 . Consultado el 2 de noviembre de 2007 .
- Receptor de formilo + péptido + en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.