La reacción de Atherton-Todd es una reacción con nombre en química orgánica que se remonta a los químicos británicos FR Atherton, HT Openshaw y AR Todd. Estos describieron la reacción por primera vez en 1945 como un método para convertir fosfitos de dialquilo en clorofosfatos de dialquilo. [1] Sin embargo, los clorofosfatos de dialquilo formados suelen ser demasiado reactivos para ser aislados. Por esta razón, la síntesis de fosfatos o fosforamidatos puede seguir la reacción de Atherton-Todd en presencia de alcoholes o aminas . La siguiente ecuación ofrece una descripción general de la reacción de Atherton-Todd utilizando el reactivo fosfito de dimetilo como ejemplo:
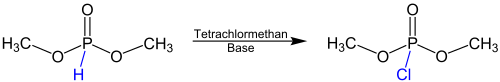
La reacción se produce tras la adición de tetraclorometano y una base . Esta base suele ser una amina primaria, secundaria o terciaria . En lugar de grupos metilo pueden estar presentes otros grupos alquilo o bencilo .
Aquí se presenta un posible mecanismo de reacción para la reacción de Atherton-Todd para el ejemplo de dimetilfosfito, al igual que en la reacción general: [2]

En primer lugar, se utiliza una amina terciaria para escindir un grupo metilo del fosfito de dimetilo. De este paso de reacción se obtiene el intermedio 1 .

Posteriormente, el intermedio 1 desprotona el compuesto de partida dimetilfosfito, de modo que se forman los intermedios 2a y 2b . A continuación, el intermedio 1 se regenera a partir del intermedio 2a .

Finalmente, el intermedio 2b se clora con tetraclorometano y se forma clorofosfato de dimetilo 3 .
Después de la síntesis del clorofosfato de dimetilo, es posible una reacción adicional (por ejemplo con una amina primaria como la anilina ) mediante la siguiente ecuación de reacción: [3]

En esta reacción, además del compuesto de partida fosfito de dialquilo, se utilizan tetraclorometano y una base (una amina) en cantidades estequiométricas . Solo el cloroformo, que se forma tras dos pasos de reacción a partir del tetraclorometano, es relevante como producto de desecho para la evaluación de la economía atómica. Además, debe tenerse en cuenta que el producto de la reacción tiene una masa molar mayor que el compuesto de partida. Por lo tanto, la economía atómica de esta reacción puede clasificarse como relativamente buena.
La reacción de Atherton-Todd está relacionada con la reacción de Appel . En la reacción de Appel, también se utiliza tetraclorometano para la cloración . [2]
{{citation}}: CS1 maint: varios nombres: lista de autores ( enlace ){{citation}}: CS1 maint: varios nombres: lista de autores ( enlace )