
Las sinapsis químicas son uniones biológicas a través de las cuales las señales de las neuronas pueden enviarse entre sí y a células no neuronales, como las de los músculos o las glándulas . Las sinapsis químicas permiten que las neuronas formen circuitos dentro del sistema nervioso central . Son cruciales para los cálculos biológicos que sustentan la percepción y el pensamiento . Permiten que el sistema nervioso se conecte con otros sistemas del cuerpo y los controle.
En una sinapsis química, una neurona libera moléculas de neurotransmisores en un pequeño espacio (la hendidura sináptica) adyacente a otra neurona. Los neurotransmisores están contenidos en pequeños sacos llamados vesículas sinápticas y se liberan en la hendidura sináptica por exocitosis . Estas moléculas luego se unen a los receptores de neurotransmisores en la célula postsináptica. Finalmente, los neurotransmisores se eliminan de la sinapsis a través de uno de varios mecanismos posibles, incluida la degradación enzimática o la recaptación por transportadores específicos, ya sea en la célula presináptica o en alguna otra neuroglia para terminar la acción del neurotransmisor.
Se estima que el cerebro humano adulto contiene entre 10 14 y 5 × 10 14 (100–500 billones) de sinapsis. [1] Cada milímetro cúbico de corteza cerebral contiene aproximadamente mil millones ( escala corta , es decir, 10 9 ) de ellas. [2] El número de sinapsis en la corteza cerebral humana se ha estimado por separado en 0,15 cuatrillones (150 billones) [3]
La palabra "sinapsis" fue introducida por Sir Charles Scott Sherrington en 1897. [4] Las sinapsis químicas no son el único tipo de sinapsis biológicas : también existen sinapsis eléctricas e inmunológicas . Sin embargo, sin un calificativo, "sinapsis" se refiere comúnmente a las sinapsis químicas.

Las sinapsis son conexiones funcionales entre neuronas, o entre neuronas y otros tipos de células. [5] [6] Una neurona típica da lugar a varios miles de sinapsis, aunque hay algunos tipos que producen muchas menos. [7] La mayoría de las sinapsis conectan axones con dendritas , [8] [9] pero también hay otros tipos de conexiones, incluidas las de axón a cuerpo celular, [10] [11] axón a axón, [10] [11] y dendrita a dendrita . [9] Las sinapsis son generalmente demasiado pequeñas para ser reconocibles usando un microscopio óptico excepto como puntos donde las membranas de dos células parecen tocarse, pero sus elementos celulares se pueden visualizar claramente usando un microscopio electrónico .
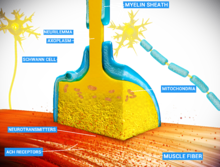
Las sinapsis químicas transmiten información de manera direccional desde una célula presináptica a una célula postsináptica y, por lo tanto, son asimétricas en estructura y función. La terminal axónica presináptica o sinápticaEl botón es un área especializada dentro del axón de la célula presináptica que contiene neurotransmisores encerrados en pequeñas esferas unidas a una membrana llamadas vesículas sinápticas (así como una serie de otras estructuras y orgánulos de soporte, como las mitocondrias y el retículo endoplasmático ). Las vesículas sinápticas están acopladas a la membrana plasmática presináptica en regiones llamadas zonas activas .
Justo enfrente hay una región de la célula postsináptica que contiene receptores de neurotransmisores ; para las sinapsis entre dos neuronas, la región postsináptica puede encontrarse en las dendritas o el cuerpo celular. Inmediatamente detrás de la membrana postsináptica hay un complejo elaborado de proteínas interconectadas llamado densidad postsináptica (PSD).
Las proteínas de la PSD participan en el anclaje y el tráfico de receptores de neurotransmisores y en la modulación de la actividad de estos receptores. Los receptores y las PSD se encuentran a menudo en protuberancias especializadas del eje dendrítico principal llamadas espinas dendríticas .
Las sinapsis pueden describirse como simétricas o asimétricas. Cuando se examinan con un microscopio electrónico, las sinapsis asimétricas se caracterizan por vesículas redondeadas en la célula presináptica y una densidad postsináptica prominente. Las sinapsis asimétricas son típicamente excitatorias. Las sinapsis simétricas, en cambio, tienen vesículas aplanadas o alargadas y no contienen una densidad postsináptica prominente. Las sinapsis simétricas son típicamente inhibidoras.
La hendidura sináptica , también llamada brecha sináptica , es un espacio entre las células presinápticas y postsinápticas que tiene aproximadamente 20 nm (0,02 μ) de ancho. [12] El pequeño volumen de la hendidura permite que la concentración de neurotransmisores aumente y disminuya rápidamente. [13]
Una autapsis es una sinapsis química (o eléctrica) que se forma cuando el axón de una neurona hace sinapsis con sus propias dendritas.
A continuación se presenta un resumen de la secuencia de eventos que tienen lugar en la transmisión sináptica desde una neurona presináptica a una célula postsináptica. Cada paso se explica con más detalle a continuación. Tenga en cuenta que, con excepción del paso final, el proceso completo puede durar solo unos pocos cientos de microsegundos, en las sinapsis más rápidas. [14]
La liberación de un neurotransmisor se desencadena por la llegada de un impulso nervioso (o potencial de acción ) y ocurre a través de un proceso inusualmente rápido de secreción celular ( exocitosis ). Dentro de la terminal nerviosa presináptica, las vesículas que contienen neurotransmisores se localizan cerca de la membrana sináptica. El potencial de acción que llega produce una afluencia de iones de calcio a través de canales iónicos dependientes del voltaje y selectivos del calcio en el recorrido descendente del potencial de acción (corriente de cola). [15] Los iones de calcio luego se unen a las proteínas sinaptotagminas que se encuentran dentro de las membranas de las vesículas sinápticas, lo que permite que las vesículas se fusionen con la membrana presináptica. [16] La fusión de una vesícula es un proceso estocástico , que conduce a un fallo frecuente de la transmisión sináptica en las sinapsis muy pequeñas que son típicas del sistema nervioso central . Las sinapsis químicas grandes (por ejemplo, la unión neuromuscular ), por otro lado, tienen una probabilidad de liberación sináptica, en efecto, de 1. La fusión de vesículas es impulsada por la acción de un conjunto de proteínas en la terminal presináptica conocidas como SNARE . En su conjunto, el complejo proteico o estructura que media el acoplamiento y la fusión de vesículas presinápticas se denomina zona activa. [17] La membrana añadida por el proceso de fusión se recupera posteriormente por endocitosis y se recicla para la formación de vesículas nuevas llenas de neurotransmisores.
Una excepción a la tendencia general de liberación de neurotransmisores por fusión vesicular se encuentra en las células receptoras de tipo II de las papilas gustativas de los mamíferos . En ellas, el neurotransmisor ATP se libera directamente desde el citoplasma hacia la hendidura sináptica a través de canales dependientes del voltaje. [18]
Receptors on the opposite side of the synaptic gap bind neurotransmitter molecules. Receptors can respond in either of two general ways. First, the receptors may directly open ligand-gated ion channels in the postsynaptic cell membrane, causing ions to enter or exit the cell and changing the local transmembrane potential.[14] The resulting change in voltage is called a postsynaptic potential. In general, the result is excitatory in the case of depolarizing currents, and inhibitory in the case of hyperpolarizing currents. Whether a synapse is excitatory or inhibitory depends on what type(s) of ion channel conduct the postsynaptic current(s), which in turn is a function of the type of receptors and neurotransmitter employed at the synapse. The second way a receptor can affect membrane potential is by modulating the production of chemical messengers inside the postsynaptic neuron. These second messengers can then amplify the inhibitory or excitatory response to neurotransmitters.[14]
After a neurotransmitter molecule binds to a receptor molecule, it must be removed to allow for the postsynaptic membrane to continue to relay subsequent EPSPs and/or IPSPs. This removal can happen through one or more processes:
The strength of a synapse has been defined by Bernard Katz as the product of (presynaptic) release probability pr, quantal size q (the postsynaptic response to the release of a single neurotransmitter vesicle, a 'quantum'), and n, the number of release sites. "Unitary connection" usually refers to an unknown number of individual synapses connecting a presynaptic neuron to a postsynaptic neuron. The amplitude of postsynaptic potentials (PSPs) can be as low as 0.4 mV to as high as 20 mV.[20] The amplitude of a PSP can be modulated by neuromodulators or can change as a result of previous activity. Changes in the synaptic strength can be short-term, lasting seconds to minutes, or long-term (long-term potentiation, or LTP), lasting hours. Learning and memory are believed to result from long-term changes in synaptic strength, via a mechanism known as synaptic plasticity.
Desensitization of the postsynaptic receptors is a decrease in response to the same neurotransmitter stimulus. It means that the strength of a synapse may in effect diminish as a train of action potentials arrive in rapid succession – a phenomenon that gives rise to the so-called frequency dependence of synapses. The nervous system exploits this property for computational purposes, and can tune its synapses through such means as phosphorylation of the proteins involved.
Synaptic transmission can be changed by previous activity. These changes are called synaptic plasticity and may result in either a decrease in the efficacy of the synapse, called depression, or an increase in efficacy, called potentiation. These changes can either be long-term or short-term. Forms of short-term plasticity include synaptic fatigue or depression and synaptic augmentation. Forms of long-term plasticity include long-term depression and long-term potentiation. Synaptic plasticity can be either homosynaptic (occurring at a single synapse) or heterosynaptic (occurring at multiple synapses).
La plasticidad homosináptica (o también modulación homotrópica) es un cambio en la fuerza sináptica que resulta de la historia de actividad en una sinapsis particular. Esto puede ser resultado de cambios en el calcio presináptico, así como de la retroalimentación sobre los receptores presinápticos, es decir, una forma de señalización autocrina . La plasticidad homosináptica puede afectar el número y la tasa de reposición de vesículas o puede afectar la relación entre el calcio y la liberación de vesículas. La plasticidad homosináptica también puede ser de naturaleza postsináptica. Puede resultar en un aumento o disminución de la fuerza sináptica.
Un ejemplo son las neuronas del sistema nervioso simpático (SNS), que liberan noradrenalina , que, además de afectar a los receptores postsinápticos, también afecta a los receptores α2-adrenérgicos presinápticos , inhibiendo la liberación adicional de noradrenalina. [21] Este efecto se utiliza con clonidina para realizar efectos inhibidores en el SNS.
La plasticidad heterosináptica (o también modulación heterotrópica) es un cambio en la fuerza sináptica que resulta de la actividad de otras neuronas. Nuevamente, la plasticidad puede alterar el número de vesículas o su tasa de reposición o la relación entre el calcio y la liberación de vesículas. Además, podría afectar directamente la entrada de calcio. La plasticidad heterosináptica también puede ser de naturaleza postsináptica, afectando la sensibilidad del receptor.
Un ejemplo son nuevamente las neuronas del sistema nervioso simpático , que liberan noradrenalina , la cual, además, genera un efecto inhibidor sobre las terminales presinápticas de las neuronas del sistema nervioso parasimpático . [21]
En general, si una sinapsis excitatoria es lo suficientemente fuerte, un potencial de acción en la neurona presináptica desencadenará un potencial de acción en la célula postsináptica. En muchos casos, el potencial postsináptico excitatorio (PSPE) no alcanzará el umbral para generar un potencial de acción. Cuando los potenciales de acción de múltiples neuronas presinápticas se activan simultáneamente, o si una sola neurona presináptica se activa a una frecuencia lo suficientemente alta, los PSPE pueden superponerse y sumarse. Si se superponen suficientes PSPE, el PSPE sumado puede alcanzar el umbral para iniciar un potencial de acción. Este proceso se conoce como suma y puede servir como un filtro de paso alto para las neuronas. [22]
Por otra parte, una neurona presináptica que libera un neurotransmisor inhibidor, como el GABA , puede provocar un potencial postsináptico inhibidor (IPSP) en la neurona postsináptica, alejando el potencial de membrana del umbral, disminuyendo su excitabilidad y haciendo más difícil que la neurona inicie un potencial de acción. Si un IPSP se superpone con un EPSP, el IPSP puede en muchos casos impedir que la neurona dispare un potencial de acción. De esta manera, la salida de una neurona puede depender de la entrada de muchas neuronas diferentes, cada una de las cuales puede tener un grado diferente de influencia, dependiendo de la fuerza y el tipo de sinapsis con esa neurona. John Carew Eccles realizó algunos de los primeros experimentos importantes sobre la integración sináptica, por los que recibió el Premio Nobel de Fisiología o Medicina en 1963.
Cuando se libera un neurotransmisor en una sinapsis, alcanza su concentración más alta dentro del estrecho espacio de la hendidura sináptica, pero es seguro que una parte se difunde antes de ser reabsorbida o degradada. Si se difunde, tiene el potencial de activar receptores que se encuentran en otras sinapsis o en la membrana alejada de cualquier sinapsis. La actividad extrasináptica de un neurotransmisor se conoce como transmisión de volumen . [23] Está bien establecido que tales efectos ocurren en algún grado, pero su importancia funcional ha sido durante mucho tiempo un tema de controversia. [24]
Trabajos recientes indican que la transmisión de volumen puede ser el modo predominante de interacción para algunos tipos especiales de neuronas. En la corteza cerebral de los mamíferos, una clase de neuronas llamadas células neurogliaformes pueden inhibir a otras neuronas corticales cercanas al liberar el neurotransmisor GABA en el espacio extracelular. [25] En la misma línea, el GABA liberado desde las células neurogliaformes al espacio extracelular también actúa sobre los astrocitos circundantes , asignando un papel para la transmisión de volumen en el control de la homeostasis iónica y de neurotransmisores. [26] Aproximadamente el 78% de los botones de las células neurogliaformes no forman sinapsis clásicas. Este puede ser el primer ejemplo definitivo de neuronas que se comunican químicamente donde no hay sinapsis clásicas. [25]
An electrical synapse is an electrically conductive link between two abutting neurons that is formed at a narrow gap between the pre- and postsynaptic cells, known as a gap junction. At gap junctions, cells approach within about 3.5 nm of each other, rather than the 20 to 40 nm distance that separates cells at chemical synapses.[27][28] As opposed to chemical synapses, the postsynaptic potential in electrical synapses is not caused by the opening of ion channels by chemical transmitters, but rather by direct electrical coupling between both neurons. Electrical synapses are faster than chemical synapses.[13] Electrical synapses are found throughout the nervous system, including in the retina, the reticular nucleus of the thalamus, the neocortex, and in the hippocampus.[29] While chemical synapses are found between both excitatory and inhibitory neurons, electrical synapses are most commonly found between smaller local inhibitory neurons. Electrical synapses can exist between two axons, two dendrites, or between an axon and a dendrite.[30][31] In some fish and amphibians, electrical synapses can be found within the same terminal of a chemical synapse, as in Mauthner cells.[32]
One of the most important features of chemical synapses is that they are the site of action for the majority of psychoactive drugs. Synapses are affected by drugs, such as curare, strychnine, cocaine, morphine, alcohol, LSD, and countless others. These drugs have different effects on synaptic function, and often are restricted to synapses that use a specific neurotransmitter. For example, curare is a poison that stops acetylcholine from depolarizing the postsynaptic membrane, causing paralysis. Strychnine blocks the inhibitory effects of the neurotransmitter glycine, which causes the body to pick up and react to weaker and previously ignored stimuli, resulting in uncontrollable muscle spasms. Morphine acts on synapses that use endorphin neurotransmitters, and alcohol increases the inhibitory effects of the neurotransmitter GABA. LSD interferes with synapses that use the neurotransmitter serotonin. Cocaine blocks reuptake of dopamine and therefore increases its effects.
During the 1950s, Bernard Katz and Paul Fatt observed spontaneous miniature synaptic currents at the frog neuromuscular junction.[33] Based on these observations, they developed the 'quantal hypothesis' that is the basis for our current understanding of neurotransmitter release as exocytosis and for which Katz received the Nobel Prize in Physiology or Medicine in 1970.[34] In the late 1960s, Ricardo Miledi and Katz advanced the hypothesis that depolarization-induced influx of calcium ions triggers exocytosis.
Sir Charles Scott Sherringtonin coined the word 'synapse' and the history of the word was given by Sherrington in a letter he wrote to John Fulton:
'I felt the need of some name to call the junction between nerve-cell and nerve-cell... I suggested using "syndesm"... He [ Sir Michael Foster ] consulted his Trinity friend Verrall, the Euripidean scholar, about it, and Verrall suggested "synapse" (from the Greek "clasp").'–Charles Scott Sherrington[4]
sinapsis conectan los axones al cuerpo celular.