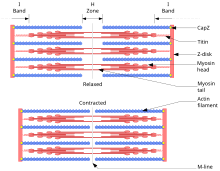
La teoría del filamento deslizante explica el mecanismo de contracción muscular basado en proteínas musculares que se deslizan unas sobre otras para generar movimiento. [1] Según la teoría del filamento deslizante, la miosina ( filamentos gruesos ) de las fibras musculares se desliza más allá de la actina ( filamentos delgados ) durante la contracción muscular, mientras que los dos grupos de filamentos permanecen en una longitud relativamente constante.
La teoría fue introducida de forma independiente en 1954 por dos equipos de investigación, uno formado por Andrew Huxley y Rolf Niedergerke de la Universidad de Cambridge , y el otro formado por Hugh Huxley y Jean Hanson del Instituto Tecnológico de Massachusetts . [2] [3] Fue concebida originalmente por Hugh Huxley en 1953. Andrew Huxley y Niedergerke la presentaron como una hipótesis "muy atractiva". [4]
Antes de la década de 1950, existían varias teorías contrapuestas sobre la contracción muscular, incluida la atracción eléctrica, el plegamiento de proteínas y la modificación de proteínas. [5] La nueva teoría introdujo directamente un nuevo concepto llamado teoría de puentes cruzados (puente cruzado oscilante clásico, ahora conocido principalmente como ciclo de puentes cruzados ) que explica el mecanismo molecular del filamento deslizante. La teoría de los puentes cruzados establece que la actina y la miosina forman un complejo proteico (clásicamente llamado actomiosina ) mediante la unión de la cabeza de miosina al filamento de actina, formando así una especie de puente cruzado entre los dos filamentos. La teoría del filamento deslizante es una explicación ampliamente aceptada del mecanismo que subyace a la contracción muscular. [6]
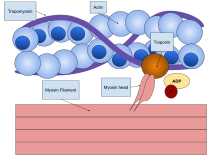

La primera proteína muscular descubierta fue la miosina por el científico alemán Willy Kühne , quien la extrajo y le puso nombre en 1864. [7] En 1939, un equipo formado por marido y mujer rusos, Vladimir Alexandrovich Engelhardt y Militsa Nikolaevna Lyubimova, descubrieron que la miosina tenía una enzima (llamada ATPasa ). propiedad que puede descomponer el ATP para liberar energía. [8] Albert Szent-Györgyi , un fisiólogo húngaro, centró su atención en la fisiología muscular después de ganar el Premio Nobel de Fisiología o Medicina en 1937 por sus trabajos sobre la vitamina C y el ácido fumárico . En 1942 demostró que el ATP era la fuente de energía para la contracción muscular. De hecho, observó que las fibras musculares que contenían miosina B se acortaban en presencia de ATP, pero no con miosina A, experiencia que más tarde describió como "quizás el momento más emocionante de mi vida". [9] Con Brunó Ferenc Straub , pronto descubrió que la miosina B estaba asociada a otra proteína, a la que llamaron actina, mientras que la miosina A no. Straub purificó la actina en 1942 y Szent-Györgyi purificó la miosina A en 1943. Se hizo evidente que la miosina B era una combinación de miosina A y actina, de modo que la miosina A conservó el nombre original, mientras que cambiaron el nombre de miosina B a actomiosina. A finales de la década de 1940, el equipo de Szent-Györgyi había postulado con evidencia que la contracción de actomiosina era equivalente a la contracción muscular en su conjunto. [10] Pero la idea fue generalmente rechazada, incluso por parte de personas como premios Nobel como Otto Fritz Meyerhof y Archibald Hill , quienes adhirieron al dogma predominante de que la miosina era una proteína estructural y no una enzima funcional. [3] Sin embargo, en una de sus últimas contribuciones a la investigación muscular, Szent-Györgyi demostró que la actomiosina impulsada por ATP era el principio básico de la contracción muscular. [11]

Cuando Hugh Huxley obtuvo su doctorado en la Universidad de Cambridge en 1952 sobre su investigación sobre la estructura del músculo, Szent-Györgyi había centrado su carrera en la investigación del cáncer. [12] Huxley fue al laboratorio de Francis O. Schmitt en el Instituto Tecnológico de Massachusetts con una beca postdoctoral en septiembre de 1952, donde se le unió otro becario postdoctoral inglés, Jean Hanson, en enero de 1953. Hanson tenía un doctorado. en estructura muscular del King's College de Londres en 1951. Huxley había utilizado la difracción de rayos X para especular que las proteínas musculares, en particular la miosina, forman filamentos estructurados que dan lugar al sarcómero (un segmento de fibra muscular). Su principal objetivo era utilizar la microscopía electrónica para estudiar los detalles de esos filamentos como nunca antes se había hecho. Pronto descubrieron y confirmaron la naturaleza filamentosa de las proteínas musculares. La miosina y la actina forman filamentos superpuestos; los filamentos de miosina constituyen principalmente la banda A (la región oscura de un sarcómero), mientras que los filamentos de actina atraviesan las bandas A e I (región clara). [13] Huxley fue el primero en sugerir la teoría del filamento deslizante en 1953, afirmando:
"... [S]i se postula que el estiramiento del músculo tiene lugar, no mediante una extensión de los filamentos, sino mediante un proceso en el que los dos conjuntos de filamentos se deslizan [énfasis añadido] uno sobre el otro; entonces se inhibirá la extensibilidad si la miosina y la actina están unidas". [14]
Posteriormente, en 1996, Huxley lamentó haber incluido a Hanson en la formulación de su teoría porque se basaba en su trabajo colaborativo. [15]
Andrew Huxley , a quien Alan Hodgkin describió como "un mago con aparatos científicos", acababa de descubrir el mecanismo de transmisión del impulso nervioso ( potencial de acción ) (por el que él y Hodgkin ganaron más tarde el Premio Nobel de Fisiología o Medicina en 1963) en 1949 utilizando su propio diseño de pinza de voltaje y estaba buscando un asociado que pudiera diseccionar adecuadamente las fibras musculares. [16] Por recomendación de un amigo cercano, Robert Stämpfli, el médico alemán Rolf Niedergerke se unió a él en la Universidad de Cambridge en 1952. Para entonces se dio cuenta de que el microscopio de contraste de fases utilizado convencionalmente no era adecuado para estructuras finas de fibras musculares, y Así desarrolló su propio microscopio de interferencia . Entre marzo de 1953 y enero de 1954 ejecutaron su investigación. [17] Huxley recordó que en ese momento la única persona que pensó en filamentos deslizantes antes de 1953 fue Dorothy Hodgkin (más tarde ganadora del Premio Nobel de Química en 1964 ). [18] Pasó el verano de 1953 en el Laboratorio de Biología Marina en Woods Hole, Massachusetts, para utilizar el microscopio electrónico allí. Allí conoció a Hugh Huxley y Hanson con quienes compartió datos e información sobre sus obras. Se separaron con el acuerdo de que se mantendrían en contacto y, cuando lograran su objetivo, publicarían juntos, si alguna vez "llegaban a conclusiones similares". [2]

La teoría del filamento deslizante nació de dos artículos consecutivos publicados en la edición del 22 de mayo de 1954 de Nature bajo el tema común "Cambios estructurales en el músculo durante la contracción". Aunque sus conclusiones fueron fundamentalmente similares, sus proposiciones y datos experimentales subyacentes eran diferentes.
El primer artículo, escrito por Andrew Huxley y Rolf Niedergerke, se titula "Microscopía de interferencia de fibras musculares vivas". Se basó en su estudio del músculo de la rana utilizando un microscopio de interferencia, que Andrew Huxley desarrolló para tal fin. Según ellos: [4]
El segundo artículo, de Hugh Huxley y Jean Hanson, se titula "Cambios en las estrías cruzadas del músculo durante la contracción y el estiramiento y su interpretación estructural". Es más elaborado y se basó en su estudio del músculo de conejo utilizando microscopios electrónicos y de contraste de fases. Según ellos: [19]
A pesar de las pruebas contundentes, la teoría del filamento deslizante no obtuvo ningún apoyo durante varios años. [20] El propio Szent-Györgyi se negó a creer que los filamentos de miosina estuvieran confinados al filamento grueso (banda A). [15] FO Schmitt, cuyo microscopio electrónico proporcionó los mejores datos, también se mostró escéptico ante las imágenes originales. [21] También hubo discusiones inmediatas sobre la organización de los filamentos, si los dos conjuntos (miosina y actina) de filamentos eran simplemente superpuestos o continuos. Sólo con el nuevo microscopio electrónico Hugh Huxley confirmó la naturaleza superpuesta de los filamentos en 1957. [22] También fue a partir de esta publicación que se demostró claramente la existencia del enlace actina-miosina (ahora llamado puente cruzado). Pero tardó otros cinco años en aportar pruebas de que el puente cruzado era una interacción dinámica entre los filamentos de actina y miosina. [23] Obtuvo la disposición molecular real de los filamentos utilizando cristalografía de rayos X al asociarse con Kenneth Holmes , quien fue entrenado por Rosalind Franklin , en 1965. [24] Fue solo después de una conferencia en 1972 en el Laboratorio Cold Spring Harbor. , donde se deliberaron sobre la teoría y su evidencia, que llegó a ser generalmente aceptada. [25] En la conferencia, como recordaría más tarde Koscak Maruyama, Hanson tuvo que responder a las críticas gritando: "Sé que no puedo explicar el mecanismo todavía, pero el deslizamiento es un hecho". [26] Las pruebas objetivas llegaron a principios de la década de 1980, cuando diferentes investigadores pudieron demostrar el movimiento de deslizamiento real utilizando herramientas novedosas y sofisticadas. [27] [28] [29]
Con pruebas sustanciales, Hugh Huxley propuso formalmente el mecanismo para el deslizamiento del filamento, que se denomina modelo de puente cruzado oscilante, teoría de puente cruzado o modelo de puente cruzado. [3] [30] (Él mismo prefería el nombre "modelo de puente cruzado oscilante", porque, como recordó, "al fin y al cabo [el descubrimiento] era la década de 1960". [2] ) Publicó su teoría en el siglo XX. Número de junio de 1969 de Science con el título "El mecanismo de contracción muscular". [31] Según su teoría, el deslizamiento de los filamentos se produce por unión y desprendimiento cíclico de miosina en los filamentos de actina. La contracción ocurre cuando la miosina tira del filamento de actina hacia el centro de la banda A, se desprende de la actina y crea una fuerza (golpe) para unirse a la siguiente molécula de actina. [32] Esta idea se demostró posteriormente en detalle y se conoce más apropiadamente como ciclo de puentes cruzados . [33]