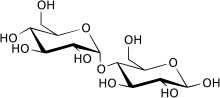


Maltasa es el nombre informal de una familia de enzimas que catalizan la hidrólisis del disacárido maltosa en dos azúcares simples de glucosa . Las maltasas se encuentran en plantas, bacterias, levaduras, seres humanos y otros vertebrados.
La digestión del almidón requiere seis enzimas intestinales. Dos de estas enzimas son endoglucosidasas luminales llamadas alfa-amilasas. Las otras cuatro enzimas han sido identificadas como diferentes maltasas, exoglucosidasas unidas a la superficie luminal de los enterocitos. Dos de estas actividades de maltasa se asociaron con la sacarasa-isomaltasa (maltasa Ib, maltasa Ia). Las otras dos maltasas sin características distintivas se denominaron maltasa-glucoamilasa (maltasas II y III). Las actividades de estas cuatro maltasas también se describen como alfa-glucosidasas porque todas digieren oligosacáridos lineales de almidón a glucosa. [1] [2]
Las maltasas son miembros de un grupo de enzimas intestinales llamadas Familia GH13 ( familia 13 de las glicósidos hidrolasas ) que son responsables de descomponer los enlaces α-glucosidasa de los carbohidratos complejos en moléculas de glucosa fáciles de usar. [3] Las moléculas de glucosa se utilizarían entonces como una especie de "alimento" para que las células produzcan energía ( trifosfato de adenosina ) durante la respiración celular . Los siguientes son genes que pueden codificar la maltasa:

El mecanismo de todas las enzimas de la familia GH13 es romper un enlace de la α-glucosidasa mediante su hidrolización. La maltasa se centra en romper la maltosa, un disacárido que es un enlace entre dos unidades de glucosa, en el enlace α-(1->4). La velocidad de hidrólisis está controlada por el tamaño del sustrato (tamaño del carbohidrato). [6]
La alfa-amilasa tiene una función importante en la degradación de los almidones, por lo que se utiliza con frecuencia en la industria de la panificación. Se utiliza principalmente como medio para realzar el sabor y mejorar la calidad del pan. [4] Sin la alfa-amilasa, la levadura no podría fermentar. [7]
La maltosa-glucoamilasa se utiliza comúnmente como fuente de fermentación, ya que es capaz de cortar el almidón en maltosa, que luego se utiliza para elaborar cerveza y sake. [4]
Además de la elaboración de cerveza, se ha estudiado la maltosa glucoamilasa introduciendo inhibidores específicos para detener la hidrólisis de los enlaces de la α-glucosidasa. Al inhibir la ruptura de los enlaces, los científicos esperan idear un fármaco que sea más eficaz y menos tóxico para el tratamiento de la diabetes. [8]
La historia del descubrimiento de la maltasa comenzó cuando Napoleón Bonaparte declaró un bloqueo continental en su “decreto de Berlín” en 1806. Esto inició la búsqueda de fuentes alternativas de azúcar. En 1833, los químicos franceses Anselm Payen y Jean-Francois Persoz descubrieron un extracto de malta que convertía el almidón en glucosa, a la que llamaron diastasa en ese momento. [9] En 1880, HT Brown descubrió la actividad de la maltasa en las mucosas y la diferenció de la diastasa, ahora llamada amilasa. [2] En la década de 1960, los avances en la química de las proteínas permitieron a Arne Dahlqvist y Giorgio Semenza fraccionar y caracterizar las actividades de la maltasa en el intestino delgado. Ambos grupos demostraron que había cuatro fracciones principales de la actividad de la maltasa que eran intrínsecas a dos estructuras peptídicas diferentes, la sacarasa-isomaltasa y la maltasa-glucoamilasa. [1] [2] [9] [6] Cincuenta años después, entrando en la era genómica, la clonación y secuenciación de la hidrolasa de almidón de la mucosa confirmaron los hallazgos de Dahlqvist y Semenza. [9]
La deficiencia de maltasa ácida (DMRE), también conocida como enfermedad de Pompe, fue descrita por primera vez por el patólogo holandés JC Pompe en 1932. [10] [11] La DMRE es una enfermedad autosómica recesiva no ligada al sexo en la que se produce una acumulación excesiva de glucógeno en las vacuolas de los lisosomas en casi todos los tipos de células del cuerpo. [10] [11] [12] Es una de las enfermedades de almacenamiento de glucógeno más graves que afectan al tejido muscular. [13]
La DMAE se clasifica en tres tipos diferentes según la edad de aparición de los síntomas en el individuo afectado: infantil (tipo a), niñez (tipo b) y adultez (tipo c). El tipo de DMAE está determinado por el tipo de mutación genética localizada en 17q23. El tipo de mutación determinará el nivel de producción de maltasa ácida. La DMAE es extremadamente mortal. El tipo a generalmente muere de insuficiencia cardíaca antes del año de edad. El tipo b muere de insuficiencia respiratoria entre los tres y los veinticuatro años de edad. El tipo c muere de insuficiencia respiratoria entre 10 y 20 años de la aparición de los síntomas. [13]
Los murciélagos vampiros son los únicos vertebrados conocidos que no muestran actividad de maltasa intestinal. [14]