

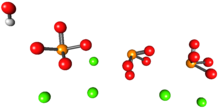
La hidroxiapatita ( nombre IMA : hidroxiapatita [5] ) (Hap, HAp o HA) es una forma mineral natural de apatita cálcica con la fórmula Ca 5 (PO 4 ) 3 (OH) , a menudo escrita Ca 10 (PO 4 ) 6. (OH) 2 para indicar que la celda unitaria de cristal comprende dos entidades. [6] Es el miembro final hidroxilo del complejo grupo apatita . El ion OH- puede ser reemplazado por fluoruro o cloruro , produciendo fluorapatita o clorapatita . Cristaliza en el sistema cristalino hexagonal . El polvo puro de hidroxiapatita es blanco. Sin embargo, las apatitas naturales también pueden presentar coloraciones marrones, amarillas o verdes, comparables a las decoloraciones de la fluorosis dental .
Hasta el 50% en volumen y el 70% en peso del hueso humano es una forma modificada de hidroxiapatita, conocida como mineral óseo . [7] La hidroxiapatita carbonatada deficiente en calcio es el principal mineral que compone el esmalte dental y la dentina . Los cristales de hidroxiapatita también se encuentran en calcificaciones patológicas como las que se encuentran en los tumores de mama , [8] así como en calcificaciones dentro de la glándula pineal (y otras estructuras del cerebro) conocidas como cuerpos arenacea o "arena cerebral". [9]
La hidroxiapatita se puede sintetizar mediante varios métodos, como la deposición química húmeda, la deposición biomimética, la ruta sol-gel (precipitación química húmeda) o la electrodeposición. [10] La suspensión de nanocristales de hidroxiapatita se puede preparar mediante una reacción de precipitación química húmeda siguiendo la siguiente ecuación de reacción: [11]
10 Ca(OH) 2 + 6 H 3 PO 4 → Ca 10 (PO 4 ) 6 (OH) 2 + 18 H 2 O
La capacidad de replicar sintéticamente la hidroxiapatita tiene implicaciones clínicas invaluables, especialmente en odontología. Cada técnica produce cristales de hidroxiapatita de características variadas, como tamaño y forma. [12] Estas variaciones tienen un marcado efecto sobre las propiedades biológicas y mecánicas del compuesto y, por lo tanto, estos productos de hidroxiapatita tienen diferentes usos clínicos. [13]
Hidroxiapatita deficiente en calcio (no estequiométrica), Ca 10− x (PO 4 ) 6− x (HPO 4 ) x (OH) 2− x (donde x está entre 0 y 1) tiene una relación Ca/P entre 1,67 y 1.5. La relación Ca/P se utiliza a menudo en la discusión de las fases de fosfato cálcico. [14] La apatita estequiométrica Ca 10 (PO 4 ) 6 (OH) 2 tiene una relación Ca/P de 10:6, normalmente expresada como 1,67. Las fases no estequiométricas tienen la estructura de hidroxiapatita con vacantes de cationes ( Ca 2+ ) y aniones ( OH − ). Los sitios ocupados únicamente por aniones fosfato en la hidroxiapatita estequiométrica, están ocupados por fosfato o hidrogenofosfato, HPO2-4, aniones. [14] La preparación de estas fases deficientes en calcio se puede preparar mediante precipitación a partir de una mezcla de nitrato de calcio y fosfato diamónico con la relación Ca/P deseada, por ejemplo, para hacer una muestra con una relación Ca/P de 1,6: [15 ]
La sinterización de estas fases no estequiométricas forma una fase sólida que es una mezcla íntima de fosfato tricálcico e hidroxiapatita, denominada fosfato cálcico bifásico : [16]
La hidroxiapatita está presente en huesos y dientes ; el hueso está formado principalmente por cristales de HA intercalados en una matriz de colágeno ; entre el 65 y el 70% de la masa ósea es HA. De manera similar, el HA constituye del 70 al 80% de la masa de dentina y esmalte de los dientes. En el esmalte, la matriz del HA está formada por amelogeninas y esmalteinas en lugar de colágeno. [17]
Los depósitos de hidroxiapatita en los tendones alrededor de las articulaciones provocan la afección médica tendinitis calcificada . [18]
La hidroxiapatita es un componente de los cálculos renales de fosfato de calcio . [19]
La remineralización del esmalte dental implica la reintroducción de iones minerales en el esmalte desmineralizado. [20] La hidroxiapatita es el principal componente mineral del esmalte de los dientes. [21] Durante la desmineralización, los iones de calcio y fósforo se extraen de la hidroxiapatita. Los iones minerales introducidos durante la remineralización restauran la estructura de los cristales de hidroxiapatita. [21] Si hay iones de fluoruro presentes durante la remineralización, a través de la fluoración del agua o el uso de pasta de dientes que contiene fluoruro, se forman cristales de fluorapatita más fuertes y resistentes a los ácidos en lugar de cristales de hidroxiapatita. [22]
Los apéndices del Odontodactylus scyllarus (camarón mantis pavo real) están hechos de una forma extremadamente densa del mineral que tiene una fuerza específica más alta; esto ha llevado a su investigación para posibles usos en síntesis e ingeniería. [23] Sus apéndices dáctilos tienen una excelente resistencia al impacto debido a que la región de impacto está compuesta principalmente de hidroxiapatita cristalina, que ofrece una dureza significativa. Una capa periódica debajo de la capa de impacto compuesta de hidroxiapatita con menor contenido de calcio y fósforo (lo que da como resultado un módulo mucho más bajo) inhibe el crecimiento de grietas al obligar a nuevas grietas a cambiar de dirección. Esta capa periódica también reduce la energía transferida a través de ambas capas debido a la gran diferencia de módulo, reflejando incluso parte de la energía incidente. [24]
A partir de 2019 [actualizar], el uso de hidroxiapatita, o su forma fabricada sintéticamente, nanohidroxiapatita, aún no es una práctica común. Algunos estudios sugieren que es útil para contrarrestar la hipersensibilidad de la dentina, prevenir la sensibilidad después de procedimientos de blanqueamiento dental y prevenir la caries. [25] [26] [27] La hidroxiapatita de cáscara de huevo aviar puede ser un material de relleno viable en procedimientos de regeneración ósea en cirugía oral. [28]
La nanohidroxiapatita posee componentes bioactivos que pueden impulsar el proceso de mineralización de los dientes, remediando la hipersensibilidad. Se cree que la hipersensibilidad de los dientes está regulada por el líquido que se encuentra dentro de los túbulos dentinarios. [25] Se dice que el movimiento de este líquido como resultado de diferentes estímulos excita las células receptoras en la pulpa y desencadena sensaciones de dolor. [25] Las propiedades físicas de la nanohidroxiapatita pueden penetrar y sellar los túbulos, deteniendo la circulación del líquido y por tanto las sensaciones de dolor derivadas de los estímulos. [26] Se preferiría la nanohidroxiapatita, ya que es paralela al proceso natural de remineralización de la superficie. [27]
En comparación con tratamientos alternativos para el alivio de la hipersensibilidad de la dentina, se ha demostrado que el tratamiento que contiene nanohidroxiapatita funciona mejor clínicamente. Se demostró que la nanohidroxiapatita es mejor que otros tratamientos para reducir la sensibilidad a los estímulos evaporativos, como una ráfaga de aire, y a los estímulos táctiles, como golpear el diente con un instrumento dental. Sin embargo, no se observaron diferencias entre la nanohidroxiapatita y otros tratamientos para los estímulos fríos. [29] La hidroxiapatita ha demostrado importantes efectos desensibilizantes a medio y largo plazo sobre la hipersensibilidad de la dentina mediante estímulos evaporativos y la escala analógica visual (junto con nitrato de potasio, arginina, glutaraldehído con metacrilato de hidroxietilo, hidroxiapatita, sistemas adhesivos, cementos de ionómero de vidrio y láser). [30]
Los agentes blanqueadores dentales liberan especies reactivas de oxígeno que pueden degradar el esmalte. [26] Para evitar esto, se puede agregar nanohidroxiapatita a la solución blanqueadora para reducir el impacto del agente blanqueador al bloquear los poros dentro del esmalte. [26] Esto reduce la sensibilidad después del proceso de decoloración. [27]
La nanohidroxiapatita posee un efecto remineralizante en los dientes y puede usarse para prevenir daños causados por ataques de caries. [27] En caso de un ataque ácido por parte de bacterias cariogénicas, las partículas de nanohidroxiapatita pueden infiltrarse en los poros de la superficie del diente para formar una capa protectora. [26] Además, la nanohidroxiapatita puede tener la capacidad de revertir el daño causado por ataques de caries, ya sea reemplazando directamente los minerales de la superficie deteriorados o actuando como un agente aglutinante para los iones perdidos. [26]
En algunas pastas de dientes, la hidroxiapatita se puede encontrar en forma de nanocristales (ya que se disuelven fácilmente). En los últimos años, los nanocristales de hidroxiapatita (nHA) se han utilizado en pastas de dientes para combatir la hipersensibilidad dental. Colaboran en la reparación y remineralización del esmalte , contribuyendo así a prevenir la sensibilidad dental. El esmalte dental puede desmineralizarse debido a diversos factores, entre ellos la erosión ácida y la caries dental . Si no se trata, esto puede provocar la exposición de la dentina y la posterior exposición de la pulpa dental . En varios estudios, el uso de nanohidroxiapatita en la pasta de dientes mostró resultados positivos para ayudar a la remineralización del esmalte dental. [31] Además de la remineralización, estudios in vitro han demostrado que las pastas dentales que contienen nanohidroxiapatita tienen el potencial de reducir la formación de biopelículas tanto en el esmalte dental como en las superficies compuestas a base de resina . [32]
La hidroxiapatita es muy utilizada dentro de la odontología y la cirugía oral y maxilofacial , debido a su similitud química con el tejido duro. [33]
En el futuro, existen posibilidades de utilizar nanohidroxiapatita para la ingeniería y reparación de tejidos. La característica principal y más ventajosa de la nanohidroxiapatita es su biocompatibilidad. [34] Es químicamente similar a la hidroxiapatita natural y puede imitar la estructura y función biológica de las estructuras que se encuentran en la matriz extracelular residente. [35] Por lo tanto, se puede utilizar como armazón para diseñar tejidos como el hueso y el cemento. [26] Puede usarse para restaurar labios y paladares leporinos y perfeccionar las prácticas existentes, como la preservación del hueso alveolar después de la extracción para una mejor colocación del implante. [26]
El Comité Científico para la Seguridad del Consumidor (SCCS) de la Comisión Europea emitió un dictamen oficial en 2021, en el que consideró si el nanomaterial hidroxiapatita era seguro cuando se usaba en productos cosméticos dérmicos y orales sin enjuague y sin enjuague, teniendo en cuenta las previsiones razonables. condiciones de exposición. Declaró: [36]
Tras considerar los datos facilitados y otra información pertinente disponible en la literatura científica, el SCCS no puede llegar a ninguna conclusión sobre la seguridad de la hidroxiapatita compuesta de nanopartículas en forma de varilla para su uso en productos cosméticos para el cuidado bucal en las concentraciones máximas y especificaciones indicadas en el presente dictamen. Esto se debe a que los datos/información disponibles no son suficientes para excluir preocupaciones sobre el potencial genotóxico del HAP-nano.
El Comité Científico para la Seguridad del Consumidor (SCCS) de la Comisión Europea volvió a emitir una opinión actualizada en 2023, donde eliminó las preocupaciones sobre la genotoxicidad de la nanohidroxiapatita en forma de varilla, lo que permite que los productos de consumo contengan concentraciones de nanohidroxiapatita de hasta el 10% para las pastas de dientes y 0,465% para enjuagues bucales. Sin embargo, advierte sobre la nanohidroxiapatita en forma de aguja y sobre la inhalación en productos en aerosol. Declaró: [37]
Según los datos proporcionados, el SCCS considera segura la hidroxiapatita (nano) cuando se utiliza en concentraciones de hasta el 10% en la pasta de dientes y hasta el 0,465% en el enjuague bucal. Esta evaluación de seguridad sólo se aplica a la hidroxiapatita (nano) con las siguientes características:
– compuestos por partículas en forma de varilla de las cuales al menos el 95,8% (en número de partículas) tienen una relación de aspecto inferior a 3, y el 4,2% restante tiene una relación de aspecto no superior a 4,9;
– las partículas no están recubiertas ni modificadas en su superficie.
Además de sus aplicaciones médicas, la hidroxiapatita también se utiliza en aplicaciones posteriores bajo cromatografía de modo mixto en el paso de pulido. Los iones presentes en la superficie de la hidroxiapatita la convierten en un candidato ideal con selectividad, separación y purificación únicas de mezclas de biomoléculas. En la cromatografía en modo mixto, la hidroxiapatita se utiliza como fase estacionaria en las columnas de cromatografía.
La presencia combinada de iones calcio (sitios C) y sitios fosfato (sitios P) proporciona afinidad por el metal y propiedades de intercambio iónico, respectivamente. Los sitios C en la superficie de la resina experimentan interacciones de afinidad metálica con grupos fosfato o carboxilo presentes en las biomoléculas. Al mismo tiempo, estos sitios C cargados positivamente tienden a repeler grupos funcionales cargados positivamente (p. ej., grupos amino) en las biomoléculas. Los sitios P sufren intercambio catiónico con grupos funcionales cargados positivamente en biomoléculas. Exhiben repulsión electrostática con grupos funcionales cargados negativamente en biomoléculas. Para la elución de moléculas se utiliza un tampón con alta concentración de fosfato y cloruro de sodio. La naturaleza de los diferentes iones cargados en la superficie de la hidroxiapatita proporciona el marco para una selectividad y unión únicas de biomoléculas, lo que facilita una separación sólida de biomoléculas.
La hidroxiapatita está disponible en diferentes formas y en diferentes tamaños para la purificación de proteínas. Las ventajas de los medios de hidroxiapatita son la alta estabilidad del producto y la uniformidad en varios lotes durante su producción. Generalmente, la hidroxiapatita se utilizó en la etapa de pulido de anticuerpos monoclonales, aislamiento de plásmidos libres de endotoxinas, purificación de enzimas y partículas virales. [38]
En arqueología , la hidroxiapatita de restos humanos y animales se puede analizar para reconstruir dietas , migraciones y paleoclimas antiguos. Las fracciones minerales de los huesos y los dientes actúan como reservorio de oligoelementos , entre ellos carbono, oxígeno y estroncio. El análisis de isótopos estables de hidroxiapatita humana y faunística puede utilizarse para indicar si una dieta era predominantemente de naturaleza terrestre o marina (carbono, estroncio); [39] el origen geográfico y los hábitos migratorios de un animal o un ser humano (oxígeno, estroncio) [40] y reconstruir temperaturas y cambios climáticos pasados (oxígeno). [41] La alteración post-deposicional del hueso puede contribuir a la degradación del colágeno óseo, la proteína necesaria para el análisis de isótopos estables. [42]
La hidroxiapatita es un adsorbente potencial para la defluoración del agua potable , ya que forma fluorapatita en un proceso de tres pasos. La hidroxiapatita elimina F - del agua para reemplazar OH - formando fluorapatita. Sin embargo, durante el proceso de defluoración, la hidroxiapatita se disuelve y aumenta el pH y la concentración de iones fosfato , lo que hace que el agua defluorada no sea apta para beber. [43] Recientemente, se sugirió una técnica de defluoración de ″hidroxiapatita modificada con calcio″ para superar la lixiviación de fosfato de la hidroxiapatita. [43] Esta técnica también puede afectar la reversión de la fluorosis al proporcionar agua potable alcalina enriquecida con calcio a las áreas afectadas por la fluorosis.
La materia inorgánica representa alrededor del 50% del peso seco del hueso... los cristales muestran imperfecciones y no son idénticos a la hidroxiapatita que se encuentra en los minerales de roca.
![]() Medios relacionados con la hidroxiapatita en Wikimedia Commons
Medios relacionados con la hidroxiapatita en Wikimedia Commons