Los lípidos de membrana son un grupo de compuestos (estructuralmente similares a las grasas y aceites) que forman la bicapa lipídica de la membrana celular . Las tres clases principales de lípidos de membrana son los fosfolípidos , los glicolípidos y el colesterol . Los lípidos son anfifílicos : tienen un extremo que es soluble en agua ('polar') y un extremo que es soluble en grasa ('apolar'). Al formar una doble capa con los extremos polares apuntando hacia afuera y los extremos apolares apuntando hacia adentro, los lípidos de membrana pueden formar una 'bicapa lipídica' que mantiene el interior acuoso de la célula separado del exterior acuoso. La disposición de los lípidos y varias proteínas, que actúan como receptores y poros de canal en la membrana, controla la entrada y salida de otras moléculas e iones como parte del metabolismo de la célula. Para realizar funciones fisiológicas, las proteínas de membrana pueden rotar y difundirse lateralmente en la extensión bidimensional de la bicapa lipídica gracias a la presencia de una capa de lípidos estrechamente adherida a la superficie de la proteína, denominada capa lipídica anular .
La bicapa formada por lípidos de membrana sirve como unidad de contención de una célula viva. Los lípidos de membrana también forman una matriz en la que residen las proteínas de membrana . Históricamente se pensaba que los lípidos solo cumplían una función estructural. De hecho, los papeles funcionales de los lípidos son muchos: sirven como agentes reguladores en el crecimiento y la adhesión celular . Participan en la biosíntesis de otras biomoléculas . Pueden servir para aumentar las actividades enzimáticas de las enzimas . [1]
Los lípidos que no forman bicapas, como el monogalactosil diglicérido (MGDG), predominan en las membranas tilacoidales y, cuando se hidratan solos, forman una fase cilíndrica hexagonal inversa. Sin embargo, en combinación con otros lípidos y carotenoides / clorofilas de las membranas tilacoidales, también se unen para formar bicapas lipídicas. [2]
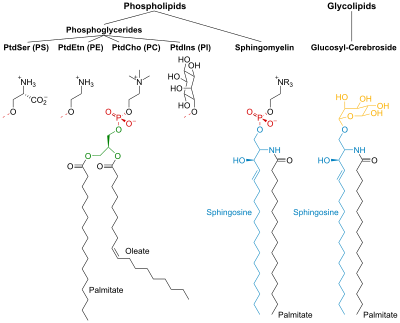
Los fosfolípidos y los glicolípidos constan de dos cadenas de hidrocarburos largas, no polares ( hidrofóbicas ) unidas a un grupo de cabeza hidrofílico .
Las cabezas de los fosfolípidos están fosforiladas y consisten en:
El tetraéter de dialquilglicerol glicerol (GDGT) está ayudando a estudiar factores ambientales antiguos . [3]
Las cabezas de los glicolípidos (glico- significa azúcar) contienen una esfingosina con una o varias unidades de azúcar unidas a ella. Las cadenas hidrófobas pertenecen a:
Los galactolípidos , el diglicérido de monogalactosil (MGDG) y el diglicérido de digalactosil (DGDG), forman los lípidos predominantes en las membranas tilacoides de los cloroplastos de las plantas superiores; se ha descubierto que las estructuras liposomales formadas por el extracto lipídico total de las membranas tilacoides son sensibles a la sacarosa, ya que convierte las bicapas en estructuras micelares. [4]
Los ácidos grasos en los fosfolípidos y glicolípidos suelen contener un número par, típicamente entre 14 y 24, de átomos de carbono , siendo los de 16 y 18 carbonos los más comunes. Los AG pueden ser saturados o insaturados, con la configuración de los dobles enlaces casi siempre cis . La longitud y el grado de insaturación de las cadenas de AG tienen un profundo efecto en la fluidez de las membranas . Las membranas tilacoides de las plantas mantienen una alta fluidez, incluso a temperaturas ambientales relativamente frías, debido a la abundancia de cadenas de acilo graso de 18 carbonos con tres dobles enlaces, ácido linolénico , como se ha revelado mediante estudios de RMN de 13-C. [5]
En los fosfoglicéridos , los grupos hidroxilo en C-1 y C-2 del glicerol se esterifican a los grupos carboxilo de los AG. El grupo hidroxilo C-3 se esterifica al ácido fosfórico. El compuesto resultante, llamado fosfatidato , es el fosfoglicerato más simple . Solo pequeñas cantidades de fosfatidato están presentes en las membranas. Sin embargo, es un intermediario clave en la biosíntesis de los otros fosfoglicéridos.
La esfingosina es un aminoalcohol que contiene una cadena hidrocarbonada larga e insaturada . En la esfingomielina y los glicolípidos, el grupo amino de la esfingosina está unido a los AG mediante un enlace amida . En la esfingomielina, el grupo hidroxilo primario de la esfingosina está esterificado a fosforilcolina .

En los glicolípidos, el componente de azúcar está unido a este grupo. El glicolípido más simple es el cerebrósido , en el que solo hay un residuo de azúcar, ya sea Glc o Gal . Los glicolípidos más complejos, como los gangliósidos , contienen una cadena ramificada de hasta siete residuos de azúcar.
El esterol más conocido es el colesterol , que se encuentra en los seres humanos. El colesterol también se encuentra de forma natural en las membranas de otras células eucariotas . Los esteroles tienen una estructura rígida de anillo fusionado de cuatro miembros hidrófobos y un pequeño grupo de cabeza polar.
El colesterol se biosintetiza a partir del mevalonato mediante una ciclización de escualeno de los terpenoides . Las membranas celulares requieren altos niveles de colesterol, típicamente un promedio de 20% de colesterol en toda la membrana, aumentando localmente en áreas de balsa hasta 50% de colesterol (- % es la relación molecular). [6] Se asocia preferentemente con esfingolípidos (ver diagrama) en áreas de balsas lipídicas ricas en colesterol de las membranas en células eucariotas. [7] La formación de balsas lipídicas promueve la agregación de proteínas periféricas y transmembrana, incluido el acoplamiento de las proteínas SNARE y VAMP . [8] Los fitoesteroles , como el sitosterol y el estigmasterol, y los hopanoides cumplen una función similar en plantas y procariotas .