La isosorbida es un compuesto químico bicíclico del grupo de los dioles y los heterociclos que contienen oxígeno , que contiene dos anillos de furano fusionados . El material de partida para la isosorbida es el D-sorbitol , que se obtiene por hidrogenación catalítica de la D-glucosa , que a su vez se produce por hidrólisis del almidón . La isosorbida se analiza como una plataforma química de origen vegetal a partir de la cual se pueden obtener derivados biodegradables de diversas funcionalidades .
En 2022, fue el 119.º medicamento más recetado en los Estados Unidos, con más de 5 millones de recetas. [1] [2]
Debido a su pronunciada higroscopicidad, la isosorbida se utiliza como humectante y en medicina como diurético osmótico (para el tratamiento de la hidrocefalia ) y el glaucoma agudo de ángulo cerrado . [3] Los dos grupos hidroxi secundarios hacen de la isosorbida una plataforma química versátil accesible a partir de recursos renovables. Como diol, la isosorbida puede monoderivatizarse o biderivatizarse utilizando los métodos estándar de la química orgánica , como la nitración , la esterificación , la eterificación , la tosilación , etc., y convertirse en compuestos con propiedades interesantes o en unidades monoméricas para nuevos polímeros. [4]
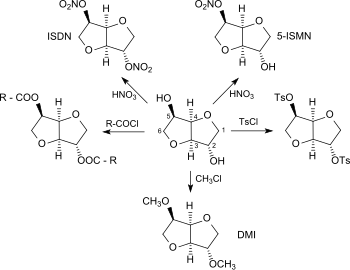
Mediante la nitración de isosorbida con ácido nítrico concentrado , se puede obtener dinitrato de 2,5-isosorbida (ISDN). El dinitrato de 2,5-isosorbida es adecuado (al igual que su principal metabolito, el mononitrato de 5-isosorbida , ISMN [5] ) para el tratamiento de la angina de pecho debido a su efecto vasodilatador . [6]
La esterificación de isosorbida con ácidos grasos permite obtener monoésteres de isosorbida, que son útiles como detergentes en limpiadores domésticos, detergentes para lavavajillas y preparaciones cosméticas, debido a sus propiedades como tensioactivos. [7] Los diésteres de isosorbida, también fácilmente disponibles [8], se utilizan como dispersantes para pigmentos, conservantes, estabilizadores de polímeros, como emulsionantes para cosméticos y como plastificantes para polímeros de vinilo (en particular, cloruro de polivinilo , PVC). El dioctanoato de isosorbida [9] es un diéster de isosorbida y ácido octanoico (obtenido a partir de aceite de palma , por ejemplo) y, por lo tanto, está hecho completamente de bloques de construcción de base biológica y ha sido utilizado como Polysorb ID 37 por Roquette Frères durante algún tiempo como un producto particularmente no tóxico. [10]
Los éteres de isosorbida (y en particular su representante más simple, 2,5-dimetilisosorbida, abreviado DMI), se utilizan cada vez más como disolvente renovable para preparaciones cosméticas y farmacéuticas, [11] como aditivo electrolítico para acumuladores de iones de litio [12] [18] y como aditivo de combustible para diésel . [13]
Los derivados del ácido fosfórico de isosorbida se están explorando como una alternativa respetuosa con el medio ambiente a los retardantes de llama que contienen halógenos . Hasta ahora, el 1,2,5,6,9,10-hexabromociclododecano (HBCD) se ha utilizado ampliamente como retardante de llama en espuma de poliestireno extruido (XPS) en el sector de la construcción y el aislamiento, pero se prohibió su fabricación y aplicación como SVHC ( sustancia altamente preocupante ) en mayo de 2013. Los compuestos de isosorbida a base de fósforo, como el bis (difenilfosfato) de isosorbida [ISTP], se consideran como un reemplazo.

El ISTP es fácilmente accesible mediante la transesterificación de isosorbida con fosfato de trifenilo en presencia de carbonato de potasio a 150 °C. El fosfato de isosorbida-bis-difenilo obtenido con un rendimiento del 88% como un aceite amarillento contiene alrededor del 20% de dímeros. [14] La alta temperatura de descomposición del ISTP permite su uso en XPS , aunque el alto efecto suavizante es un inconveniente. La retardancia de la llama es particularmente pronunciada en presencia de sinergistas que contienen azufre, como el bis(difenilfosfinotionil)disulfuro (BDPS). Esto permite alcanzar el requisito mínimo de protección contra incendios (clase B2) con solo un 3% de ISTP. [15]
Se ha examinado el isosorbide como una plataforma química potencial para la producción de diversos polímeros y resinas. [4] Los grupos hidroxi se pueden convertir en grupos amino primarios [4] a través de los tosilatos y azidas o mediante la adición de acrilonitrilo seguida de hidrogenación en los derivados aminopropílicos correspondientes. [16] Estos últimos tienen potencial para la preparación de poliuretanos, como diaminas para la preparación de poliamidas y como endurecedor para resinas epoxi.
Cuando el monoetilenglicol como diol se reemplaza por isosorbida en el tereftalato de polietileno de poliéster (PET), se obtiene tereftalato de poliisosorbida (PIT), que se caracteriza por una estabilidad térmica extrema (hasta 360 °C bajo nitrógeno). Sin embargo, la reactividad inherentemente menor de los grupos hidroxilo secundarios en isosorbida causa en comparación pesos moleculares más bajos y altos contenidos residuales de ácido tereftálico , lo que conduce a la estabilidad química insuficiente de los polímeros resultantes. Por lo tanto, los poliésteres actuales con isosorbida y monoetilenglicol se examinan como componentes de diol que muestran propiedades mejoradas, como una menor decoloración. [17] [18]
El isosorbide también es de interés como precursor de los policarbonatos . [19] En principio, podría reemplazar al bisfenol A , que se identificó como xenoestrógeno . Las limitaciones de los policarbonatos basados en isosorbide son su resistencia a la temperatura insatisfactoria y su resistencia limitada al impacto, que se puede mejorar mediante la adición de comonómeros al isosorbide o mediante mezclas de polímeros. [20]
El isosorbida, un diol, es un precursor de los poliuretanos In. [21] o como un bloque de construcción para el poliol [22] [29] Podría convertirse en el componente diisocianato [23] así como en un extensor de cadena. [24]
Al reaccionar isosorbida con epiclorhidrina , se forma isosorbida bis-glicidil éter [25] (un bis-epóxido), que podría usarse como reemplazo del análogo bis-epóxido de bisfenol A. El isosorbida bis-glicidil éter se puede reticular a resinas epoxi termoendurecibles con agentes de curado adecuados, tales como poliaminas o anhídridos de ácidos cíclicos . Estas resinas se utilizan como adhesivos, pinturas o recubrimientos para latas de alimentos. [26] Además, se describen polioxazolidonas que se pueden obtener por reacción de isosorbida diglicidil éteres con diisocianatos. [27] Las polioxazolidonas podrían encontrar uso como plásticos termoendurecibles rígidos, altamente ramificados y resistentes a los solventes en la industria eléctrica y electrónica.
La hidrogenación de la glucosa produce sorbitol . La isosorbida se obtiene por deshidratación catalizada por ácido del D- sorbitol , que produce el furanoide monocíclico sorbitán , [4] que a su vez forma por deshidratación adicional el derivado bicíclico furofurano isosorbida. [28]
La reacción produce entre un 70 y un 80% de isosorbida además de un 30 a un 20% de subproductos indeseables que deben eliminarse de forma costosa mediante destilación, recristalización en alcoholes, recristalización en la masa fundida [29] , mediante una combinación de estos métodos o mediante deposición desde la fase de vapor [30] . Un producto de alta pureza (> 99,8% [30] ) es esencial para el uso de un monómero cuando se deben obtener polímeros incoloros y de alto peso molecular.
La isosorbida es un sólido blanco, cristalino y altamente hidrófilo. Los dos grupos hidroxilo secundarios en el sistema bicíclico en forma de V poseen diferentes orientaciones que conducen a diferentes reactividades químicas. Esto permite una monoderivatización selectiva de la isosorbida. El grupo hidroxilo en la posición 5 está orientado endo y forma un enlace de hidrógeno con el átomo de oxígeno en el anillo de furano adyacente. Esto hace que el grupo hidroxilo en la posición 5 sea más nucleofílico y más reactivo que el grupo hidroxilo orientado exo en la posición 2; sin embargo, está más protegido del ataque de reactivos estéricamente exigentes. [31]
Con un valor LD 50 de 25,8 g·kg −1 (rata, oral [32] ), la isosorbida es igualmente no tóxica que la D-glucosa (también con un LD 50 de 25,8 g·kg −1 , rata, oral [33] ) y está clasificada por la Administración de Alimentos y Medicamentos (FDA) como GRAS (" generalmente reconocida como segura "). [34]
{{cite journal}}: CS1 maint: DOI inactivo a partir de noviembre de 2024 ( enlace )