El isocianato de metilo ( MIC ) es un compuesto orgánico con la fórmula molecular CH 3 NCO. Sinónimos son isocianatometano y metilcarbilamina . El isocianato de metilo es una sustancia química intermedia en la producción de pesticidas carbamatos (como carbarilo , carbofurano , metomilo y aldicarb ). También se ha utilizado en la producción de cauchos y adhesivos . Como compuesto extremadamente tóxico e irritante, es muy peligroso para la salud humana. El MIC fue el principal tóxico involucrado en el desastre del gas de Bhopal , que mató brevemente a entre 4.000 y 8.000 personas y causó lesiones permanentes y muertes prematuras a decenas de miles más. [6] [7] [8] [9] [10] También es un agente lacrimógeno muy potente . [11]
El isocianato de metilo es un líquido incoloro, venenoso, lacrimógeno ( agente desgarrador ) e inflamable. [12] Es soluble en agua en una proporción de 6 a 10 partes por 100 partes, pero también reacciona con el agua (consulte Reacciones a continuación).
Tiene un índice de refracción de 1,363 con una longitud de onda de 589 nm a una temperatura de 20 °C [13]
El isocianato de metilo suele fabricarse mediante la reacción de monometilamina y fosgeno . Para la producción a gran escala es ventajoso combinar estos reactivos a mayor temperatura en la fase gaseosa. Se forma una mezcla de isocianato de metilo y dos moles de cloruro de hidrógeno , pero se forma cloruro de N-metilcarbamoílo (MCC) a medida que se condensa la mezcla, dejando un mol de cloruro de hidrógeno en forma gaseosa.
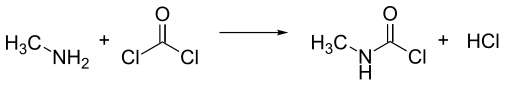
El isocianato de metilo se obtiene tratando el MCC con una amina terciaria , como N,N-dimetilanilina , o con piridina , [14] o separándolo mediante técnicas de destilación . [15]

El isocianato de metilo también se fabrica a partir de N-metilformamida y aire. En este último proceso, se consume inmediatamente en un proceso de circuito cerrado para producir metomilo . [16] Se han informado otros métodos de fabricación. [17] [18]
El isocianato de metilo reacciona fácilmente con muchas sustancias que contienen grupos NH u OH. Con agua, forma 1,3-dimetilurea y dióxido de carbono con el desprendimiento de calor (1358,5 julios, o 325 calorías, por gramo de MIC): reacciona relativamente lentamente por debajo de 68 °F, pero aumentará su velocidad con temperaturas elevadas o en presencia de ácidos o bases. [19]
A 25 °C, en exceso de agua, se consume la mitad de la MIC en 9 min.; [20] si el calor no se elimina eficientemente de la mezcla de reacción, la velocidad de la reacción aumentará y rápidamente hará que el MIC hierva. Esta reacción desencadenó el desastre de Bhopal después de que se introdujera una gran cantidad de agua en un tanque de almacenamiento del MIC. La consecuencia del proceso exotérmico fuera de control fue una reacción descontrolada y la liberación directa de 42 toneladas de MIC a la atmósfera.
Si la MIC está en exceso, se forma 1,3,5-trimetilbiuret junto con dióxido de carbono . [12] Los alcoholes y fenoles , que contienen un grupo OH, reaccionan lentamente con la MIC, pero la reacción puede ser catalizada por trialquilaminas o dicarboxilato de dialquilestaño. Las oximas , hidroxilaminas y enoles también reaccionan con la MIC para formar metilcarbamatos. [12] Estas reacciones producen los productos que se describen a continuación (Usos).
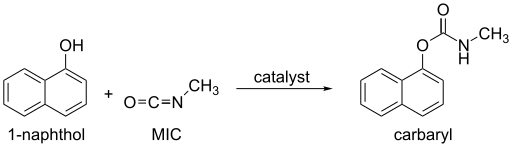
El amoníaco y las aminas primarias y secundarias reaccionan rápidamente con la MIC para formar ureas sustituidas . Otros compuestos de NH, como las amidas y las ureas , reaccionan mucho más lentamente con la MIC. [21]
También reacciona consigo mismo para formar un trímero o polímeros de mayor peso molecular. En presencia de catalizadores , la MIC reacciona consigo misma para formar un trímero sólido, isocianurato de trimetilo o un polímero de mayor peso molecular:

El metóxido de sodio , la trietilfosfina , el cloruro férrico y algunos otros compuestos metálicos catalizan la formación del trímero MIC, mientras que la formación del polímero de alto peso molecular es catalizada por determinadas trialquilaminas . Dado que la formación del trímero de MIC es exotérmica (1246 julios o 298 calorías por gramo de MIC), la reacción puede provocar una ebullición violenta de la MIC. El polímero de alto peso molecular se hidroliza en agua caliente para formar isocianurato de trimetilo . Dado que se pueden formar sales metálicas catalíticas a partir de impurezas en MIC y acero de calidad comercial, este producto no debe almacenarse en tambores o tanques de acero. [12]
El isocianato de metilo es extremadamente tóxico . No existe ningún antídoto conocido . El valor límite umbral establecido por la Conferencia Americana de Higienistas Industriales Gubernamentales es 0,02 ppm . La MIC es tóxica por inhalación, ingestión y contacto en cantidades tan bajas como 0,4 ppm . Los síntomas de exposición incluyen tos, dolor de pecho , disnea , asma , irritación de los ojos , nariz y garganta , así como daños en la piel . Niveles más altos de exposición, superiores a 21 ppm, pueden provocar edema pulmonar o pulmonar , enfisema y hemorragias , neumonía bronquial y la muerte . Aunque la mayoría de las personas no pueden detectar el olor del isocianato de metilo a 5 ppm, sus potentes propiedades lagrimales proporcionan una excelente advertencia de su presencia (a una concentración de 2 a 4 partes por millón (ppm) los ojos se irritan, mientras que a 21 ppm, los sujetos no podían tolerar la presencia de isocianato de metilo en el aire). [11]
Se debe tener el cuidado adecuado al almacenar isocianato de metilo debido a su facilidad de polimerización exotérmica (ver Reacciones) y su sensibilidad similar al agua. Sólo se pueden utilizar de forma segura recipientes de acero inoxidable o vidrio ; El MIC debe almacenarse a temperaturas inferiores a 40 °C (104 °F) y preferiblemente a 4 °C (39 °F). [ cita necesaria ]
El efecto tóxico del compuesto fue evidente en el desastre de Bhopal de 1984 , cuando alrededor de 42.000 kilogramos (93.000 libras) de isocianato de metilo y otros gases fueron liberados de los depósitos subterráneos de la fábrica de Union Carbide India Limited (UCIL), sobre una zona poblada en 3 de diciembre de 1984, matando a unas 3.500 personas inmediatamente, 8.000 personas en las primeras 48 horas y 15.000 más durante los años siguientes. 200.000 personas sufrieron efectos duraderos en la salud a causa del desastre. [22] [23]
Durante los incendios estructurales, los materiales naturales pueden contribuir a la liberación de isocianatos, incluido el isocianato de metilo. [24]
Hasta décadas recientes, el mecanismo de la toxicidad del isocianato de metilo en humanos era en gran medida desconocido o poco claro. [25] [26] El isocianato de metilo y otros isocianatos son electrófilos y actualmente se cree que causan toxicidad por la alquilación de biomoléculas. [27] Anteriormente se sospechaba que el mecanismo del isocianato de metilo era la carbamilación de la hemoglobina , interfiriendo así con su capacidad de unión de oxígeno y provocando hipoxia . Sin embargo, los experimentos demostraron que cuando se expusieron ratas y cobayas a isocianato de metilo en concentraciones superiores a la concentración letal media ( CL 50 , la concentración suficiente para matar al 50% de la población analizada), sólo el 2% de las moléculas de hemoglobina estaban carbamiladas, lo que sugiere que Probablemente este no sea el mecanismo de toxicidad. [28] [29]

El 30 de julio de 2015, los científicos informaron que tras el primer aterrizaje del módulo de aterrizaje Philae en la superficie del cometa 67/P , las mediciones realizadas por los instrumentos COSAC y Ptolomeo revelaron dieciséis compuestos orgánicos , cuatro de los cuales fueron vistos por primera vez en un cometa . incluyendo acetamida , acetona , isocianato de metilo y propionaldehído . [31] [32] [33]
En 2017, dos equipos de astrónomos utilizaron el interferómetro Atacama Large Millimeter Array (ALMA) , formado por 66 radiotelescopios en el desierto de Atacama (norte de Chile ), descubrieron la presencia de MIC alrededor de estrellas jóvenes similares al Sol. [30]
MIC es considerada una molécula prebiótica como explican los descubridores de los hallazgos de ALMA en IRAS 16293-2422 , un sistema múltiple de estrellas muy jóvenes: "Esta familia de moléculas orgánicas participa en la síntesis de péptidos y aminoácidos , que, en el forma de proteínas , son la base biológica de la vida tal como la conocemos". [30]
{{cite journal}}: Falta o está vacío |title=( ayuda )