La temperatura crítica más baja de la solución ( LCST ) o temperatura más baja del consoluto es la temperatura crítica por debajo de la cual los componentes de una mezcla son miscibles en todas las proporciones. [1] [2] La palabra inferior indica que la LCST es un límite inferior a un intervalo de temperatura de miscibilidad parcial, o miscibilidad solo para ciertas composiciones.
El comportamiento de fases de las soluciones poliméricas es una propiedad importante involucrada en el desarrollo y diseño de la mayoría de los procesos relacionados con polímeros. Las soluciones de polímeros parcialmente miscibles a menudo exhiben dos límites de solubilidad, la temperatura crítica superior de la solución (UCST) y la LCST, las cuales dependen de la masa molar y la presión. A temperaturas inferiores a LCST, el sistema es completamente miscible en todas las proporciones, mientras que por encima de LCST se produce una miscibilidad parcial de líquidos. [3] [4]
En el diagrama de fases de los componentes de la mezcla, el LCST es el mínimo compartido de las curvas cóncavas espinodal y binodal (o de coexistencia). En general , depende de la presión y aumenta en función del aumento de presión.
Para moléculas pequeñas, la existencia de una LCST es mucho menos común que la existencia de una temperatura crítica superior de solución (UCST), pero existen algunos casos. Por ejemplo, el sistema trietilamina -agua tiene un LCST de 19 °C, de modo que estas dos sustancias son miscibles en todas las proporciones por debajo de 19 °C pero no a temperaturas más altas. [1] [2] El sistema nicotina -agua tiene una LCST de 61 °C, y también una UCST de 210 °C a presiones lo suficientemente altas como para que exista agua líquida a esa temperatura. Por lo tanto, los componentes son miscibles en todas las proporciones por debajo de 61 °C y por encima de 210 °C (a alta presión) y parcialmente miscibles en el intervalo de 61 a 210 °C. [1] [2]
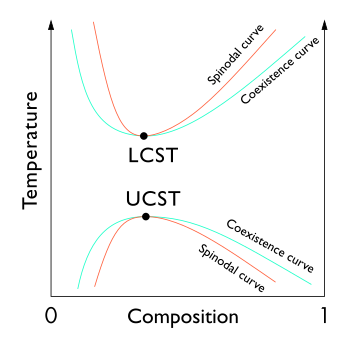
Algunas soluciones poliméricas tienen una LCST a temperaturas superiores a la UCST. Como se muestra en el diagrama, esto significa que hay un intervalo de temperatura de miscibilidad completa, con miscibilidad parcial tanto a temperaturas más altas como a temperaturas más bajas. [5]
En el caso de soluciones poliméricas, la LCST también depende del grado de polimerización , polidispersidad y ramificación del polímero [6] , así como de la composición y arquitectura del polímero. [7] Uno de los polímeros más estudiados cuyas soluciones acuosas exhiben LCST es la poli (N-isopropilacrilamida) . Aunque se cree ampliamente que esta transición de fase ocurre a 32 °C (90 °F), [8] las temperaturas reales pueden diferir de 5 a 10 °C (o incluso más) dependiendo de la concentración del polímero, [8] masa molar de cadenas de polímeros, dispersidad de polímeros y restos terminales. [8] [9] Además, otras moléculas en la solución de polímero, como sales o proteínas, pueden alterar la temperatura del punto de enturbiamiento. [10] [11] Otro monómero cuyos homopolímeros y copolímeros exhiben comportamiento LCST en solución es el metacrilato de 2-(dimetilamino)etilo. [12] [13] [14] [15] [16]
La LCST depende de la preparación del polímero y, en el caso de los copolímeros, de las proporciones de monómeros, así como de la naturaleza hidrófoba o hidrófila del polímero.
Hasta la fecha, se han encontrado más de 70 ejemplos de polímeros no iónicos con una LCST en solución acuosa. [17]
Un factor físico clave que distingue el LCST de otros comportamientos de mezcla es que la separación de fases del LCST está impulsada por una entropía de mezcla desfavorable . [18] Dado que la mezcla de las dos fases es espontánea por debajo del LCST y no por encima, el cambio de energía libre de Gibbs (ΔG) para la mezcla de estas dos fases es negativo por debajo del LCST y positivo por encima, y el cambio de entropía ΔS = – ( dΔG/dT) es negativo para este proceso de mezcla. Esto contrasta con el caso más común e intuitivo en el que las entropías impulsan la mezcla debido al mayor volumen accesible a cada componente durante la mezcla.
En general, la entropía desfavorable de la mezcla responsable del LCST tiene uno de dos orígenes físicos. La primera es asociar interacciones entre los dos componentes, como interacciones polares fuertes o enlaces de hidrógeno , que impiden la mezcla aleatoria. Por ejemplo, en el sistema trietilamina-agua, las moléculas de amina no pueden formar enlaces de hidrógeno entre sí sino sólo con moléculas de agua, por lo que en solución quedan asociadas a moléculas de agua con pérdida de entropía. La mezcla que se produce por debajo de 19 °C no se debe a la entropía sino a la entalpía de formación de los enlaces de hidrógeno.
El segundo factor físico que puede conducir a una LCST son los efectos de compresibilidad, especialmente en sistemas polímero-solvente. [18] Para sistemas no polares como el poliestireno en ciclohexano , se ha observado separación de fases en tubos sellados (a alta presión) a temperaturas cercanas al punto crítico líquido-vapor del disolvente. A tales temperaturas, el disolvente se expande mucho más rápidamente que el polímero, cuyos segmentos están unidos covalentemente. Por lo tanto, la mezcla requiere la contracción del solvente para la compatibilidad del polímero, lo que resulta en una pérdida de entropía. [5]
Dentro de la mecánica estadística , el LCST se puede modelar teóricamente mediante el modelo de fluido reticular, una extensión de la teoría de soluciones de Flory-Huggins , que incorpora vacantes y, por lo tanto, tiene en cuenta los efectos variables de densidad y compresibilidad. [18]
Hay tres grupos de métodos para correlacionar y predecir LCST. El primer grupo propone modelos que se basan en una sólida base teórica utilizando datos experimentales líquido-líquido o vapor-líquido. Estos métodos requieren datos experimentales para ajustar los parámetros desconocidos, lo que da como resultado una capacidad predictiva limitada. [19] Otro enfoque utiliza ecuaciones empíricas que correlacionan θ (LCST) con propiedades fisicoquímicas como la densidad, propiedades críticas, etc., pero tiene la desventaja de que estas propiedades no siempre están disponibles. [20] [21] Un nuevo enfoque propuesto por Liu y Zhong desarrolla modelos lineales para la predicción de θ(LCST) utilizando índices de conectividad molecular, que depende únicamente de las estructuras del disolvente y del polímero. [22] [23] Este último enfoque ha demostrado ser una técnica muy útil en la investigación de relaciones cuantitativas estructura-actividad/propiedad (QSAR/QSPR) para polímeros y soluciones poliméricas. Los estudios QSAR / QSPR constituyen un intento de reducir el elemento de prueba y error en el diseño de compuestos con actividad/propiedades deseadas mediante el establecimiento de relaciones matemáticas entre la actividad/propiedad de interés y parámetros medibles o computables, como los topológicos, fisicoquímicos y estereoquímicos. , o índices electrónicos. Más recientemente se han publicado modelos QSPR para la predicción de θ (LCST) utilizando descriptores moleculares (electrónicos, fisicoquímicos, etc.). [24] Utilizando modelos QSPR robustos validados, el tiempo y el esfuerzo experimentales se pueden reducir significativamente ya que se pueden obtener estimaciones confiables de θ (LCST) para soluciones poliméricas antes de que realmente se sinteticen en el laboratorio.
{{cite journal}}: CS1 maint: multiple names: authors list (link)