La hiperpolarización es la polarización del espín nuclear de un material en un campo magnético mucho más allá de las condiciones de equilibrio térmico determinadas por la distribución de Boltzmann . [1] Se puede aplicar a gases como 129 Xe y 3 He , y a moléculas pequeñas donde los niveles de polarización pueden mejorarse en un factor de 10 4 -10 5 por encima de los niveles de equilibrio térmico. Los gases nobles hiperpolarizados se utilizan normalmente en la resonancia magnética (MRI) de los pulmones. [2] Las moléculas pequeñas hiperpolarizadas se utilizan normalmente para obtener imágenes metabólicas in vivo . Por ejemplo, se puede inyectar un metabolito hiperpolarizado en animales o pacientes y se puede realizar un seguimiento de la conversión metabólica en tiempo real. Otras aplicaciones incluyen la determinación de la función de las estructuras de espín de los neutrones mediante la dispersión de electrones polarizados desde un objetivo muy polarizado ( 3 He), estudios de interacción de superficies y experimentos de polarización de neutrones. [3]
El bombeo óptico de intercambio de espín (SEOP) [3] es una de varias técnicas de hiperpolarización que se analizan en esta página. Esta técnica se especializa en crear gases nobles hiperpolarizados (HP), como 3 He, 129 Xe y 131 Xe cuadrupolar, 83 Kr y 21 Ne. [4] Se requieren gases nobles porque la SEOP se realiza en la fase gaseosa, son químicamente inertes, no reactivos, químicamente estables con respecto a los metales alcalinos y su T 1 es lo suficientemente largo como para generar polarización. Los gases nobles de espín 1/2 cumplen todos estos requisitos, y los gases nobles de espín 3/2 los cumplen hasta cierto punto, aunque algunos espines 3/2 no tienen una T 1 suficiente . Cada uno de estos gases nobles tiene su propia aplicación específica, como la caracterización del espacio y el tejido pulmonar mediante imágenes moleculares in vivo e imágenes funcionales de los pulmones, para estudiar cambios en el metabolismo de células sanas frente a células cancerosas, [4] o su uso como objetivos para la física nuclear. experimentos. [5] Durante este proceso, se utiliza luz láser infrarroja polarizada circularmente , sintonizada a la longitud de onda adecuada, para excitar electrones en un metal alcalino , como cesio o rubidio, dentro de un recipiente de vidrio sellado. La luz infrarroja es necesaria porque contiene las longitudes de onda necesarias para excitar los electrones de los metales alcalinos, aunque la longitud de onda necesaria para excitar los electrones del sodio está por debajo de esta región (Tabla 1).
El momento angular se transfiere de los electrones de los metales alcalinos a los núcleos de los gases nobles mediante colisiones. Como gas de extinción se utiliza nitrógeno, que evita la fluorescencia del metal alcalino polarizado, lo que conduciría a la despolarización del gas noble. Si la fluorescencia no se apagara, la luz emitida durante la relajación se polarizaría aleatoriamente, trabajando en contra de la luz láser polarizada circularmente. Si bien se utilizan diferentes tamaños de recipientes de vidrio (también llamados celdas) y, por lo tanto, diferentes presiones, según la aplicación, un amagat de presión total de gas noble y nitrógeno es suficiente para SEOP y se necesitan 0,1 amagat de densidad de nitrógeno para apagar la fluorescencia. [3] Grandes mejoras en la tecnología de hiperpolarización 129 Xe han logrado un nivel > 50 % a velocidades de flujo de 1 a 2 L/min, lo que permite aplicaciones clínicas en humanos. [9]
El descubrimiento de SEOP tardó décadas en encajar todas las piezas para crear una técnica completa. Primero, en 1897, los estudios de Zeeman sobre el vapor de sodio condujeron al primer resultado del bombeo óptico . [4] [10] La siguiente pieza se encontró en 1950 cuando Kastler determinó un método para polarizar electrónicamente el vapor de metal alcalino de rubidio utilizando un campo magnético aplicado e iluminando el vapor con luz resonante polarizada circularmente. [4] Diez años más tarde, Marie-Anne Bouchiat , TM Carver y CM Varnum realizaron un intercambio de espín , en el que la polarización del espín electrónico se transfirió a los espines nucleares de un gas noble ( 3 He y 129 Xe) a través de colisiones en fase gaseosa. [4] Desde entonces, este método se ha mejorado y ampliado enormemente para utilizarlo con otros gases nobles y metales alcalinos.

Para explicar más fácilmente los procesos de excitación, bombeo óptico e intercambio de espín, se utilizará como ejemplo el metal alcalino más común utilizado para este proceso, el rubidio. El rubidio tiene un número impar de electrones, y solo uno en la capa más externa puede excitarse en las condiciones adecuadas. Hay dos transiciones que pueden ocurrir, una denominada línea D 1 donde ocurre la transición del estado 5 2 S 1/2 al estado 5 2 P 1/2 y otra referida a la línea D 2 donde ocurre la transición. del estado 5 2 S 1/2 al estado 5 2 P 3/2 . [7] [11] Las transiciones D 1 y D 2 pueden ocurrir si los átomos de rubidio se iluminan con luz a una longitud de onda de 794,7 nm y 780 nm, respectivamente (Figura 1). [7] Si bien es posible causar cualquiera de las dos excitaciones, la tecnología láser está bien desarrollada para provocar que se produzca la transición D 1 . Se dice que esos láseres están sintonizados a la longitud de onda D 1 (794,7 nm) del rubidio.

Para aumentar el nivel de polarización por encima del equilibrio térmico, se deben alterar las poblaciones de los estados de espín. En ausencia de campo magnético, los dos estados de espín de un espín I = ½ núcleos están en el mismo nivel de energía, pero en presencia de un campo magnético, los niveles de energía se dividen en m s = ±1/2 niveles de energía (Figura 2). [12] Aquí, m s es el momento angular de giro con posibles valores de +1/2 (giro hacia arriba) o -1/2 (giro hacia abajo), a menudo dibujados como vectores que apuntan hacia arriba o hacia abajo, respectivamente. La diferencia de población entre estos dos niveles de energía es lo que produce una señal de RMN. Por ejemplo, los dos electrones en el estado de giro hacia abajo cancelan dos de los electrones en el estado de giro hacia arriba, dejando solo un núcleo de giro hacia arriba para detectar con RMN. Sin embargo, las poblaciones de estos estados pueden alterarse mediante hiperpolarización, lo que permite que el nivel de energía de giro esté más poblado y, por lo tanto, aumente la señal de RMN. Esto se hace primero bombeando ópticamente metal alcalino y luego transfiriendo la polarización a un núcleo de gas noble para aumentar la población del estado de giro.

La absorción de la luz láser por el metal alcalino es el primer proceso en SEOP. [3] La luz polarizada circularmente hacia la izquierda sintonizada con la longitud de onda D 1 del metal alcalino excita los electrones del estado de giro hacia abajo 2 S 1/2 (m s =-1/2) al estado de giro hacia arriba 2 P 1/2 ( m s =+1/2), donde se produce la mezcla por colisión cuando los átomos del gas noble chocan con los átomos de metales alcalinos y el estado m s =-1/2 está parcialmente poblado (Figura 3). [3] La luz polarizada circularmente es necesaria en campos magnéticos bajos porque permite que solo se absorba un tipo de momento angular, lo que permite polarizar los espines. [3] Luego se produce la relajación desde los estados excitados (m s =±1/2) a los estados fundamentales (m s =±1/2) cuando los átomos chocan con el nitrógeno, extinguiendo así cualquier posibilidad de fluorescencia y provocando que los electrones regresar a los dos estados fundamentales en poblaciones iguales. [3] Una vez que los espines se despolarizan (vuelven al estado m s =-1/2), son excitados nuevamente por la luz láser de onda continua y el proceso se repite. De esta manera, se acumula una mayor población de espines de electrones en el estado m s =+1/2. La polarización del rubidio, P Rb , se puede calcular utilizando la siguiente fórmula:
Donde n ↑ y n ↓ y son el número de átomos en los estados de giro hacia arriba (m S =+1/2) y giro hacia abajo (m S =-1/2) 2 S 1/2 . [13]

A continuación, el metal alcalino bombeado ópticamente choca con el gas noble, lo que permite que se produzca un intercambio de espín donde la polarización electrónica del metal alcalino se transfiere a los núcleos del gas noble (Figura 4). Hay dos mecanismos en los que esto puede ocurrir. El momento angular se puede transferir mediante colisiones binarias (Figura 4A, también llamadas colisiones de dos cuerpos) o mientras el gas noble, el gas tampón N 2 y el metal alcalino en fase de vapor se mantienen muy cerca mediante fuerzas de van der Waals (Figura 4B, también llamadas colisiones de tres cuerpos). [3] En los casos en los que las fuerzas de Van der Waals son muy pequeñas en comparación con las colisiones binarias (como es el caso del 3 He), el gas noble y el metal alcalino chocan y la polarización se transfiere de la AM al gas noble. [3] Las colisiones binarias también son posibles para 129 Xe. A altas presiones dominan las fuerzas de van der Waals, pero a bajas presiones dominan las colisiones binarias. [3]
Este ciclo de excitación, polarización, despolarización y repolarización, etc. toma tiempo antes de que se logre una polarización neta. La acumulación de polarización nuclear, P N (t), viene dada por:
Donde ⟨P A ⟩ es la polarización del metal alcalino, γ SE es la tasa de intercambio de espín y Γ es la tasa de relajación longitudinal del gas noble. [14] La relajación de la polarización nuclear puede ocurrir a través de varios mecanismos y se escribe como una suma de estas contribuciones:
Donde Γ t , Γ p , Γ g y Γ w representan la relajación del dímero Xe 2 transitorio , el dímero Xe 2 persistente , la difusión a través de gradientes en el campo magnético aplicado y la relajación de la pared, respectivamente. [14] En la mayoría de los casos, los mayores contribuyentes a la relajación total son los dímeros persistentes y las relajaciones de la pared. [14] Un dímero Xe 2 puede ocurrir cuando dos átomos de Xe chocan y se mantienen unidos mediante fuerzas de van der Waals, y puede romperse cuando un tercer átomo choca con él. [15] Es similar a Xe-Rb durante el intercambio de espín (transferencia de espín), donde se mantienen muy cerca uno del otro a través de fuerzas de van der Waals. [15] La relajación de la pared se produce cuando el Xe hiperpolarizado choca con las paredes de la célula y se despolariza debido a las impurezas paramagnéticas del vidrio.
La constante de tiempo de acumulación, Γ B , se puede medir recogiendo espectros de RMN en intervalos de tiempo que caen dentro del tiempo necesario para alcanzar la polarización en estado estacionario (es decir, la polarización máxima que se puede lograr, vista por la salida de señal máxima). Luego, las integrales de señal se trazan a lo largo del tiempo y pueden ajustarse para obtener la constante de tiempo de acumulación. Se puede utilizar la recopilación de una curva de acumulación a varias temperaturas diferentes y trazar los valores en función de la densidad de vapor del metal alcalino (ya que la densidad de vapor aumenta con un aumento en la temperatura de la celda) para determinar la tasa de destrucción de espín y la tasa de intercambio de espín por átomo usando :
Donde γ' es la tasa de intercambio de espín por átomo, [AM] es la densidad de vapor del metal alcalino y Γ SD es la tasa de destrucción de espín. [16] Esta gráfica debe ser lineal, donde γ' es la pendiente y Γ SD es la intersección con el eje y.
El bombeo óptico de intercambio de espín puede continuar indefinidamente con iluminación continua, pero hay varios factores que causan la relajación de la polarización y, por lo tanto, el retorno a las poblaciones de equilibrio térmico cuando se detiene la iluminación. Para utilizar gases nobles hiperpolarizados en aplicaciones como imágenes pulmonares, el gas debe transferirse desde la configuración experimental a un paciente. Tan pronto como el gas deja de ser bombeado ópticamente de forma activa, el grado de hiperpolarización comienza a disminuir hasta alcanzar el equilibrio térmico. Sin embargo, la hiperpolarización debe durar el tiempo suficiente para transferir el gas al paciente y obtener una imagen. El tiempo de relajación del espín longitudinal, denominado T 1 , se puede medir fácilmente recogiendo espectros de RMN a medida que la polarización disminuye con el tiempo una vez que se detiene la iluminación. Esta tasa de relajación está gobernada por varios mecanismos de despolarización y se escribe como:
Donde los tres términos contribuyentes son relajación por colisión (CR), relajación por falta de homogeneidad del campo magnético (MFI) y relajación causada por la presencia de oxígeno paramagnético (O2). [17] La duración de T 1 podría ser desde minutos hasta varias horas, dependiendo de cuánto cuidado se ponga en disminuir los efectos de CR, MFI y O 2 . El último término se ha cuantificado en 0,360 s −1 amagat −1 , [18] pero el primer y segundo términos son difíciles de cuantificar ya que el grado de su contribución al T 1 general depende de qué tan bien se haya realizado la configuración experimental y la celda. están optimizados y preparados. [18]

Para realizar SEOP, primero es necesario preparar la celda óptica. Las celdas ópticas (Figura 5) están diseñadas para el sistema particular en mente y el vidrio se sopla utilizando un material transparente, generalmente vidrio pyrex (borosilicato). Luego, esta celda debe limpiarse para eliminar todos los contaminantes, particularmente los materiales paramagnéticos que disminuyen la polarización y la T 1 . Luego se recubre la superficie interna de la celda para (a) servir como capa protectora para el vidrio con el fin de disminuir la posibilidad de corrosión por el metal alcalino, y (b) minimizar la despolarización causada por las colisiones de moléculas de gas polarizadas con el paredes de la célula. [19] La disminución de la relajación de la pared conduce a una polarización mayor y más prolongada del gas noble. [19]
Si bien se han probado varios recubrimientos a lo largo de los años, SurfaSil (Figura 6, ahora denominado fluido siliconante soluble en hidrocarburos) es el recubrimiento más común utilizado en una proporción de 1:10 SurfaSil:hexano porque proporciona valores T 1 prolongados. [19] El espesor de la capa de SurfaSil es de aproximadamente 0,3-0,4 μm. [19] Una vez recubierta y seca uniformemente, la celda se coloca en un ambiente inerte y se coloca una gota de metal alcalino (≈200 mg) en la celda, que luego se dispersa para crear un recubrimiento uniforme en las paredes de las celdas. . Un método para transferir el metal alcalino a la celda es mediante destilación. [20] En el método de destilación, la celda está conectada a un colector de vidrio equipado para contener gas presurizado y vacío, donde se conecta una ampolla de metal alcalino. [21] Se aspiran el colector y la celda, luego se rompe el sello de la ampolla y el metal alcalino se mueve hacia la celda usando la llama de un soplete de gas. [21] A continuación, la celda se llena con la mezcla de gases deseada de nitrógeno y gas noble. [5] Se debe tener cuidado de no envenenar la célula en ninguna etapa de su preparación (exponer la célula al aire atmosférico).
A lo largo de los años se han utilizado varios tamaños y diseños de celdas. La aplicación deseada es la que rige el diseño de la celda de bombeo óptico y depende del diámetro del láser, las necesidades de optimización y las consideraciones de uso clínico. Los gases y metales alcalinos específicos también se eligen en función de las aplicaciones deseadas.

Una vez que la celda está completa, se pega con cinta adhesiva una bobina de superficie (o bobinas, según el tipo de bobina deseado) al exterior de la celda, lo que a) permite que se produzcan pulsos de RF para inclinar los espines polarizados hacia el campo de detección ( plano x,y) yb) detecta la señal producida por los espines nucleares polarizados. La celda se coloca en un horno que permite calentar la celda y su contenido para que el metal alcalino entre en la fase de vapor, y la celda se centra en un sistema de bobina que genera un campo magnético aplicado (a lo largo del eje z). Luego se alinea un láser, sintonizado con la línea D 1 (transición dipolo eléctrico [14] ) del metal alcalino y con un diámetro de haz que coincide con el diámetro de la celda óptica, con las partes planas ópticas de la celda de tal manera que La totalidad de la celda se ilumina con luz láser para proporcionar la mayor polarización posible (Figura 7). El láser puede tener entre decenas de vatios y cientos de vatios, [3] donde mayor potencia produce una mayor polarización pero es más costoso. Para aumentar aún más la polarización, se coloca un espejo retrorreflectante detrás de la celda para hacer pasar la luz láser a través de la celda dos veces. Además, se coloca un iris IR detrás del espejo, que proporciona información sobre la absorción de la luz láser por parte de los átomos de metales alcalinos. Cuando el láser ilumina la célula, pero ésta está a temperatura ambiente, se utiliza el iris IR para medir el porcentaje de transmitancia de la luz láser a través de la célula. A medida que la celda se calienta, el rubidio entra en la fase de vapor y comienza a absorber la luz láser, lo que hace que el porcentaje de transmitancia disminuya. La diferencia en el espectro IR entre un espectro a temperatura ambiente y un espectro tomado mientras la celda se calienta se puede utilizar para calcular un valor estimado de polarización de rubidio, P Rb .
A medida que SEOP continúa desarrollándose y mejorando, existen varios tipos de bobinas de RMN, hornos, bobinas generadoras de campos magnéticos y láseres que se han utilizado y se utilizan para generar gases hiperpolarizados. Generalmente, las bobinas de RMN se fabrican a mano para un propósito específico, ya sea girando alambre de cobre a mano en la forma deseada [22] o imprimiendo la bobina en 3D. [23] Comúnmente, el horno es un horno de aire forzado, con dos caras hechas de vidrio para que la luz láser pase a través de la celda, una tapa removible y un orificio a través del cual se conecta una línea de aire caliente, que permite que la celda calentarse por conducción. [24] Las bobinas generadoras de campo magnético pueden ser un par de bobinas de Helmholtz, utilizadas para generar la intensidad del campo magnético deseada, [24] cuyo campo deseado se rige por:
Donde ω es la frecuencia de Larmour, o frecuencia de detección deseada, γ es la relación giromagnética de los núcleos de interés y B 0 es el campo magnético requerido para detectar los núcleos a la frecuencia deseada. [25] También se puede utilizar un conjunto de cuatro bobinas electromagnéticas (es decir, de Acutran) [22] y se están probando otros diseños de bobinas.
En el pasado, la tecnología láser era un factor limitante para SEOP, donde solo se podían utilizar unos pocos metales alcalinos debido a la falta de, por ejemplo, láseres de cesio. Sin embargo, ha habido varios desarrollos nuevos, incluidos mejores láseres de cesio, mayor potencia, ancho espectral más estrecho, etc., que están permitiendo que aumente el alcance de SEOP. Sin embargo, se requieren varias características clave. Lo ideal es que el láser sea de onda continua para garantizar que el metal alcalino y el gas noble permanezcan polarizados en todo momento. Para inducir esta polarización, la luz láser debe polarizarse circularmente en la dirección que permita que los electrones se polaricen por espín. Esto se hace pasando la luz láser a través de un divisor de haz polarizador para separar los componentes s y p , luego a través de una placa de cuarto de onda, que convierte la luz polarizada linealmente en luz polarizada circularmente. [17]
SEOP se ha utilizado con éxito y está bastante bien desarrollado para 3 He, 129 Xe y 83 Kr para aplicaciones biomédicas. [4] Además, se están realizando varias mejoras para obtener imágenes mejoradas e interpretables de las células cancerosas en la ciencia biomédica. [26] Se están realizando estudios que involucran la hiperpolarización de 131 Xe, lo que despierta el interés de los físicos. También se están realizando mejoras para permitir que no solo se utilice rubidio en la transferencia de espín, sino también cesio. En principio, se puede utilizar cualquier metal alcalino para SEOP, pero normalmente se prefiere el rubidio debido a su alta presión de vapor, lo que permite realizar experimentos a temperaturas relativamente bajas (80 °C-130 °C), lo que disminuye la posibilidad de dañar el metal alcalino. celda de vidrio. [3] Además, la tecnología láser para el metal alcalino de elección debe existir y desarrollarse lo suficiente como para lograr una polarización sustancial. Anteriormente, los láseres disponibles para excitar la transición de cesio D 1 no estaban bien desarrollados, pero ahora son cada vez más potentes y menos costosos. Los estudios preliminares incluso muestran que el cesio puede proporcionar mejores resultados que el rubidio, a pesar de que el rubidio ha sido el metal alcalino elegido para SEOP.
El método de hiperpolarización llamado bombeo óptico de intercambio de espín (SEOP) se utiliza para hiperpolarizar gases nobles como el xenón-129 y el helio-3. Cuando se obtienen imágenes de un gas hiperpolarizado inhalado como 3He o 129Xe, hay una mayor densidad de magnetización de moléculas activas en RMN en el pulmón en comparación con las imágenes tradicionales de 1H, lo que mejora las imágenes de resonancia magnética que se pueden obtener. A diferencia de la resonancia magnética de protones, que informa sobre las características anatómicas de los tejidos pulmonares, XenonMRI informa la función pulmonar, incluida la ventilación, difusión y perfusión de gas. [27]
Nuestro objetivo es identificar la infección o enfermedad (cáncer, por ejemplo) en cualquier parte de nuestro cuerpo como cerebro, cerebro, sangre, fluidos y tejidos. Esta célula infecciosa se denomina colectivamente biomarcador. [28] Según la Organización Mundial de la Salud (OMS) y en colaboración con las Naciones Unidas y la Organización Internacional del Trabajo han definido de manera convincente el biomarcador como “cualquier sustancia, estructura o proceso que puede medirse en el cuerpo o sus productos e influir o predecir la incidencia del resultado o enfermedad”. El biomarcador debe ser cuantificable hasta cierto nivel en el proceso biológico del bienestar. [28]
Un ejemplo específico de biomarcador es el colesterol en sangre, que comúnmente conocemos como confiable para la enfermedad coronaria; Otro biomarcador es el PSA (antígeno prostático específico) y ha contribuido al cáncer de próstata. [28] Hay muchos biomarcadores que se consideran cáncer: ácido ribonucleico del virus de la hepatitis C (ARN-VHC), índice normalizado internacional (INR), tiempo de protrombina (TP), proteína monoclonal (proteína M), antígeno canceroso-125. (CA-125), Virus de la Inmunodeficiencia Humana -Ácido Ribonucleico (ARN del VIH), Péptido Natriurético tipo B (BNP). 27 y células de linfoma (líneas celulares Ramos y líneas celulares Jurkat), una forma de cáncer. [29]
Otros biomarcadores comunes son el cáncer de mama, el cáncer de ovario, el cáncer colorrectal, el cáncer de pulmón y el tumor cerebral. [30]
Este agente patógeno es un biomarcador que existe en cantidades extremadamente pequeñas, especialmente en el estado inicial de la enfermedad. Por lo tanto, identificar u obtener imágenes de biomarcadores es complicado y, en algunas circunstancias, incierto para la tecnología de RMN. Por lo tanto, debemos utilizar el agente de contraste para mejorar las imágenes al menos a nivel de visualización para los médicos. Como moléculas de biomarcador es menos abundante en el sistema vivo. El experimento de RMN o RM proporciona una señal muy pequeña, incluso en algunos casos, el analizador puede perder el pico de señal en los datos debido a la falta de biomarcadores. Por lo tanto, para asegurarnos de llegar a la verdadera conclusión sobre la existencia de biomarcadores que causan problemas, necesitamos mejorar la sonda (mecanismos de contraste) para obtener el pico claro en el nivel más visible de altura del pico, así como la posición del pico de datos. Si es posible recopilar datos aceptables y claramente interpretables de los experimentos de RMN o RMN utilizando el agente de contraste, entonces los expertos podrán dar un paso inicial correcto para recuperar a los pacientes que ya han padecido cáncer. [28] Entre las diversas técnicas para obtener datos mejorados en el experimento de resonancia magnética, SEOP es una de ellas.
Los investigadores de SEOP están interesados en utilizar el 129 Xe. [ cita necesaria ] Porque 129 Xe tiene una serie de hechos favorables en NMR Tech. para actuar como agente de contraste incluso sobre los otros gases novedosos:

Solubilidad del xenón en medio acuoso 11% significa que a 25 °C 100 ml de agua podrían absorber 11 ml de gas xenón.
Figura 9 a continuación. En los datos experimentales de RMN, existen diferentes valores de desplazamiento químico para diferentes tejidos en un entorno in vivo . Todos los picos están posicionados a través de un rango tan grande de valores de desplazamiento químico que el 129 Xe es viable. Porque 129 Xe tiene un rango de valores de cambio químico de largo alcance de hasta 1700 ppm en datos de RMN. [ cita necesaria ] Otra información espectral importante incluye:
Figura 9. Datos de RMN para el biosensor Xe-129 en un sistema biológico in vivo . [ cita necesaria ]

(Figura-10) 129 Xe (g) muestra una mejora satisfactoria en la polarización durante SEOP en comparación con la mejora térmica en la polarización. Esto se demuestra por los valores de los datos experimentales cuando los espectros de RMN se adquieren con diferentes intensidades de campo magnético. [22] Un par de puntos importantes de los datos experimentales son:
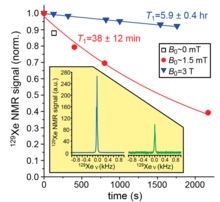
(Figura 11) El tiempo de relajación del espín longitudinal (T 1 ) es muy sensible con un aumento del campo magnético y, por lo tanto, se nota una mejora en las señales de RMN en SEOP en el caso de 129 Xe. [22] Como T 1 es mayor para el acondicionamiento de la marca azul, el experimento de RMN muestra un pico más mejorado en comparación con otros. [22] Para 129 Xe hiperpolarizado en bolsas de tedlar, el T 1 es de 38 ± 12 minutos cuando los datos se recopilan en presencia de un campo magnético de 1,5 mT. Sin embargo, se observó un incremento satisfactorio en el tiempo de retardo de T 1 (354 ± 24 minutos) cuando los datos se recopilaron en presencia de un campo magnético de 3000 mT. [22]
En general, podemos utilizar átomos de metal alcalino de 87 Rb o 133 Cs con gas nitrógeno inerte. Sin embargo, estamos utilizando átomos de 133 Cs con nitrógeno para realizar el intercambio de espín con 129 Xe para obtener varias ventajas:
Aunque el 129 Xe tiene muchas aplicaciones características preferibles en la técnica de RMN, el 83 Kr también se puede utilizar ya que tiene muchas ventajas en las técnicas de RMN de diferentes maneras que el 129 Xe.
También se están tomando medidas en el mundo académico y la industria para utilizar este gas hiperpolarizado para obtener imágenes de los pulmones. Una vez que el gas ( 129 Xe) se hiperpolariza a través del proceso SEOP y se elimina el metal alcalino, un paciente (ya sea sano o que padece una enfermedad pulmonar) puede respirar el gas y se puede realizar una resonancia magnética. [34] Esto da como resultado una imagen de los espacios en los pulmones llenos de gas. Si bien el proceso para llegar al punto de obtención de imágenes del paciente puede requerir conocimientos de científicos muy familiarizados con esta técnica y el equipo, se están tomando medidas para eliminar la necesidad de este conocimiento para que un técnico del hospital pueda producir el gas hiperpolarizado. utilizando un polarizador. [22] [23]
Actualmente se están utilizando máquinas de hiperpolarización para desarrollar gas xenón hiperpolarizado que se utiliza como agente de visualización para los pulmones. El xenón-129 es un gas noble inerte seguro que puede utilizarse para cuantificar la función pulmonar. Con una única retención de la respiración de 10 segundos, se utiliza xenón-129 hiperpolarizado con resonancia magnética para permitir imágenes pulmonares tridimensionales. [35] La resonancia magnética con xenón se utiliza para monitorear pacientes con enfermedad pulmonar vascular pulmonar, obstructiva o fibrótica. [36]
129 Xe SEOP con aumento de temperatura en un modelo por lotes automatizado de alto rendimiento hiperpolarizado 129 Xe puede utilizar tres rangos de temperatura principales para establecer ciertas condiciones: primero, la tasa de hiperpolarización de 129 Xe es superlativamente alta en condiciones de calor. En segundo lugar, en condiciones cálidas la hiperpolarización de 129 Xe es la unidad. En tercer lugar, en condiciones de frío, el nivel de hiperpolarización del gas 129 Xe al menos puede obtener imágenes (a la temperatura del cuerpo humano), aunque durante la transferencia a la bolsa Tedlar tiene un porcentaje pobre de 87 Rb (dosis de menos de 5 ng/L). [37]
El análisis multiparamétrico de 87 Rb/ 129 Xe SEOP a alta presión de xenón y flujo de fotones podría usarse como impresión 3D y agente de contraste de flujo detenido a escala clínica. [38] Técnica in situ , la máquina de RMN se ejecutó para rastrear la dinámica de la polarización de 129 Xe como una función del acondicionamiento de la celda SEOP con diferentes parámetros operativos, como la temperatura de recolección de datos, el flujo de fotones y la presión parcial de 129 Xe para mejorar el 129. Polarización Xe ( P Xe ). [38]
Todos esos valores de polarización de 129 Xe se aprobaron empujando el gas 129 Xe hiperpolarizado y todos los experimentos de resonancia magnética también se realizaron en un campo magnético inferior de 47,5 mT. [38] Finalmente, las demostraciones indicaron que en una región de tan alta presión, la polarización de los gases 129 Xe podría incrementarse aún más que el límite que ya se ha demostrado. Se ha mejorado aún más la mejor gestión térmica de SEOP y la optimización de la cinética de polarización con buena eficacia. [38]
El SEOP no sólo se puede utilizar para hiperpolarizar gases nobles, sino que un desarrollo más reciente es el SEOP en sólidos. Se realizó por primera vez en 2007 [21] y se utilizó para polarizar núcleos en un sólido, permitiendo que los núcleos que no pueden polarizarse mediante otros métodos se hiperpolaricen. [21] Por ejemplo, la polarización nuclear del 133 Cs en forma de una película sólida de CsH puede aumentar por encima del límite de Boltzmann. [21] Esto se hace bombeando primero ópticamente vapor de cesio y luego transfiriendo la polarización del espín a la sal de CsH, lo que produce una mejora de 4,0. [21]
Las celdas se fabrican como se describió anteriormente mediante destilación, luego se llenan con gas hidrógeno y se calientan para permitir que el metal Cs reaccione con el hidrógeno gaseoso para formar la sal CsH. [21] Se eliminó el hidrógeno que no había reaccionado y el proceso se repitió varias veces para aumentar el espesor de la película de CsH, luego se presurizó con gas nitrógeno. [21] Por lo general, los experimentos SEOP se realizan con la celda centrada en Helmholtz o bobinas electromagnéticas, como se describió anteriormente, pero estos experimentos se realizaron en un imán superconductor de 9,4 T haciendo brillar el láser a través del imán y calentando eléctricamente la celda. [21] En el futuro, puede ser posible utilizar esta técnica para transferir polarización a 6 Li o 7 Li, lo que conducirá a aún más aplicaciones ya que se espera que el T 1 sea más largo. [21] Desde el descubrimiento de esta técnica que permite caracterizar sólidos, se ha mejorado de tal manera que no es necesaria la luz polarizada para polarizar el sólido; en su lugar, se puede utilizar luz no polarizada en un campo magnético. [39] En este método, la lana de vidrio se recubre con sal de CsH, lo que aumenta el área de superficie del CsH y, por lo tanto, aumenta las posibilidades de transferencia de espín, lo que produce mejoras 80 veces mayores en campo bajo (0,56 T). [39] Al igual que en la película de CsH hiperpolarizante, en este método de lana de vidrio se permitió que el metal cesio reaccionara con gas hidrógeno, pero en este caso el CsH se formó en las fibras de vidrio en lugar de en la celda de vidrio. [39]
3 También se puede hiperpolarizar mediante bombeo óptico de intercambio de metaestabilidad (MEOP). [ cita necesaria ] Este proceso es capaz de polarizar núcleos de 3 He en el estado fundamental con núcleos de 3 He bombeados ópticamente en el estado metaestable. MEOP solo involucra núcleos de 3 He a temperatura ambiente y a baja presión (≈unos pocos mbar). El proceso de MEOP es muy eficiente (alta tasa de polarización), sin embargo, es necesaria la compresión del gas hasta la presión atmosférica.
Los compuestos que contienen núcleos sensibles a la RMN , como 1 H, 13 C o 15 N , pueden hiperpolarizarse mediante polarización nuclear dinámica (DNP). El DNP generalmente se realiza a baja temperatura (≈1 K) y alto campo magnético (≈3 T). Posteriormente, el compuesto se descongela y se disuelve para producir una solución a temperatura ambiente que contiene núcleos hiperpolarizados. [40] Este líquido se puede utilizar en imágenes metabólicas in vivo [41] para oncología [42] y otras aplicaciones. Los niveles de polarización de 13 C en compuestos sólidos pueden alcanzar hasta ≈64% y las pérdidas durante la disolución y transferencia de la muestra para mediciones de RMN se pueden minimizar a un pequeño porcentaje. [43] Los compuestos que contienen núcleos activos en RMN también se pueden hiperpolarizar mediante reacciones químicas con parahidrógeno , consulte Polarización inducida por parahidrógeno (PHIP).
El hidrógeno molecular, H2 , contiene dos isómeros de espín diferentes , parahidrógeno y ortohidrógeno, con una proporción de 25:75 a temperatura ambiente. La creación de polarización inducida por parahidrógeno (PHIP) [44] significa que esta relación aumenta, en otras palabras, que el parahidrógeno se enriquece. Esto se puede lograr enfriando el gas hidrógeno y luego induciendo la conversión de orto a para mediante un catalizador de óxido de hierro o carbón. Cuando se realiza este procedimiento a ≈70 K (es decir, con nitrógeno líquido), el parahidrógeno se enriquece desde un 25% hasta aprox. 50%. Cuando se enfría por debajo de 20 K y luego se induce la conversión de orto a para, se puede obtener cerca del 100% de parahidrógeno. [ cita necesaria ]
Para aplicaciones prácticas, el PHIP se transfiere más comúnmente a moléculas orgánicas haciendo reaccionar el hidrógeno hiperpolarizado con moléculas precursoras en presencia de un catalizador de metal de transición. Señales de RMN de protones con ca. Se puede obtener una intensidad 10.000 veces mayor [45] en comparación con las señales de RMN de la misma molécula orgánica sin PHIP y, por tanto, sólo con polarización "térmica" a temperatura ambiente.
La amplificación de señal por intercambio reversible (SABRE) es una técnica para hiperpolarizar muestras sin modificarlas químicamente. En comparación con el ortohidrógeno o las moléculas orgánicas, una fracción mucho mayor de los núcleos de hidrógeno en el parahidrógeno se alinea con un campo magnético aplicado. En SABRE, un centro metálico se une reversiblemente tanto a la molécula de prueba como a una molécula de parahidrógeno, lo que facilita que la molécula objetivo capte la polarización del parahidrógeno. [46] Esta técnica se puede mejorar y utilizar para una amplia gama de moléculas orgánicas mediante el uso de una molécula de "retransmisión" intermedia como el amoníaco. El amoníaco se une eficazmente al centro metálico y capta la polarización del parahidrógeno. Luego, el amoníaco le transfiere otras moléculas que no se unen tan bien al catalizador metálico. [47] Esta señal de RMN mejorada permite el análisis rápido de cantidades muy pequeñas de material.