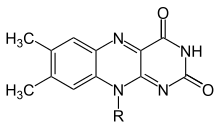

Flavinas (del latín flavus , "amarillo") se refiere generalmente a la clase de compuestos orgánicos que contienen el heterociclo tricíclico isoaloxazina o su isómero aloxazina, y sus derivados. La fuente bioquímica de flavina es la riboflavina de vitamina B amarilla . El resto de flavina a menudo se une a un difosfato de adenosina para formar dinucleótido de flavina y adenina ( FAD ) y, en otras circunstancias, se encuentra como mononucleótido de flavina (o FMN ), una forma fosforilada de riboflavina . Es en una u otra de estas formas que la flavina está presente como grupo protésico en las flavoproteínas . A pesar de los nombres similares, las flavinas (con "i") son química y biológicamente distintas de los flavonoides (con "a") y de los flavonoles (con "o").
El grupo flavina es capaz de sufrir reacciones de oxidación-reducción y puede aceptar un electrón en un proceso de dos pasos o dos electrones a la vez. La reducción se realiza mediante la adición de átomos de hidrógeno a átomos de nitrógeno específicos en el sistema de anillos de isoaloxazina :

En solución acuosa , las flavinas son de color amarillo cuando se oxidan, tomando un color rojo en estado aniónico semireducido o azul en estado neutro ( semiquinona ), e incoloras cuando están totalmente reducidas. [1] Las formas oxidada y reducida están en rápido equilibrio con la forma de semiquinona ( radical ), desplazada en contra de la formación del radical: [2]
donde Fl ox es la flavina oxidada, Fl red H 2 la flavina reducida (tras la adición de dos átomos de hidrógeno) y FlH • la forma de semiquinona (adición de un átomo de hidrógeno).
En forma de FADH 2 , es uno de los cofactores que pueden transferir electrones a la cadena de transferencia de electrones .
Tanto las flavinas libres como las unidas a proteínas son fotorreducibles , es decir, capaces de reducirse por la luz , en un mecanismo mediado por varios compuestos orgánicos, como algunos aminoácidos , ácidos carboxílicos y aminas . [2] Esta propiedad de las flavinas es explotada por varias proteínas sensibles a la luz. Por ejemplo, el dominio LOV, que se encuentra en muchas especies de plantas, hongos y bacterias, sufre un cambio estructural reversible y dependiente de la luz que implica la formación de un enlace entre un residuo de cisteína en su secuencia peptídica y un FMN unido. [3]

El dinucleótido de flavina adenina es un grupo unido a muchas enzimas, incluida la ferredoxina-NADP+ reductasa , la monoaminooxidasa , la D-aminoácido oxidasa , la glucosa oxidasa , la xantina oxidasa y la acil CoA deshidrogenasa .
FADH y FADH 2 son formas reducidas de FAD. FADH 2 se produce como grupo protésico en la succinato deshidrogenasa , una enzima implicada en el ciclo del ácido cítrico . En la fosforilación oxidativa , dos moléculas de FADH 2 normalmente producen 1,5 ATP cada una, o tres ATP combinadas.
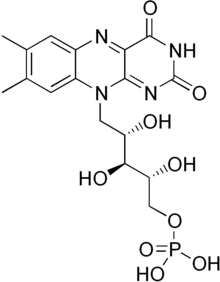
El mononucleótido de flavina es un grupo protésico que se encuentra, entre otras proteínas, en la NADH deshidrogenasa , la nitroreductasa de E. coli y la enzima amarilla antigua .