La aglomeración de partículas se refiere a la formación de conjuntos en una suspensión y representa un mecanismo que conduce a la desestabilización funcional de los sistemas coloidales . Durante este proceso, las partículas dispersas en la fase líquida se adhieren entre sí y forman espontáneamente conjuntos de partículas irregulares, flóculos o aglomerados. Este fenómeno también se conoce como coagulación o floculación y dicha suspensión también se denomina inestable . La aglomeración de partículas se puede inducir añadiendo sales u otros productos químicos denominados coagulantes o floculantes . [1]

La aglomeración de partículas puede ser un proceso reversible o irreversible. Los aglomerados de partículas definidos como "aglomerados duros" son más difíciles de redispersar en las partículas individuales iniciales. Durante la aglomeración, los aglomerados aumentan de tamaño y, como consecuencia, pueden depositarse en el fondo del recipiente, lo que se denomina sedimentación . Alternativamente, se puede formar un gel coloidal en suspensiones concentradas que cambia sus propiedades reológicas . El proceso inverso, mediante el cual los aglomerados de partículas se redispersan como partículas individuales, denominado peptización , rara vez se produce de forma espontánea, sino que puede ocurrir mediante agitación o cizallamiento .
Las partículas coloidales también pueden permanecer dispersas en líquidos durante largos períodos de tiempo (días a años). Este fenómeno se denomina estabilidad coloidal y se dice que dicha suspensión es funcionalmente estable . Las suspensiones estables a menudo se obtienen a bajas concentraciones de sal o mediante la adición de productos químicos denominados estabilizadores o agentes estabilizantes . La estabilidad de las partículas, coloidales o no, se evalúa más comúnmente en términos de potencial zeta . Este parámetro proporciona una medida fácilmente cuantificable de la repulsión entre partículas, que es el inhibidor clave de la agregación de partículas.
También se producen procesos de aglomeración similares en otros sistemas dispersos. En las emulsiones , también pueden acoplarse a la coalescencia de las gotitas , y no sólo conducir a la sedimentación sino también a la formación de crema . En los aerosoles , las partículas en el aire pueden igualmente agregarse y formar grupos más grandes (p. ej., hollín ).
Una suspensión coloidal bien dispersa consta de partículas individuales separadas y está estabilizada por fuerzas de repulsión entre partículas. Cuando las fuerzas repulsivas se debilitan o se vuelven atractivas mediante la adición de un coagulante, las partículas comienzan a agregarse. Inicialmente, los dobletes de partículas A 2 se formarán a partir de singletes A 1 según el esquema [2]
En la etapa inicial del proceso de agregación, la suspensión contiene principalmente partículas individuales. La tasa de este fenómeno se caracteriza por el coeficiente de tasa de agregación k . Dado que la formación de dobletes es un proceso de velocidad de segundo orden , las unidades de estos coeficientes son m 3 s −1, ya que las concentraciones de partículas se expresan como número de partículas por unidad de volumen (m −3 ). Dado que las tasas de agregación absolutas son difíciles de medir, a menudo se hace referencia a la relación de estabilidad adimensional W , definida como
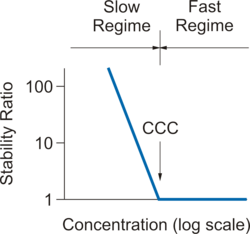
A menudo, las partículas coloidales están suspendidas en agua. En este caso, acumulan una carga superficial y se forma una doble capa eléctrica alrededor de cada partícula. [3] La superposición entre las capas difusas de dos partículas que se acercan da como resultado un potencial de interacción repulsivo de doble capa , que conduce a la estabilización de las partículas. Cuando se agrega sal a la suspensión, se filtra la repulsión eléctrica de la doble capa y la atracción de Van der Waals se vuelve dominante e induce una rápida agregación. La figura de la derecha muestra la dependencia típica del índice de estabilidad W versus la concentración de electrolito, donde se indican los regímenes de agregación lenta y rápida.
La siguiente tabla resume los rangos de concentración crítica de coagulación (CCC) para diferentes cargas netas del contraión . [4] La carga se expresa en unidades de carga elemental . Esta dependencia refleja la regla de Schulze-Hardy, [5] [6] que establece que la CCC varía como la sexta potencia inversa de la carga del contraión. La CCC también depende un poco del tipo de ion, incluso si tienen la misma carga. Esta dependencia puede reflejar diferentes propiedades de las partículas o diferentes afinidades iónicas con la superficie de las partículas. Dado que las partículas suelen estar cargadas negativamente, los cationes metálicos multivalentes representan coagulantes muy eficaces.
La adsorción de especies con carga opuesta (p. ej., protones, específicamente iones adsorbentes, tensioactivos o polielectrolitos ) puede desestabilizar una suspensión de partículas mediante la neutralización de la carga o estabilizarla mediante la acumulación de carga, lo que lleva a una agregación rápida cerca del punto de neutralización de la carga y a una agregación lenta hacia afuera. de eso.
La interpretación cuantitativa de la estabilidad coloidal se formuló por primera vez dentro de la teoría DLVO . [2] Esta teoría confirma la existencia de regímenes de agregación lentos y rápidos, aunque en el régimen lento a menudo se predice que la dependencia de la concentración de sal es mucho más fuerte de lo observado experimentalmente. La regla de Schulze-Hardy también puede derivarse de la teoría DLVO.
Son igualmente posibles otros mecanismos de estabilización coloidal, en particular los que implican polímeros. Los polímeros adsorbidos o injertados pueden formar una capa protectora alrededor de las partículas, inducir fuerzas estéricas repulsivas y conducir a una estabilización estérica, como es el caso del éter de policarboxilato (PCE), la última generación de superplastificantes químicamente diseñados específicamente para aumentar la trabajabilidad del hormigón. reduciendo al mismo tiempo su contenido en agua para mejorar sus propiedades y durabilidad. Cuando las cadenas de polímeros se adsorben libremente a las partículas, una cadena de polímero puede unir dos partículas e inducir fuerzas de puente. Esta situación se conoce como floculación puente.
Cuando la agregación de partículas está impulsada únicamente por la difusión, se habla de agregación pericinética . La agregación se puede mejorar mediante tensión cortante (por ejemplo, agitación). El último caso se llama agregación ortocinética .
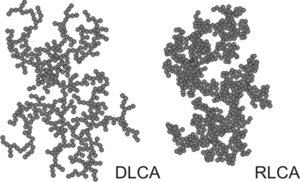
A medida que continúa el proceso de agregación, se forman grupos más grandes. El crecimiento se produce principalmente a través de encuentros entre diferentes clusters, por lo que se habla de proceso de agregación cluster-cluster. Los grupos resultantes son irregulares, pero estadísticamente autosimilares. Son ejemplos de fractales de masa , en los que su masa M crece con su tamaño típico caracterizado por el radio de giro R g como ley de potencia [2]
donde d es la dimensión fractal de masa. Dependiendo de si la agregación es rápida o lenta, se hace referencia a agregación de conglomerados limitada por difusión (DLCA) o agregación de conglomerados limitada por reacción (RLCA). Los clusters tienen características diferentes en cada régimen. Los grupos de DLCA son sueltos y ramificados ( d ≈ 1,8), mientras que los grupos de RLCA son más compactos ( d ≈ 2,1). [7] La distribución del tamaño de los conglomerados también es diferente en estos dos regímenes. Los grupos de DLCA son relativamente monodispersos, mientras que la distribución de tamaño de los grupos de RLCA es muy amplia.
Cuanto mayor sea el tamaño del cúmulo, mayor será su velocidad de sedimentación. Por lo tanto, las partículas agregadas sedimentan y este mecanismo proporciona una forma de separarlas de la suspensión. En concentraciones de partículas más altas, los grupos en crecimiento pueden interconectarse y formar un gel de partículas. Tal gel es un cuerpo sólido elástico, pero se diferencia de los sólidos ordinarios por tener un módulo elástico muy bajo .
Cuando la agregación ocurre en una suspensión compuesta de partículas coloidales monodispersas similares, el proceso se llama homoagregación (u homocoagulación ). Cuando la agregación ocurre en una suspensión compuesta de partículas coloidales diferentes, se habla de heteroagregación (o heterocoagulación ). El proceso de heteroagregación más simple ocurre cuando se mezclan dos tipos de partículas coloidales monodispersas. En las primeras etapas, se pueden formar tres tipos de dobletes: [8]
Mientras que los dos primeros procesos corresponden a la homoagregación en suspensiones puras que contienen partículas A o B, la última reacción representa el proceso de heteroagregación real. Cada una de estas reacciones se caracteriza por los respectivos coeficientes de agregación k AA , k BB y k AB . Por ejemplo, cuando las partículas A y B tienen carga positiva y negativa, respectivamente, las tasas de homoagregación pueden ser lentas, mientras que la tasa de heteroagregación es rápida. A diferencia de la homoagregación, la tasa de heteroagregación se acelera al disminuir la concentración de sal. Los grupos formados en etapas posteriores de tales procesos de heteroagregación están aún más ramificados que los obtenidos durante DLCA ( d ≈ 1,4). [9]
Un caso especial importante de un proceso de heteroagregación es la deposición de partículas sobre un sustrato. [1] Las primeras etapas del proceso corresponden a la unión de partículas individuales al sustrato, que pueden representarse como otra partícula mucho más grande. Las etapas posteriores pueden reflejar el bloqueo del sustrato a través de interacciones repulsivas entre las partículas, mientras que las interacciones atractivas pueden conducir a un crecimiento multicapa, lo que también se conoce como maduración. Estos fenómenos son relevantes en el ensuciamiento de membranas o filtros .
Se han desarrollado numerosas técnicas experimentales para estudiar la agregación de partículas. Las más utilizadas son las técnicas ópticas de resolución temporal que se basan en la transmitancia o dispersión de la luz. [10]
Transmision de luz. La variación de la luz transmitida a través de una suspensión agregante se puede estudiar con un espectrofotómetro normal en la región visible. A medida que avanza la agregación, el medio se vuelve más turbio y aumenta su absorbancia . El aumento de la absorbancia se puede relacionar con la constante k de la tasa de agregación y la relación de estabilidad se puede estimar a partir de tales mediciones. La ventaja de esta técnica es su simplicidad.
Dispersión de la luz. Estas técnicas se basan en explorar la luz dispersada de una suspensión de agregación de forma resuelta en el tiempo. La dispersión de la luz estática produce el cambio en la intensidad de la dispersión, mientras que la dispersión de la luz dinámica produce la variación en el radio hidrodinámico aparente. En las primeras etapas de agregación, la variación de cada una de estas cantidades es directamente proporcional a la constante de tasa de agregación k . [11] En etapas posteriores, se puede obtener información sobre los grupos formados (por ejemplo, dimensión fractal). [7] La dispersión de la luz funciona bien para una amplia gama de tamaños de partículas. Es posible que sea necesario considerar múltiples efectos de dispersión, ya que la dispersión se vuelve cada vez más importante para partículas o agregados más grandes. Estos efectos pueden despreciarse en suspensiones débilmente turbias. Los procesos de agregación en sistemas de fuerte dispersión se han estudiado con técnicas de transmitancia , retrodispersión o espectroscopia de ondas de difusión .
Conteo de partículas individuales. Esta técnica ofrece una resolución excelente, mediante la cual los grupos formados por décimas de partículas se pueden resolver individualmente. [11] La suspensión agregante se fuerza a través de un contador de partículas capilares estrecho y el tamaño de cada agregado se analiza mediante dispersión de luz. A partir de la intensidad de dispersión, se puede deducir el tamaño de cada agregado y construir una distribución detallada del tamaño de los agregados. Si las suspensiones contienen altas cantidades de sal, también se puede utilizar un contador Coulter . A medida que pasa el tiempo, la distribución del tamaño se desplaza hacia agregados más grandes, y de esta variación se pueden deducir tasas de agregación y ruptura que involucran diferentes conglomerados. La desventaja de esta técnica es que los agregados son forzados a través de un capilar estrecho bajo condiciones de alto cizallamiento, y los agregados pueden romperse en estas condiciones.
Técnicas indirectas. Como muchas propiedades de las suspensiones coloidales dependen del estado de agregación de las partículas suspendidas, también se han utilizado varias técnicas indirectas para controlar la agregación de partículas. Si bien puede resultar difícil obtener información cuantitativa sobre las tasas de agregación o las propiedades de los grupos a partir de tales experimentos, pueden ser muy valiosos para aplicaciones prácticas. Entre estas técnicas las pruebas de resolución son las más relevantes. Cuando se inspecciona una serie de tubos de ensayo con suspensiones preparadas con diferentes concentraciones de floculante, las suspensiones estables a menudo permanecen dispersas, mientras que las inestables se sedimentan. Se han desarrollado instrumentos automatizados basados en la dispersión/transmitancia de la luz para monitorear la sedimentación de la suspensión, y pueden usarse para sondear la agregación de partículas. Sin embargo, hay que tener en cuenta que es posible que estas técnicas no siempre reflejen correctamente el estado de agregación real de una suspensión. Por ejemplo, las partículas primarias más grandes pueden sedimentar incluso en ausencia de agregación, o los agregados que han formado un gel coloidal permanecerán en suspensión. Otras técnicas indirectas capaces de controlar el estado de agregación incluyen, por ejemplo, la filtración , la reología , la absorción de ondas ultrasónicas o las propiedades dieléctricas . [10]
La agregación de partículas es un fenómeno generalizado que ocurre espontáneamente en la naturaleza pero que también se explora ampliamente en la fabricación. Algunos ejemplos incluyen.
Formación del delta del río . Cuando el agua del río que transporta partículas de sedimentos en suspensión llega al agua salada, la agregación de partículas puede ser uno de los factores responsables de la formación del delta del río. Las partículas cargadas son estables en el agua dulce del río que contiene bajos niveles de sal, pero se vuelven inestables en el agua de mar que contiene altos niveles de sal. En este último medio, las partículas se agregan, los agregados más grandes se sedimentan y así crean el delta del río.
Fabricación de papel . Se añaden agentes de retención a la pulpa para acelerar la formación del papel. Estos coadyuvantes son coadyuvantes de coagulación que aceleran la agregación entre las fibras de celulosa y las partículas de relleno. Con frecuencia se utilizan para ello polielectrolitos catiónicos.
Tratamiento de aguas . El tratamiento de aguas residuales municipales normalmente incluye una fase en la que se eliminan las partículas sólidas finas. Esta separación se logra mediante la adición de un agente floculante o coagulante, que induce la agregación de los sólidos en suspensión. Los áridos normalmente se separan por sedimentación, lo que da lugar a lodos de depuradora. Los agentes floculantes comúnmente utilizados en el tratamiento del agua incluyen iones metálicos multivalentes (p. ej., Fe 3+ o Al 3+ ), polielectrolitos o ambos.
Elaboración de queso . El paso clave en la producción de queso es la separación de la leche en cuajada sólida y suero líquido. Esta separación se consigue induciendo los procesos de agregación entre micelas de caseína acidificando la leche o añadiendo cuajo. La acidificación neutraliza los grupos carboxilato de las micelas e induce la agregación.