En un análisis químico , el método del estándar interno implica agregar la misma cantidad de una sustancia química a cada muestra y solución de calibración . El estándar interno responde proporcionalmente a los cambios en el analito y proporciona una señal de medición similar, pero no idéntica. También debe estar ausente de la matriz de la muestra para garantizar que no haya otra fuente del estándar interno presente. Tomando la relación entre la señal del analito y la señal del estándar interno y graficandola contra las concentraciones del analito en las soluciones de calibración se obtendrá una curva de calibración . La curva de calibración se puede utilizar luego para calcular la concentración del analito en una muestra desconocida. [1]
La selección de un estándar interno adecuado tiene en cuenta las fuentes aleatorias y sistemáticas de incertidumbre que surgen durante la preparación de la muestra o la fluctuación del instrumento. Esto se debe a que la relación entre el analito y la cantidad de estándar interno es independiente de estas variaciones. Si el valor medido del analito se desplaza por error por encima o por debajo del valor real, las mediciones del estándar interno deberían desplazarse en la misma dirección. [1]
El gráfico de relación proporciona una buena manera de compensar la variación de la sensibilidad del detector, pero puede estar sesgado y debe reemplazarse por cálculos de concentración relativa/calibración relativa si la razón de la variabilidad de la respuesta está en una masa diferente de la muestra analizada y la curva de calibración tradicional (no estándar interna) de cualquier analito no es lineal a través del origen. [2]
El primer uso registrado del método del estándar interno se remonta al trabajo de espectroscopia de llama de Gouy en 1877, donde utilizó un estándar interno para determinar si la excitación en su llama era consistente. [3] [4] Su procedimiento experimental se reintrodujo más tarde en la década de 1940, cuando los fotómetros de llama de registro se volvieron fácilmente disponibles. [3] El uso de estándares internos continuó creciendo y se aplicó a una amplia gama de técnicas analíticas, incluida la espectroscopia de resonancia magnética nuclear (RMN) , la cromatografía y la espectroscopia de plasma acoplado inductivamente .
En la espectroscopia de RMN, por ejemplo, de los núcleos 1H , 13C y 29Si , las frecuencias dependen del campo magnético, que no es el mismo en todos los experimentos. Por lo tanto, las frecuencias se informan como diferencias relativas al tetrametilsilano (TMS), un estándar interno que George Tiers propuso en 1958 y que la Unión Internacional de Química Pura y Aplicada ha respaldado desde entonces. [5] [6] La diferencia relativa con el TMS se denomina desplazamiento químico . [7]
El TMS funciona como un estándar ideal porque es relativamente inerte y sus protones de metilo idénticos producen una fuerte señal de campo ascendente, aislada de la mayoría de los otros protones. [7] Es soluble en la mayoría de los solventes orgánicos y se puede eliminar mediante destilación debido a su bajo punto de ebullición. [1]
En la práctica, se conoce la diferencia entre las señales de los disolventes comunes y las de TMS. Por lo tanto, no es necesario añadir TMS a los disolventes deuterados comerciales , ya que los instrumentos modernos son capaces de detectar las pequeñas cantidades de disolvente protonado presentes. Al especificar el disolvente de bloqueo que se utilizará, los espectrómetros modernos pueden referenciar correctamente la muestra; de hecho, el propio disolvente sirve como estándar interno. [1]
En cromatografía, los estándares internos se utilizan para determinar la concentración de otros analitos mediante el cálculo del factor de respuesta . El estándar interno seleccionado debe tener un tiempo de retención y derivatización similares . Debe ser estable y no interferir con los componentes de la muestra. Esto mitiga la incertidumbre que puede ocurrir en los pasos preparatorios, como la inyección de la muestra. [1]
En la cromatografía de gases-espectrometría de masas (GC-MS), los compuestos deuterados con estructuras similares al analito actúan comúnmente como estándares internos efectivos. [8] Sin embargo, existen estándares internos no deuterados como la norleucina , que es popular en el análisis de aminoácidos porque se puede separar de los picos que la acompañan. [9] [10] [11]
La selección de un estándar interno para cromatografía líquida-espectrometría de masas (LC-MS) depende del método de ionización empleado. El estándar interno necesita una respuesta de ionización y un patrón de fragmentación comparables a los del analito. [12] Los estándares internos de LC-MS suelen ser isotópicamente análogos a la estructura del analito, utilizando isótopos como el deuterio ( 2 H), 13 C, 15 N y 18 O. [13]
La selección de un estándar interno en la espectroscopia de plasma acoplado inductivamente puede ser difícil, porque las señales de la matriz de la muestra pueden superponerse con las del analito. El itrio es un estándar interno común que está naturalmente ausente en la mayoría de las muestras. Tiene una masa de rango medio y líneas de emisión que no interfieren con muchos analitos. La intensidad de la señal de itrio es con lo que se compara la señal del analito. [1] [14]
En la espectrometría de masas con plasma acoplado inductivamente (ICP-MS), las especies con una masa similar a la del analito suelen servir como buenos estándares internos, aunque no en todos los casos. Los factores que también contribuyen a la eficacia de un estándar interno en la ICP-MS incluyen la proximidad de su potencial de ionización , el cambio de entalpía y el cambio de entropía al analito. [15]
Los estándares internos de la espectroscopia de emisión óptica con plasma acoplado inductivamente (ICP-OES) se pueden seleccionar observando cómo cambian las señales del analito y del estándar interno con distintas condiciones experimentales. Esto incluye realizar ajustes en la matriz de muestra o en la configuración de la instrumentación y evaluar si el estándar interno seleccionado está reaccionando de la misma manera que el analito. [16]
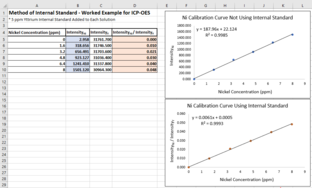
Una forma de visualizar el método de estándar interno es crear una curva de calibración que no utilice el método y una curva de calibración que sí lo utilice. Supongamos que existen concentraciones conocidas de níquel en un conjunto de soluciones de calibración: 0 ppm, 1,6 ppm, 3,2 ppm, 4,8 ppm, 6,4 ppm y 8 ppm. Cada solución también tiene 5 ppm de itrio para actuar como estándar interno. Si estas soluciones se miden utilizando ICP-OES, la intensidad de la señal de itrio debería ser constante en todas las soluciones. De lo contrario, es probable que la intensidad de la señal de níquel también sea imprecisa.
La curva de calibración que no utiliza el método de patrón interno ignora la incertidumbre entre mediciones. El coeficiente de determinación (R 2 ) para esta gráfica es 0,9985.
En la curva de calibración que utiliza el estándar interno, el eje y es la relación entre la señal de níquel y la señal de itrio. Esta relación no se ve afectada por la incertidumbre en las mediciones de níquel, ya que debería afectar a las mediciones de itrio de la misma manera. Esto da como resultado un R 2 más alto , 0,9993.