Un electrodo de ion selectivo ( ISE ), también conocido como electrodo de ion específico ( SIE ), es un transductor (o sensor ) que convierte el cambio en la concentración de un ion específico disuelto en una solución en un potencial eléctrico . En teoría, la tensión depende del logaritmo de la actividad iónica, según la ecuación de Nernst . Los electrodos selectivos de iones se utilizan en química analítica e investigación bioquímica / biofísica , donde se requieren mediciones de la concentración iónica en una solución acuosa . [1]
Hay cuatro tipos principales de membranas selectivas de iones que se utilizan en electrodos selectivos de iones (ISE): vidrio, estado sólido, base líquida y electrodo compuesto. [2] [3]
Las membranas de vidrio están hechas de un tipo de vidrio de intercambio iónico ( silicato o calcogenuro ). Este tipo de ISE tiene buena selectividad , pero sólo para varios cationes con carga única ; principalmente H + , Na + y Ag + . El vidrio calcogenuro también tiene selectividad por iones metálicos de doble carga, como Pb 2+ y Cd 2+ . La membrana de vidrio tiene una excelente durabilidad química y puede funcionar en medios muy agresivos. Un ejemplo muy común de este tipo de electrodo es el electrodo de vidrio de pH .
Las membranas cristalinas están hechas de monocristalitos o policristalitos de una sola sustancia. Tienen una buena selectividad, porque sólo los iones que pueden introducirse en la estructura cristalina pueden interferir en la respuesta del electrodo . Ésta es la principal diferencia entre este tipo de electrodos y los electrodos de membrana de vidrio. La falta de solución interna reduce las uniones potenciales. La selectividad de las membranas cristalinas puede ser tanto para el catión como para el anión de la sustancia formadora de la membrana. Un ejemplo es el electrodo selectivo de fluoruro basado en cristales de LaF 3 .
Las resinas de intercambio iónico se basan en membranas de polímeros orgánicos especiales que contienen una sustancia de intercambio iónico específica (resina). Este es el tipo más extendido de electrodo de ion específico. El uso de resinas específicas permite la preparación de electrodos selectivos para decenas de iones diferentes, tanto de un solo átomo como de múltiples átomos. También son los electrodos con selectividad aniónica más extendidos. Sin embargo, dichos electrodos tienen una durabilidad química y física baja, así como un "tiempo de supervivencia". Un ejemplo es el electrodo selectivo de potasio , basado en valinomicina como agente de intercambio iónico.
Los electrodos enzimáticos no son verdaderos electrodos selectivos de iones , pero generalmente se consideran dentro del alcance de los electrodos selectivos de iones. Un electrodo de este tipo tiene un mecanismo de "doble reacción": una enzima reacciona con una sustancia específica y el producto de esta reacción (normalmente H + u OH − ) se detecta mediante un verdadero electrodo selectivo de iones, como los electrodos selectivos de pH. . Todas estas reacciones ocurren dentro de una membrana especial, que cubre el verdadero electrodo selectivo de iones. Esta es la razón por la que los electrodos enzimáticos a veces se consideran selectivos para los iones. Un ejemplo es un electrodo selectivo de glucosa .
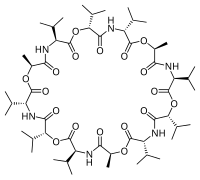
Se han desarrollado electrodos específicos para cada ion de metal alcalino, Li + , Na + , K + , Rb + y Cs + . El principio en el que se basan estos electrodos es que el ión de metal alcalino está encapsulado en una cavidad molecular cuyo tamaño se adapta al tamaño del ión. Por ejemplo, se puede utilizar un electrodo basado en valinomicina para la determinación de la concentración de iones potasio. [4]