El cloruro de hierro (II) , también conocido como cloruro ferroso , es el compuesto químico de fórmula FeCl 2 . Es un sólido paramagnético con un alto punto de fusión. El compuesto es blanco, pero las muestras típicas suelen ser blanquecinas. El FeCl 2 cristaliza en el agua como tetrahidrato verdoso , que es la forma que se encuentra más comúnmente en el comercio y el laboratorio. También hay un dihidrato. El compuesto es muy soluble en agua y produce soluciones de color verde pálido.

Las formas hidratadas de cloruro ferroso se generan mediante el tratamiento de residuos de la producción de acero con ácido clorhídrico . Estas soluciones se denominan "ácido gastado" o "licor de encurtido", especialmente cuando el ácido clorhídrico no se consume por completo:
La producción de cloruro férrico implica el uso de cloruro ferroso. El cloruro ferroso también es un subproducto de la producción de titanio, ya que algunos minerales de titanio contienen hierro. [3]
El cloruro ferroso se prepara añadiendo polvo de hierro a una solución de ácido clorhídrico en metanol. Esta reacción da el solvato de metanol del dicloruro, que al calentarlo al vacío a aproximadamente 160 °C se convierte en FeCl 2 anhidro . [4] La reacción neta se muestra:
De manera análoga se pueden preparar FeBr 2 y FeI 2 .
Una síntesis alternativa de cloruro ferroso anhidro es la reducción de FeCl 3 con clorobenceno : [5]
Para la preparación de ferroceno, el cloruro ferroso se genera in situ mediante la comparación de FeCl 3 con polvo de hierro en tetrahidrofurano (THF). [6] El cloruro férrico se descompone en cloruro ferroso a altas temperaturas.
El dihidrato, FeCl 2 (H 2 O) 2 , cristaliza en ácido clorhídrico concentrado. [7] El dihidrato es un polímero de coordinación . Cada centro de Fe está coordinado con cuatro ligandos de cloruro de doble puente . El octaedro se completa con un par de ligandos mutuamente transaquo . [8]

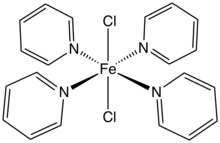
FeCl 2 y sus hidratos forman complejos con muchos ligandos. Por ejemplo, las soluciones de los hidratos reaccionan con dos equivalentes molares de [(C 2 H 5 ) 4 N]Cl para dar la sal [(C 2 H 5 ) 4 N] 2 [FeCl 4 ]. [10]
El FeCl 2 anhidro , que es soluble en THF, [2] es un precursor estándar en la síntesis organometálica. FeCl 2 se utiliza para generar complejos de NHC in situ para reacciones de acoplamiento cruzado . [11]
A diferencia del sulfato ferroso y el cloruro férrico relacionados , el cloruro ferroso tiene pocas aplicaciones comerciales. Además de su uso en la síntesis de complejos de hierro en laboratorio, el cloruro ferroso sirve como agente de coagulación y floculación en el tratamiento de aguas residuales , especialmente para desechos que contienen cromatos o sulfuros . [12] Se utiliza para el control de olores en el tratamiento de aguas residuales. Se utiliza como precursor para fabricar diversos grados de hematita que se pueden utilizar en una variedad de pigmentos. Es el precursor de los óxidos de hierro (III) hidratados que son pigmentos magnéticos. [3] El FeCl 2 encuentra algún uso como reactivo en la síntesis orgánica . [13]
La lawrencita, (Fe,Ni)Cl 2 , es la contraparte natural y un mineral meteorítico típico (aunque poco frecuente). [14] La forma natural del dihidrato es la rokühnita, un mineral muy raro. [15] Los minerales relacionados, pero más complejos (en particular, básicos o hidratados) son la hibbingita , la droninoita y la kuliginita.
{{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda ){{cite book}}: |journal=ignorado ( ayuda )