Disheveled ( Dsh ) es una familia de proteínas involucradas en vías de señalización Wnt canónicas y no canónicas . Dsh (Dvl en mamíferos) es una fosfoproteína citoplasmática que actúa directamente aguas abajo de los receptores encrespados . [1] Toma su nombre de su descubrimiento inicial en moscas , donde se observó que una mutación en el gen desaliñado causaba una orientación inadecuada de los pelos del cuerpo y de las alas. [2] Hay homólogos de vertebrados en el pez cebra, Xenopus ( Xdsh ), ratones ( Dvl1, -2, -3 ) y humanos ( DVL-1, -2, -3 ). Dsh transmite señales Wnt complejas en tejidos y células, en contextos normales y anormales. [2] [3] Se cree que interactúa con la proteína SPATS1 cuando regula la vía de señalización Wnt. [4]
El desaliñado juega papeles importantes tanto en el embrión como en el adulto, que van desde la diferenciación celular y la polaridad celular hasta el comportamiento social. [2]
Hay tres genes humanos que codifican las proteínas desaliñadas: [5]
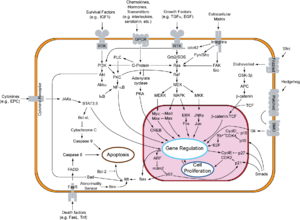
DVL es una parte integral de la vía canónica Wnt (dependiente de β-catenina) y de la vía no canónica (independiente de β-catenina). [2] En cualquiera de estos, DVL actúa corriente abajo de un receptor Frizzled, aunque las vías son distintas. [6]
La vía canónica Wnt, también conocida como vía Wnt/β-catenina, se activa durante el desarrollo, la regulación, la diferenciación celular y la proliferación. [7] La vía canónica Wnt mueve DVL entre el citoplasma y el núcleo, a través de una secuencia de exportación nuclear conservada (NES) y una secuencia de localización nuclear (NLS), ambas necesarias para el funcionamiento adecuado. [3] La unión de Wnt a los receptores Frizzled ayuda a reclutar DVL en la membrana, proporcionando un sitio para que Axin y GSK3β se unan y fosforilen LRP5/6 (proteína transmembrana relacionada con el receptor de lipoproteínas de baja densidad), evitando la degradación constitutiva de β-catenina. . [6] [7] La prevención de esta degradación mediante DVL permite la acumulación de β-catenina en el núcleo, donde actúa como un coactivador para que TCF (factor de células T) active genes que responden a Wnt. [3] [7] Por el contrario, sin señalización Wnt, el complejo de destrucción, formado por APC, CKI, GSK3β y Axin, degrada la acumulación de β-catenina, manteniendo baja la concentración de β-catenina en la célula. [7]
La vía de polaridad celular plana (PCP) es la vía independiente de β-catenina más notable: la señal Wnt es recibida por el receptor Frizzled, que transmite señales a DVL, que luego actúa como un punto de ramificación para dos vías independientes, lo que conduce a la activación. de pequeñas GTPasas Rho y Rac. [3] [7] Para la rama Rho, las señales Wnt inducen a DVL a formar un complejo con Daam1 (activador asociado desaliñado de la morfogénesis 1). [3] Este complejo luego interactúa con el factor de intercambio de nucleótidos de guanina Rho WGEF (GEF de similitud débil), que activa efectores posteriores como Rho GTPasa y Rho-associated kinase (ROCK), que activa la arquitectura de actina y citoesqueleto en la célula. Para la rama Rac, DVL activa la Rac GTPasa. [3] La activación de la Rac GTPasa estimula la quinasa N-terminal c-Jun (JNK) efectora aguas abajo, que controla los reordenamientos en el citoesqueleto y la expresión genética. [7] Más específicamente, regula la polaridad y el movimiento de una célula, en procesos en vertebrados (como Xenopus), incluida la gastrulación, el cierre del tubo neural y la orientación de los estereocilios en el oído interno. [7]
Otra vía independiente de la β-catenina es la vía Wnt-Ca 2+ , que participa en el cáncer, la inflamación y la neurodegeneración. Wnt desencadena la activación mediada por Frizzled, lo que desencadena una cascada que conduce a la liberación de Ca 2+ , que activa efectores (por ejemplo, CaMKII ) que controlan la transcripción de genes relevantes para el destino celular y la migración celular. [7] Esta vía puede desactivar la cascada Wnt/β-catenina y también puede inhibirse mediante la activación de DVL. [8]
Hay cinco regiones principales altamente conservadas que existen en todas las variaciones de DVL. Estos incluyen un dominio DIX (N-terminal) amino terminal, un dominio PDZ (central), un dominio DEP (terminal C) carboxilo terminal y dos regiones con residuos de aminoácidos cargados positivamente. [3] Hay una región rica en prolina entre los dominios DIX y PDZ, y una región en gran medida básica entre los dominios DIX y PDZ que ha conservado residuos de serina y treonina. Estas regiones median las interacciones proteína-proteína y ayudan a DVL a canalizar señales hacia la vía independiente de β-catenina o β-catenina. [3] Además, existe la secuencia de exportación nuclear conservada (NES) y una secuencia de localización nuclear (NLS), cuya capacidad para mover DVL entre el citoplasma y el núcleo puede ser una parte importante de su función. [3]

Ubicado cerca de la región N-terminal de DVL y que consta de aproximadamente 82-85 aminoácidos para la proteína DVL humana, DIX se encuentra en proteínas como Axin y la proteína en espiral que contiene el dominio DIX I (DIXdc1 o Ccd1). El dominio DIX de DVL tiene cinco cadenas β y una hélice α con residuos de aminoácidos altamente conservados. [3] [6]
PDZ, cuyo nombre consta de las iniciales de las tres primeras proteínas identificadas que comparten este dominio estructural común ( proteína de densidad post sináptica (PSD95), supresor de tumores grandes del disco D rosophila (Dlg1) y proteína Z onula occludens-1 (zo-1). )), se encuentra en la región central de DVL. PDZ normalmente tiene alrededor de 73 aminoácidos en cada proteína DVL humana y consta de 5-6 cadenas β y 2-3 hélices α [3] [6] Este motivo desempeña un papel fundamental en la unión del ligando y las propiedades conformacionales de la DVL. proteína. Esta región media muchas interacciones proteína-proteína y regula múltiples procesos biológicos. [3]
DEP, que se encuentra en el dominio C-terminal de DVL, tiene 75 aminoácidos en las proteínas DVL humanas y tiene tres hélices α, un brazo de horquilla β y dos hebras β cortas. [3] [6] Este dominio permite la interacción entre DVL y DAAM1, activando así la vía no canónica. Este dominio también tiene resultados que respaldan las afirmaciones de que el dominio DEP es el responsable de dirigir las proteínas DVL a la membrana tras la estimulación de la señal Wnt. El dominio DEP también puede ser esencial para el ensamblaje de señalosomas funcionales y para la transducción de señales Wnt al núcleo. [3]
Además de estas regiones conservadas, DVL tiene tanto NES como NLS, que regulan la localización celular de DVL mediante el movimiento entre el núcleo y el citoplasma. El NLS está entre los dominios PDZ y DEP, y el NES está entre el DEP y el extremo C de DVL. [3]
Hay tres tipos principales de modificación postraduccional de DVL : fosforilación, ubiquitinación y metilación. La fosforilación es la mejor estudiada y parece actuar de tal manera que la fosforilación específica de un sitio puede provocar una amplia variedad de respuestas biológicas. [3] La ubiquitinación es la modificación postraduccional que tiene un papel en la regulación de la degradación de DVL.