El trióxido de renio u óxido de renio (VI) es un compuesto inorgánico con la fórmula ReO 3 . Es un sólido rojo con un brillo metálico que se asemeja al cobre en apariencia. Es el único trióxido estable de los elementos del Grupo 7 ( Mn , Tc , Re ).
El trióxido de renio se puede formar reduciendo el óxido de renio (VII) con monóxido de carbono a 200 °C o renio elemental a 400 °C. [1]
El Re 2 O 7 también se puede reducir con dioxano . [2]
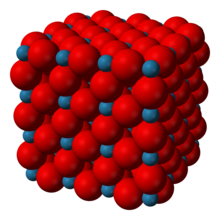

El trióxido de renio cristaliza con una celda unitaria cúbica primitiva , con un parámetro reticular de 3,742 Å (374,2 pm ). La estructura de ReO 3 es similar a la de la perovskita (ABO 3 ), sin el gran catión A en el centro de la celda unitaria. Cada centro de renio está rodeado por un octaedro definido por seis centros de oxígeno. Estos octaedros comparten vértices para formar la estructura tridimensional. El número de coordinación de O es 2, porque cada átomo de oxígeno tiene 2 átomos de Re vecinos. [3]
El ReO 3 es inusual para un óxido porque exhibe una resistividad muy baja . Se comporta como un metal en el sentido de que su resistividad disminuye a medida que disminuye su temperatura. A 300 K , su resistividad es de 100,0 nΩ·m , mientras que a 100 K, esta disminuye a 6,0 nΩ·m, 17 veces menos que a 300 K. [3]
El trióxido de renio es insoluble en agua, así como en ácidos y bases diluidos. Al calentarlo en una base se produce una desproporción que da lugar a ReO
2y ReO−
4, mientras que la reacción con ácido a alta temperatura produce Re
2Oh
7En ácido nítrico concentrado, produce ácido perrénico . Al calentarlo a 400 °C al vacío, sufre una desproporción : [2]
El trióxido de renio se puede clorar para dar cloruro de trióxido de renio : [4]
El trióxido de renio encuentra cierto uso en la síntesis orgánica como catalizador para la reducción de amida . [5]